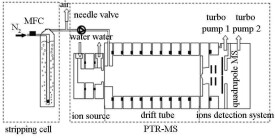
亨利常數
亨利常數
亨利常數,是指一定溫度下溶於定量液體中的氣體量正比於與溶液處於平衡的該氣體分壓。亨利常數亦可作為描述化合物在氣液兩相中分配能力的物理常數,有機物在氣液兩相中的遷移方向和速率主要取決於亨利常數的大小。根據有機物的亨利常數可以判斷氣體在液體中的溶解度(溫度一定時,同一溶劑中亨利常數大者難溶)、液體的揮發作用和在多介質環境中的遷移及趨勢。亨利常數還是環境修復、吸附平衡等過程的關鍵參數,在環境科學與工程領域有廣泛的應用。目前測定亨利常數的方法主要有利用平衡后的頂空氣濃度比來計算的靜態平衡法、色譜法、定量結構-性質相關法等。