摩爾體積
摩爾物質的體積
摩爾體積是指單位物質的量的某種物質的體積,也就是一摩爾物質的體積。理想中一摩爾氣體在標準大氣壓下的體積為22.4L,較精確的是Vm=22.41410L/mol。1摩爾任何物質所含的結構微粒數目為6.02×10。1摩爾物質的質量叫做摩爾質量。1摩爾的原子,它的質量如以克作單位,則數值上等於它的原子量(相當於舊單位中的克原子量);1摩爾的分子,它的質量如以克作單位,則數值上等於它的分子量(相當於舊單位中的克分子量)。
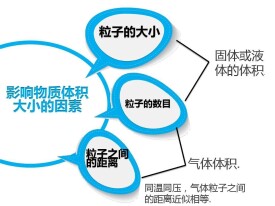
摩爾物質的體積。各種固態或液態物質的摩爾體積是不同的,因為固態或液態物質微粒間的距離是很小的,摩爾體積決定於微粒的大小,不同物質的原子、分子、離子大小不同,它們的摩爾體積當然不同。但氣態物質在相同的溫度和壓力下的摩爾體積卻幾乎相等。因為氣態物質微粒間的距離要比微粒本身大得多,所以氣體的摩爾體積決定於微粒間的平均距離,它決定於氣體的溫度和壓力而與氣體的其他性質無關。在標準狀況下(0℃、1大氣壓)氣體的摩爾體積約為22.4升,理想氣體的摩爾體積的精確值為22.41383升。
摩爾體積=V÷n
V為物質體積(單位:L);n為物質的量(單位:mol)氣體摩爾體積。
理想中一摩爾氣體在標準大氣壓下的體積為22.4L,較精確的是:Vm=22.41410L/mol。
使用時應注意:
①必須是標準狀況(101kpa、0℃)。
②“任何氣體”既包括純凈物又包括氣體混合物。
③22.4升是個近似數值。
④單位是升/摩爾(L/mol),而不是升(L)。
單位物質的量的氣體所佔的體積叫做氣體摩爾體積,相同氣體摩爾體積的氣體其含有的粒子數也相同。氣體摩爾體積不是固定不變的,它決定於氣體所處的溫度和壓強如在25度101千帕時氣體摩爾體積為24.5升/摩爾,在外界條件相同的情況下,氣體的摩爾體積相同。
氣體摩爾體積Vm與T、P、n等之間關係:
1、同溫度、同壓強下,V相同,則N相同,n相同。
2、同溫度、同壓強下,V1/V2=n1/n2=N1/N2。
3、P·V=n·R·T。
如果物質是由原子組成的,那麼這種物質的摩爾質量就是6.022×10¨個原子的質量,在數值上就等予這種元素的原子量,單位為克/摩爾(相當於克原予量的概念。本書中摩爾質量、克原子量的概念均有使用)。
如果物質是由分子組成的,那麼這種物質的摩爾質量就是6.022×10¨個分子的質量,在數值上就等於該物質的分子量,單位為克/摩爾(相當子克分子量的概念。本書中摩爾質量、克分子量的概念均有使用)。
例如:1摩爾Fe的質量為55.85克,即55.85克/摩爾。1摩爾H2O的質量為18克,即18克/摩爾。1摩爾H2SO4的質量為98克,即98克/摩爾。因此在一定量的物質中所含有幾個摩爾即摩爾數,可以用下式計算:摩爾數=物質的質量(克)該物質的摩爾質量(克/摩爾)或,物質的質量(克)=摩爾數×摩爾質量(克/摩爾)。摩爾數可以是整數,也可以不是整數。物質的當量以克作單位,稱為該物質的克當量。物質的質量與克當量、克當量數之間有如下的關係:物質的克當量數=物質的質量(克)該物質的克當量