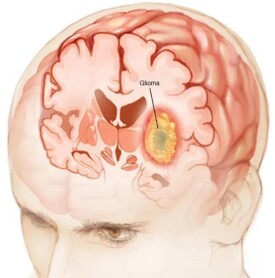
惡性腦膠質瘤
最常見的顱內惡性腫瘤
源自神經上皮的腫瘤統稱為腦膠質瘤(膠質細胞瘤),占顱腦腫瘤的40-50%,是最常見的顱內惡性腫瘤。根據病理又可分為星形細胞瘤、髓母細胞瘤、多形膠母細胞瘤、室管膜瘤、少枝膠母細胞瘤等。
此類腫瘤生長部位、惡性程度不同。惡性腦膠質瘤是臨床上常見的一類顱腦腫瘤,其發病率在顱腦腫瘤中高達60%。
手術切除為本,有些易複發。腦膠質瘤主要以浸潤性方式生長,擴散速度快,因此加重臨床治療困難,手術治療的關鍵是切除腫瘤的同時延長患者生存期,但手術難以將其全部切除,複發性極高,因此,惡性腦質瘤術后聯合化療是極為重要的。
根據現如今的WHO分型標準,膠質瘤被分為四種組織學等級。
膠質瘤Ⅰ級,例如毛細胞型星形細胞瘤是生長非常緩慢的腫瘤,若此型腫瘤得到完全切除,患者則有治癒的可能。
膠質瘤Ⅱ級(常見的有少突星形細胞瘤、星形細胞瘤等)。
侵襲性的Ⅲ級膠質瘤(間變性星形細胞瘤、間變性少突膠質細胞瘤等)處於中間臨床病變過程。
Ⅳ級膠質瘤(惡性膠質瘤)則具有高度的侵襲性(中位生存期為14.5~16.6個月)。
腦膠質瘤是由於大腦和脊髓膠質細胞癌變所產生的、最常見的原發性顱腦腫瘤,影響腦組織功能,早期可表現為刺激癥狀如局限性癲癇,後期表現為神經功能缺失癥狀如癱瘓,對人類健康事業造成巨大威脅。
顱內良性 膠質瘤是指生長在顱內某一部位(多在腦神經組織外),細胞分化良好,生長緩慢,多能根治的腫瘤。而顱內惡性膠質瘤則相反(大都生長在腦神經組織內),細胞分化不良,生長迅速,難以根治。有些顱內良性腫瘤,由於位置深在,其周圍有許多重要結構,發現時體積已很大,手術不能全部切除,預后不良。而有些部分的所謂顱內惡性腫瘤,由於生長在不很重要的腦組織中,幾乎能全部切除,手術后也能生存較長時間,甚至能治癒。有極個別的腦瘤,開始為良性,以後轉變成惡性。顱內膠質細胞瘤、轉移瘤及侵入瘤多為惡性。惡性膠質瘤亦稱腦癌,是生長於顱內的惡性腫瘤。
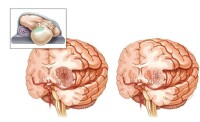
腦膠質瘤
1級為良性,2級為低度惡性,3級4級為高度惡性。
(毛細胞性 星形細胞瘤):手術是可以治癒性的。如果在術后影像上有殘餘腫瘤,則可行第二次手術切除整個腫瘤。放療和化療對此類腫瘤極其有限。
(低度惡性膠質瘤):手術是非功能區腫瘤的最主要的治療手段。對於40歲以下的肉眼全切的病人,無需額外的其他治療。對於40以下的不全切除的腫瘤病人以及病人年齡大約40歲不管是否全切都應該進行放療。
(間變星形細胞瘤):需要手術來達到組織病理診斷和減小腫瘤體積。病人應當進行放療和化療。
(多形性膠質母細胞瘤):同樣需要手術來達到組織病理診斷和減小腫瘤體積。術後放療(劑量在60Gy左右)。化療手段包括卡莫司汀,聯合方案PCV(甲基苄肼,環己亞硝脲和長春新鹼),或者替莫唑胺用來對腫瘤生長進行控制。
腦膠質瘤
為高度惡性腫瘤,好發於2-10歲的兒童,最少者可見於幾月余小兒,大多數來源於小腦蚓部向四腦室及延髓小腦半球生長,以額、頂、顳葉區為多見。病人主要表現為神經功能障礙。常無法徹底手術切除,且複發迅速。因阻塞腦脊液循環通道,發現時多已伴有腦積水,CT及MR可發現后顱窩佔位,因CT對此部位顯示不清,故推薦MR檢查。
為低度惡性腫瘤,偏良性,不少人亦稱其為良性腫瘤。生長慢,瘤內常可見鈣化斑塊
亦為膠質瘤的一種,原則與星形細胞瘤基本相同。
腦膠質瘤大多緩慢發病,自出現癥狀至就診時間一般為數周至數月,少數可達數年。惡性程度高的和后顱窩腫瘤病史較短,較良性的或位於靜區的腫瘤病史較長。腫瘤若有出血或囊變,癥狀會突然加重,甚至有類似腦血管病的發病過程。膠質瘤的臨床癥狀可分兩方面,一是顱內壓增高癥狀,如頭痛、嘔吐、視力減退、復視、精神癥狀等;另一是腫瘤壓迫、浸潤、破壞腦組織所產生的局灶癥狀,早期可表現為刺激癥狀如局限性癲癇,後期表現為神經功能缺失癥狀如癱瘓。
胚胎性腫瘤中樞神經系統 (CNS)包括惡性生殖細胞瘤、成神經管細胞瘤、原始神經外胚層腫瘤 (PNET)等 ,好發於兒童青少年
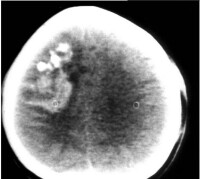
腦膠質瘤
腦幹腫瘤(腦幹膠質瘤)的癥狀可分為一般癥狀和局灶性癥狀兩類。一般癥狀以後枕部頭痛為常見。兒童常有性格改變,不少病人伴有排尿困難。顱內壓增高常不是腦幹腫瘤的首發癥狀。因此,對於進行性交叉性麻痹或多發性顱神經麻痹合併錐體束損害,無論有無顱內壓增高均應首先考慮腦幹腫瘤的可能。腦幹腫瘤的局灶性癥狀隨腫瘤的部位而異,由於腫瘤的浸潤性生長,明確劃分具體部位如中腦或橋腦實際上是困難的。
腦幹腫瘤(腦幹膠質瘤)癥狀:
由於腫瘤極易阻塞導水管,故早期可出現顱內壓增高癥狀。也有首發癥狀為精神和智力改變,這可能與網狀結構受累有關。根據腫瘤侵襲部位不同,常表現有:①動眼神經交叉性偏癱綜合症——Weber綜合症,病變位於大腦腳底部,出現病側動眼神經麻痹,對側上、下肢體和面、舌肌中樞性癱瘓。②四疊體綜合症——Parrnaud綜合症,表現眼瞼下垂、上視麻痹、瞳孔固定、對光反應消失、會聚不能等。③benedikt綜合症,表現為耳聾等、病側動眼神經麻痹、對側肢體肌張力增強、震顫等。
佔全部腦幹腫瘤半數以上,多見於兒童。早期兒童常以復視、易跌跤為首發癥狀;成年人則常以眩暈、共濟失調為首發癥狀。90%以上病人有顱神經麻痹癥狀,約40%病人以外展神經麻痹為首發癥狀,隨著腫瘤發展出現面神經、三叉神經等顱神經損害和肢體的運動感覺障礙。常表現有Millard-Gubler綜合症——橋腦半側損害,包括面神經交叉癱,若病變位於橋腦下半部偏一側時致病側周圍性面癱伴對側肢體偏癱。
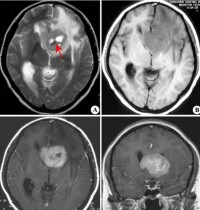
腦膠質瘤
臨床上常表現的延髓半側損害有:①舌下神經交叉癱(Jackson綜合症);②吞咽、迷走交叉癱(Avellis綜合症);③Schmidt綜合症——病側Ⅸ~Ⅶ顱神經麻痹及對側半身偏癱;④延髓背外側綜合症(Wallenberg綜合症)等。
膠質瘤的診斷,根據其生物學特徵、年齡、性別、好發部位及臨床過程進行分析,在病史及體征基礎上,採用電生理、超聲波、放射性核素、放射學及核磁共振等輔助檢查,定位正確率幾乎是100%,定性診斷正確率可在90%以上。
腦膠質瘤由於腫瘤呈浸潤性生長,與腦組織無明確分界,難以徹底切除,手術治療的原則是在保存神經功能的前提下儘可能切除腫瘤。早期腫瘤較小又位於適當部位者可爭取全部切除。位於額葉的腫瘤,可作腦葉切除。當額葉或顳葉腫瘤範圍較廣不能全部切除時,可同時切除額極或顳極作內減壓術。腫瘤位於運動、言語區而無明顯偏癱、失語者,宜注意保存神經功能,適當切除腫瘤,避免發生嚴重後遺症。腦室腫瘤宜從非功能區切開腦組織進入腦室,儘可能切除腫瘤,解除腦梗阻。位於丘腦、腦幹的膠質瘤,除小的結節性或囊性者可作切除外,一般作分流術,緩解增高的顱內壓后,進行中醫藥綜合治療。
膠質細胞瘤的生長特點為浸潤性生長,與正常腦組織無明顯界限,多數不限於一個腦葉,向腦組織外呈指狀深入破壞腦組織,偏良性者生長緩慢,病程較長,惡性者瘤體生長快,病程短。
目前國內外對於膠質瘤的治療普遍為手術、中醫藥、放療、化療、X刀、和γ刀。
手術治療基於膠質瘤的生長特點,理論上手術不可能完全切除,生長在腦幹等重要部位的腫瘤有的則根本不能手術,所以手術的治療目的只能局限於以下5個方面①明確病理診斷,②減少腫瘤體積降低腫瘤細胞數量,③改善癥狀緩解高顱壓癥狀;④延長生命並為隨後的其他綜合治療創造時機;⑤獲得腫瘤細胞動力學資料,為尋找有效治療提供依據。依據生長位置及生長特點,約50%無法全切,為了避免手術后功能損害,即使為全切術,在原發部位仍會有腫瘤殘存,所以很難根治,複發率很高。根據我院長時間的,隨訪和調查膠質瘤3、4級複發最快的一個月左右,慢的多半年。
1、2級一般的複發1-2年。
放射治療幾乎是各型膠質瘤的常規治療,但療效評價不一,除髓母細胞瘤對放療高度敏感,室管膜瘤中度敏感外,其他類型對放療均不敏感,有觀察認為放療與非放療者預后相同。此外射線引起的放射性壞死對於腦功能的影響亦不可低估。X-刀、γ-刀—均屬放射治療範疇,因腫瘤的部位、瘤體大小(一般限於3厘米以下)及瘤體對射線的敏感程度,治療範疇局限,目前認為膠質瘤,特別是性質惡性的星形Ⅲ-Ⅳ級或膠質母細胞瘤均不適合採用R-刀治療。
原則上用於惡性腫瘤,但化療藥物限於血腦屏障及藥物的毒副作用,療效尚不肯定,常用治療的腦膠質瘤幾種西藥有效率均在30%以下。
中醫中藥也是腦膠質瘤治療的最重要的治療手段。
顱內惡性腫瘤大都生長在腦神經組織內,細胞分化不良,生長迅速,難以根治。有極個別的腦瘤,開始為良性,以後轉變成惡性。顱內膠質細胞瘤、轉移瘤及侵入瘤多為惡性。目前的研究認為:惡性腦瘤的發生髮展是一個由多種病因引起、多階段的發生髮展過程。就惡性腦瘤的治療方法來說,有中醫及西醫兩大方法,而其對惡性腦瘤的治療又各有優缺點,現將中西醫治療惡性腦瘤優缺點比較如下:
西醫:惡性膠質瘤的病因至今不甚明確,西醫在預防惡性腦瘤的發生方面缺乏有效的措施和辦法,只是在控制某些與惡性腦瘤發生的環境因素和相關疾病方面做了一些探索;在治療方面,西醫在防治惡性膠質瘤局部病變或由於腫塊壓迫造成的功能障礙等方面有較好效果,但對於惡性膠質瘤腫瘤引起的病理生理變化常缺乏有效的治療措施。
中醫:中醫按照其獨特的理論體系,應用中藥防治惡性膠質瘤的發生和發展已經取得了一些效果。在治療方面,中醫在消除腫塊方面作用較差,但中藥人蔘皂苷rh2在防治惡性膠質瘤腫瘤引起的病理生理變化具有較好作用,是目前西醫達不到的作用。
腦瘤專家說由於中、西醫其理論體系和臨床實踐的差異,對惡性腦膠質瘤的治療各有其特點和長處,正確地選用這兩種手段可以起到相互增效、提高腫瘤治療效果的目的和作用。
惡性膠質瘤並不是一個均一的群體,同種病理類型不同病人對同一化療方案的療效不一樣,膠質瘤中某些遺傳特徵的改變與其對化療的敏感性密切相關。如何識別出化療有效人群,對提高化療療效,避免盲目/無效化療具有重要意義。目前,比較肯定與臨床療效相關的分子有:O6-甲基鳥嘌呤-DNA甲基轉移酶(O6-methylguanine-DNA methyltransferase , MGMT)和染色體1p/19q雜合性缺失(loss of heterozygosity, LOH)。在化療前先檢測腫瘤組織中MGMT和染色體1p/19q的表達,據檢測結果選擇化療方案有望提高化療的有效性。
(1) MGMT強陽性(++)和陽性(+)表達患者化療方案
這類患者由於存在由MGMT介導的耐葯因素,不宜用亞硝脲類藥物單葯或TMZ五天方案化療。可選用不含亞硝脲和TMZ的化療方案,如VM26+DDP;亞硝脲類藥物或TMZ聯合其他藥物化療,DDP在亞硝脲類藥物或TMZ給葯前24小時給予可降低MGMT轉錄;由於TMZ有自身耗竭MGMT的作用,可選用TMZ較長時間持續用藥方案。
(2) MGMT可疑陽性(±)和陰性(-)表達患者化療方案:
這類患者選擇化療藥物的範圍相對比較廣,可結合年齡、卡氏評分、病理級別、腫瘤組織中其他分子指標如PCNA、PTEN、TOPOII、GST等的表達,選用亞硝脲類或替莫唑胺單葯或與其他藥物聯合用藥方案,也可選用不含亞硝脲類或替莫唑胺方案。
染色體1p/19q雜合性缺失的少突膠質瘤患者對化療敏感,預后好,生存期長,手術后先行PCV方案或TMZ組成的方案化療,放療可推遲,作為複發時的挽救治療。單1p LOH的少突膠質瘤患者也對化療敏感,但化療療效持續時間及生存期相對短,需放化療結合治療,手術后可先行化療,化療結束后儘快行放療。1p/19q均無LOH,尤其伴有PTEN突變、10q LOH、EGFR擴增、CDKN2A 缺失和環狀強化的患者預后非常差,建議6周同期放化療,然後序貫周期化療。
用於膠質瘤化療臨床研究的分子靶向藥物較多。常用的有靶向血小板衍生的生長因子受體(platelet-derived growth factor receptor , PDGFR)的小分子酪氨酸激酶抑製劑伊馬替尼(imatinib)、靶向表皮生長因子受體(epidermal growth factor receptor, EGFR)的小分子酪氨酸激酶抑製劑吉非替尼(gefitinib)、靶向血管內皮生長因子(vascular endothelial growth factor, VEGF)的重組人單克隆IgG1抗體貝伐單抗(Bevacizumab)等。
由於信號傳導通路的複雜性以及不同通路之間的交互作用,單一靶向藥物治療惡性膠質瘤作用有限。針對多個靶點的藥物,或有互補作用的不同靶向藥物的聯合,靶向藥物和細胞毒類藥物如替莫唑胺,以及放療的聯合治療將是提高療效的關鍵。
就目前治療現狀而言,惡性腦瘤仍是醫學上未被攻克的一大難題,但是這也並不等於得了惡性膠質瘤就被宣判了死刑,臨床上亦有不少治療后長期生存的病例。早期惡性膠質瘤能治好嗎?主要取決於是否及時採取了恰當的治療手段。早期惡性腦瘤癌腫較小,若部位合適,應行手術切除。若癌腫部位切除難度大,可先行放療,待癌腫變小后,再行手術切除。另外,西醫各治療手段均會對人體正常細胞造成不同程度的損傷,臨床上多主張聯合中醫藥治療,以起到增效減毒的作用。