乳狀液
乳狀液
徠乳狀液是一種液體以液珠形式分散在與它不相混溶的另一種液體中而形成的分散體系。乳狀液一般不透明,呈乳白色。液滴直徑大多在100納米~10微米之間。
對可見光的反射比較顯著,可用一般光學顯微鏡觀察。乳狀液可分水包油(O/W)和油包水(W/O)兩種類型。
兩種互不相溶的液體經振蕩后形成的分散體系的表面吉布斯函數很高,是熱力學不穩定體系,因此,要形成穩定的乳狀液,必須設法降低混合體系的吉布斯函數。常用的方法是加入乳化劑(表面活性劑)。乳化劑分子的一端親水,另一端親油。在乳狀液中,乳化劑分子在水、油兩相的界面定向排列,如圖下圖所示。極性基團指向水,非極性基團指向油,從而降低界面張力,增強乳狀液的穩定性。另外,乳化劑分子緊密地定向排列在油一水界面上,形成一層保護膜,阻止了液滴的自動聚集,使乳狀液趨於穩定。

乳化液示意圖
乳狀液有兩種類型,其鑒別方法很簡單,常用的一種是稀釋法,用水去沖稀乳狀液,如能混溶則其連續相必定是水相,因而是O/W型,如不能,則是W/O型。另一種是染色法,乳化前在油相中加入少量染料,乳化后在顯微鏡下觀察,液珠帶色是O/W型,連續相帶色則是W/O型。也可把染料溶於水相進行觀察。
影響乳狀液類型的因素:
表面活性劑作乳化劑的影響
如果用表面活性劑作乳化劑,則表面活性劑親水、親油能力的相對大小是決定乳狀液類型的主要因素。如果表面活性劑的親水能力強,則它在水中的溶解度比在油中的大,容易形成O/W型乳狀液;反之,則易形成W/O型乳狀液。一般稱此為班克羅夫特規律。例如鈉皂、鉀皂和特溫型非離子表面活性劑溶於水,是 O/W型乳化劑。二價、三價金屬皂和斯潘型非離子表面活性劑溶於油,是W/O型乳化劑。
親水親油平衡的英文縮寫為HLB,由W.C.格里芬提出,表面活性劑的 HLB值是它的親水、親油能力相對大小的衡量。HLB值為8~18的表面活性劑的親水性強,可作O/W型乳化劑。HLB值為3~6的表面活性劑的親油性強,可作W/O型乳化劑。HLB值是表面活性劑的一個重要參數,一般通過實驗測定,對某些個別類型的表面活性劑,也可通過公式計算。
對非離子表面活性劑的親水、親油能力的大小除與分子中非極性基的大小和極性基中環氧乙烷鏈節數目有關外,還與溫度有關。溫度低於濁點(水溶液變濁時的溫度)時,表面活性劑親水性強和溶於水的是O/W型乳化劑。溫度高於霧點(即油溶液的濁點)時,表面活性劑親油性強和溶於油的是W/O型乳化劑。在濁點附近,乳狀液存在一相轉變溫度(PIT)。用非離子表面活性劑作乳化劑形成的乳狀液類型,決定於乳化溫度是低於還是高於PIT。
固體粉末做乳化劑的影響
它由油、水兩相在粉末表面互相接觸時接觸角θW和θO的大小決定。0°<θW<90°時,則粉末大部分在水相,是O/W型乳化劑。0°<θO<90°時,則粉末大部分在油相,是W/O型乳化劑。θW(或θO)=0°時,則固體粉末完全浸入水相(或油相),無乳化劑的作用。
相體積分數的影響一般指的是油、水兩相在乳狀液中所佔體積百分數。若液滴是大小相同的圓球,從立體幾何可以算出,圓球以最緊密的方式堆積時,圓球佔總體積的74.02%。奧斯特瓦爾德認為,如果乳狀液內相的體積分數m超過74.02%,則導致乳狀液的變形或破壞。乳狀液的類型與相體積分數有關,內相體積分數增加,有可能引起乳狀液類型的變化,但其變型的位置與乳化劑的親水、親油能力有關,m一定在74.02%處。因為乳狀液的顆粒大小不均勻,如果乳化時採用內相往外相中加入的方式,則可製備內相體積分數大於99%的乳狀液。
乳狀液是一種多相分散體系,分散相與連續相之間有液-液界面,因而有界面自由能(見界面現象)。乳化時,液-液界面增加,體系的界面自由能增加。因此,乳化過程是熱力學不自發過程(見熱力學過程),需要外界對體系作功。乳狀液液滴在互相碰撞時合併,則是界面縮小,體系界面自由能下降過程,屬於熱力學自發過程。因此,乳狀液是熱力學不穩定體系。如果乳狀液液滴的合併速度很慢,則可認為乳狀液具有一定的相對穩定性。液滴能否在熱運動或重力作用下互相碰撞而合併的關鍵是液-液界面膜的性質。
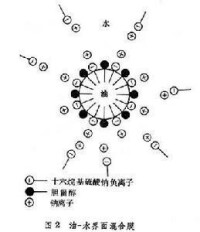
乳化劑的加入,可降低油-水界面張力,因而也降低了乳化時能量的消耗,有利於體系的乳化和乳狀液的穩定。但降低界面張力的更重要作用是表面活性劑在油-水界面上形成一種定向單分子層,根據吉布斯吸附公式,界面張力下降得越低,表面活性劑在界面上的吸附量越大,則定向單分子層在界面上排列越緊密,界面膜的強度越大,乳狀液越穩定。為了增加界面膜的強度,用混合乳化劑比用單一乳化劑效果更好。例如十六烷基硫酸鈉加入膽甾醇即可在油-水界面上形成緊密混合膜。對陰離子表面活性劑,一般高級脂肪醇、胺、酸均有此種作用。對非離子表面活性劑,特溫型與斯潘型混合使用也可形成緊密混合膜。這種油-水界面上的緊密混合膜,因雙電層重疊時的排斥作用(離子型表面活性劑)或因兩個吸附層接近時的空間阻礙作用,都可阻止液滴互相接近時發生合併,因而可提高乳狀液的穩定性。
乳狀液液滴的顆粒較大,油-水兩相的密度一般不等,因而在重力作用下,液滴上浮(分散介質密度大於分散相的)或下沉(分散介質密度小於分散相的),乳狀液分為兩層,在一層中分散相比原來的多,在另一層中則相反。此即乳狀液的分層。對已分層的乳狀液,只需輕輕攪動,液滴即可重新均勻分佈於整個體系中。
乳狀液的不穩定性有幾種可能的表現形式:分層或沉降((ireaming or se(limentation)、絮凝(fl()(-('uialion)、聚結(c:oale.scence)、破乳(demulsifiCation ol'l,reakdown)、變型或相轉變( invrrsiorl(’r phase inversion)和熟化(ostwald ripening)。這些過程代表著乳狀液不穩定性不同的表現形式或階段,某些情況下,這些過程可能是相互關聯的。乳狀液在完全破乳以前可能經歷絮凝、聚結和分層。如牛奶、奶油的上浮,或未經過均質化的牛奶會分為兩層,在一層中分散相比原來的多,在另一層中分散相則較少 變型則是乳狀液由O/W(W/O)型變成W/O( O/W)型,破乳聚沉過程可分為兩步:第一步,絮凝過程中分散相的液珠可逆地聚集成團;第二、步,聚結過程中聚集團不可逆地合成一個大滴。破乳聚沉與分層或變型可以同時發生。下面介紹兩種:
分層或沉降
由於油相和水相的密度不同,在外力(如重力、離心力)作用下液滴將上浮或下沉,在乳狀液中建立平衡的液滴濃度梯度,這個過程稱為分層或沉降。雖然分層使乳狀液的均勻性遭到破壞,但乳狀液並未真正被破壞,往往液滴密集地排列在體系的一端(上層或下層),分成兩層,其界限可以足漸變或明顯的;一般情況下,分層過程中液滴大小和分佈沒有明顯的改變,只是在乳狀液內建立起平衡的液滴濃度梯度。
絮凝
乳狀液中分散相的液滴聚集成團,形成二維的液滴簇,稱為絮凝物(flocs),這個過程稱為絮凝。一般情況下,絮凝物中液滴的大小和分佈沒有明顯的變化,不會發生液滴的聚結,液滴仍然保持其原有特性。絮凝是由於液滴之間的吸引力引起的,這種作用會使得乳狀液中的分散相聚集成團。
乳化劑
乳狀液