Perkin反應
Perkin反應
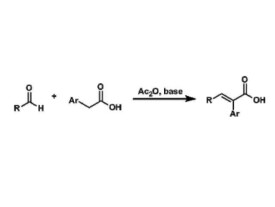
Perkin反應,又稱普爾金反應,由不含有α-H的芳香醛(如苯甲醛)在強鹼弱酸鹽的作用下與有機酸酐進行的縮合反應。
與Knoevenagel反應一致的條件下(鹼性)、酸酐與芳香族醛或酮脫水縮合,形成取代烯烴的反應。
Perkin反應,又稱普爾金反應,由不含有α-H的芳香醛(如苯甲醛)在強鹼弱酸鹽(如碳酸鉀、醋酸鉀等)的催化下,與含有α-H的酸酐(如乙酸酐、丙酸酐等)所發生的縮合反應,並生成α,β-不飽和羧酸鹽,後者經酸性水解即可得到α,β-不飽和羧酸。
與Knoevenagel反應基本一樣。酸酐的α位的H酸性相對比較高,被弱鹼奪去後進行的整個反應。
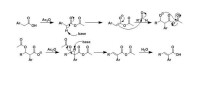
反應原理
肉桂酸,化學名β-苯基丙烯酸或3-苯基-2-丙烯酸,又稱桂皮酸,無色針狀晶體,具有爽快的淡甜脂香氣,是一種重要的精細化工合成中間體。肉桂酸理論上有順、反兩種異構體,一般說的肉桂酸均指反式異構體。肉桂酸被廣泛應用於醫藥、香料、農藥、塑料和感光樹脂等精細化工產品的製備,還可以用作長效殺菌劑、果品蔬菜防腐劑、植物生長促進劑和測定釩、鈾及分離釷的試劑等。近年來,隨著新型人工甜味劑阿斯巴甜作為甜味劑的優秀代表異軍突起,肉桂酸作為合成阿斯巴甜的重要前體物質展示出了巨大的市場潛力。
肉桂酸的生產有很多方法,但目前肉桂酸的工業生產方法仍以經典的Perkin合成法和苯乙烯-四氯化碳法為主。由於四氯化碳是甲烷氯化物的一種,具有破壞臭氧層的作用,國家規定將逐步停止生產,苯乙烯-四氯化碳法可能將停止應用。因此,Perkin法合成肉桂酸的重要性進一步加強,有必要對此經典合成法作進一步研究。
Perkin法是以苯甲醛與乙酸酐為原料在醋酸鹽的催化作用下發生類似羥醛縮合的反應,生成肉桂酸。催化劑還可以是氟化鉀、碳酸鹽等。因為此法具有原料易得、工藝流程短、副產物少等優點,目前為國內外生產肉桂酸的主要方法。但其肉桂酸的收率低、成本較高等缺點的存在也制約了此法的發展。
Perkin法是芳香醛和具有α-H原子的酸酐在鹼性催化劑的作用下,發生類似羥醛縮合的反應,生成芳基取代的α,β-不飽和芳香酸的反應。
Perkin法的反應機理:羧酸鹽的負離子作為質子的受體,與酸酐作用,產生羧酸,同時生成一個羧酸酐的α-負離子,該負離子與醛發生親核加成生成烷氧負離子,然後向分子內的羰基進攻,關環,從另一側開環,得到羧酸根負離子。羧酸根負離子發生E2消除,再經酸化,最後得到芳基不飽和羧酸,主要是反式羧酸。
其反應歷程如圖1所示。
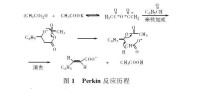
反應歷程
本實驗中苯甲醛的沸點為178~179℃,直接蒸餾去除溫度太高,因此採用水蒸氣蒸餾去除未反應的苯甲醛。
水蒸氣蒸餾的原理如下:當水和有機物一起共熱時,根據分壓定律整個體系的蒸氣壓力應為各組分蒸氣壓之和。即P=P+P,其中P代表總的蒸氣壓,P為水的蒸氣壓,P為與水不相溶物或難溶物質的蒸氣壓。
當混合物中各組分的蒸氣壓總和等於外界大氣壓時,混合物開始沸騰。這時的溫度即為它們的沸點,而這時的沸點比其中任何一組分的沸點都要低些。因此,常壓下應用水蒸氣蒸餾,就能在低於100℃的情況下將高沸點組分與水一起蒸出來。蒸餾時混合物的沸點保持不變,直到其中一組分幾乎全部蒸出。水蒸氣蒸餾法的優點在於使所需要的有機物在較低的溫度下從混合物中蒸餾出來,可以避免在常壓下蒸餾時所造成的損失,提高分離提純的效率。同時在操作和裝置方面也較減壓蒸餾簡便一些,所以水蒸氣蒸餾可以應用於分離和提純有機物。
用Perkin法合成肉桂酸,首先確定鹼性催化劑為無水碳酸鉀,進一步通過正交實驗確定影響因素主次順序依次為催化劑用量、反應時間和反應物摩爾比。結果表明,最佳工藝條件為苯甲醛與乙酸酐的摩爾比為1∶3,反應時間為90min,苯甲醛與無水碳酸鉀的摩爾比為1:1,在此條件下所合成的肉桂酸樣品,產品產率可達61.2%,純度可達97%以上。