硫化鎂
硫化鎂
硫化鎂是一種無機物,化學式為MgS,白色或紅棕色立方系晶體或粉末,溶於酸及三氯化磷,在冷水中分解生成Mg(OH)2和Mg(SH)2,在熱水中分解生成氫氧化鎂與H2S,在冷、濃HNO3中析出S。
硫化鎂可通過硫酸鎂與二硫化碳在高溫下反應,或將硫化氫通入紅熱的氧化鎂上製得。
外觀:室溫下為無色晶體,不純時為棕色粉末。
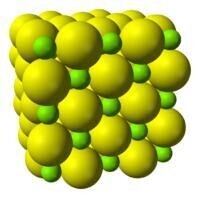
結構
密度:2.84 g/cm³
熔點:>2000 °C
溶解度:分解
硫化鎂可由硫或硫化氫與鎂作用製得。高爐煉鐵中脫硫也運用了此反應。
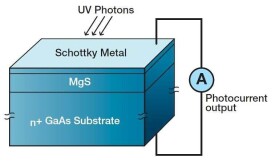
硫化鎂可用於鋼鐵脫硫:製取熒光粉,用作寬能帶間隙的半導體。
1、環境危害:對環境有危害,對水體可造成污染。燃爆危險:本品不燃,具刺激性。第四部分:急救措施 皮膚接觸:脫去污染的衣著,用流動清水沖洗。
2、眼睛接觸:提起眼瞼,用流動清水或生理鹽水沖洗。馬上就醫。
3、吸入:迅速脫離現場至空氣新鮮處。保持呼吸道通暢。如呼吸困難,給輸氧。如呼吸停止,立即進行人工呼吸。馬上就醫。
4、食入:飲足量溫水,催吐。就醫。