水溶液電解
水溶液電解
以金屬鹽水溶液為電解質進行提取或處理金屬的電化冶金方法,簡稱電解,是一種將電能轉變成化學能的過程。
利用在作為電子導體的電極與作為離子導體的電解質的界面上發生的電化學反應進行化學品的合成高純物質的製造以及材料表面的處理的過程。通電時,電解質中的陽離子移向陰極,吸收電子,發生還原作用,生成新物質;電解質中的陰離子移向陽極,放出電子,發生氧化作用,亦生成新物質。
如圖所示,由A和C兩電極浸入含有Me離子和X離子組成溶液的電解池中,在兩極的上端分別與直流電源的正負兩極接通時,直流電源便起著一個電子泵的作用;將電子壓入C,又從A將電子抽回電源。由於溶液中並不存在自由電子,因此當通過電流時,在電極-溶液界面上就會發生某種或某些組分的氧化還原,使得在C處消耗電子,而在A處放出電子。這個過程就是氧化-還原反應。電極C 就是通常所說的陰極(和電源負極相接),在它附近的離子或分子由於接受電子而被還原;而在陽極A處(與電源正極相接),由於離子或分子產生電子而氧化。總的電解池反應是兩個電極半反應的總和。當電解進行時,離子不斷向兩極遷移,正離子向陰極遷移,負離子像正極遷移。
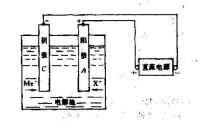
電解工作原理
近年來在電解工藝中開展的研究主要有:①提高電流密度、強化生產,主要途徑是改進電解槽結構和電解液的循環方式、周期反向電解和周期斷電電解等;②硫化物、合金直接電解和流態化電解及懸浮電解;③串聯電解等。
在有色金屬濕法冶金領域中,水溶液電解廣泛應用於兩個方面:
(1)從粗金屬、合金或其他中間物中精鍊和提取金屬,即通常所說的電解精鍊或可溶陽極電解;
(2)從浸出凈化液中提取金屬,即通常所稱的電解沉積(簡稱電積)或電解提取,也稱不溶陽極電解。
