三氧化鉬
白色或蒼黃色、透明斜方晶體
三氧化鉬是一種無機物,分子式為MoO3,分子量為144。
2017年10月27日,世界衛生組織國際癌症研究機構公布的致癌物清單初步整理參考,三氧化鉬在2B類致癌物清單中。
外觀與性狀:白色晶狀粉末。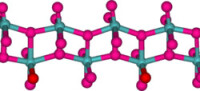 熔點(℃):795
熔點(℃):795

三氧化鉬
相對密度(水=1):4.69
沸點(℃):1150(升華)
分子式:MoO3
分子量:143.94
溶解性:微溶於水,溶於濃 硝酸、濃鹽酸,易溶於濃鹼。
加熱時變黃色,冷時即復原。即使在低於熔點情況下,也有顯著的升華現象。不溶於水,能溶於氨水和強鹼。與鹼溶液和許多金屬氧化物反應生成鉬酸鹽和多鉬酸鹽。由輝鉬礦(MoS2)灼燒或將鹽酸加入鉬酸銨中析出鉬酸后再加熱熔燒而製得,亦可直接煅燒鉬酸銨得到。用於制金屬鉬和鉬的化合物。未有特殊的燃燒爆炸特性。
未有特殊的燃燒爆炸特性。
2、用作製取金屬鉬及鉬化合物的原料。石油工業中用作催化劑。還可用於搪瓷釉藥顏料及藥物等。
3、本品為添加型阻燃劑,具有阻燃和抑煙雙重功能,與其他阻燃劑復配可降低成本,提高阻燃性,減小發煙量。三氧化鉬也有阻燃和抑煙的雙重作用,它與三水合氫氧化鋁和氧化銻都顯示了一定的協同效果。
4、光譜分析試劑。血糖、蛋白質、生物鹼、砷、酚的檢測。五氧化二磷、三氧化二砷、雙氧水的還原劑。
5、三氧化鉬在配製鉬酸鹽中用於電鍍或用作金屬氧化添加。
外觀 淺藍色至灰色粉末堆積密度0.38g/cm3
三氧化鉬的質量分數≥99.0% 10%漿料的pH值 2.9
鉬質量分數 ≥66.0% 氨水不溶物 ≤0.04%
用作高效阻燃抑煙劑,對於含氯膠黏劑更為有效。參考用量0.5~~5.0份即能使生煙量降低30%~80%,氧指數提高10%~20%。鉬化物與氧化銅、氧化鐵:氧化鎘、氧化鋅等混合使用用具有協同效應,其抑煙效果比單一MoO3更佳。國內阻燃抑煙劑多為氧化鉬、鉬酸銨的混合物。
健康危害:對眼睛、皮膚、粘膜和上呼吸道有刺激作用。
燃爆危險:該品不燃,具刺激性。
皮膚接觸:脫去污染的衣著,用大量流動清水沖洗。
眼睛接觸:提起眼瞼,用流動清水或生理鹽水沖洗。就醫。
吸入:脫離現場至空氣新鮮處。如呼吸困難,給輸氧。就醫。
食入:飲足量溫水,催吐。就醫。
有害燃燒產物:自然分解產物未知。
滅火方法:消防人員必須穿全身防火防毒服,在上風向滅火。滅火時儘可能將容器從火場移至空曠處。
應急處理:隔離泄漏污染區,限制出入。建議應急處理人員戴防塵面具(全面罩),穿防毒服。避免揚塵,小心掃起,置於袋中轉移至安全場所。若大量泄漏,用塑料布、帆布復蓋。收集回收或運至廢物處理場所處置。
操作注意事項:密閉操作,局部排風。操作人員必須經過專門培訓,嚴格遵守操作規程。建議操作人員佩戴自吸過濾式防塵口罩,戴化學安全防護眼鏡,穿防毒物滲透工作服,戴橡膠手套。避免產生粉塵。避免與酸類接觸。搬運時輕裝輕卸,防止包裝破損。配備泄漏應急處理設備。倒空的容器可能殘留有害物。
儲存注意事項:儲存於陰涼、通風的庫房。遠離火種、熱源。應與酸類、食用化學品分開存放,切忌混儲。儲區應備有合適的材料收容泄漏物。
鉬酸銨熱分解法將輝鉬精礦粉碎至60~80目,放人焙燒爐中於500~550℃氧化焙燒,用 氨水浸出,得鉬酸銨溶液除去雜質后,加熱至40~45℃,在攪拌下加入硝酸中和至pH=1.5,生成八鉬酸銨沉澱,經過濾,離心脫水后,溶於70~80℃的氨水中,再蒸發濃縮,得到 仲鉬酸銨,然後在550~600℃下進行熱分解,得三氧化鉬成品。
工業上用 二硫化鉬氧化製備三氧化鉬:
2 MoS2+ 7 O2→ 2 MoO3+ 4 SO2實驗室中,則可先由鉬酸鈉溶液酸化製得三氧化鉬水合物,再將其乾燥製得:
Na2MoO4+ H2O + 2HClO4→ MoO3(H2O)2+ 2 NaClO4
採用溶膠凝膠法成功製備了三氧化鉬 (MoO3)薄膜。首先,以CH3COCH2 COCH3,MoO3,C6 H5CH3和HOCH2 CH2 OCH3為原料合成三氧化鉬溶膠和凝膠 .凝膠的熱重和差熱分析 (TG DTA)顯示三氧化鉬的晶化出現在5 0 8℃附近的 14 0℃範圍內 .其次 ,利用旋轉塗布法在硅 (111)基片上通過 4 5 0℃退火處理製備了三氧化鉬薄膜 .XRD和FTIR譜表明薄膜為α MoO3相 .SEM形貌像顯示薄膜中晶粒分佈均勻緻密 ,在基片表面無擇優取向 ;晶粒尺度範圍在 0 .5~ 1μm之間。
三氧化鉬可溶於 鹼,生成 鉬酸鹽。
MoO3+ 2NH3.H2O → (NH4)2MoO4+ H2O
三氧化鉬高溫與氫氣反應,最終產物是金屬鉬。金屬鉬即通過此法製取
MoO3+ 3 H2→ Mo + 3 H2O
鉬藍可由鋅在溶液中還原鉬酸鹽得到。
氣態時,三氧化鉬由MoO3分子組成,Mo-O之間為雙鍵。固態時,無水三氧化鉬為正交晶系,含有變形八面體MoO6構成的層狀結構。八面體成鏈,之間有氧原子交聯,八面體中一條Mo-O(非交聯氧)鍵長較短。
危險運輸編碼:暫無
危險品標誌:有害
安全標識:S22S23
危險標識:R36/37R48/20/22
1、疏水參數計算參考值(XlogP):無
2、氫鍵供體數量:0
3、氫鍵受體數量:3
4、可旋轉化學鍵數量:0
5、互變異構體數量:無
6、拓撲分子極性表面積:51.2
7、重原子數量:4
8、表面電荷:0
9、複雜度:61.8
10、同位素原子數量:0
11、確定原子立構中心數量:0
12、不確定原子立構中心數量:0
13、確定化學鍵立構中心數量:0
14、不確定化學鍵立構中心數量:0
15、共價鍵單元數量:1
