臭氧化反應
臭氧化反應
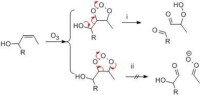
臭氧化反應,有機合成中重要的反應之一。是實現烯烴官能團向醛酮官能團轉化的手段之一。
當烯烴與臭氧反應時,可得到不穩定的臭氧化物,它具有爆炸性,通常加還原劑(如鋅粉)催化分解為兩個羰基化合物,它們正好分別與原烯烴C=C雙鍵兩側的骨架相同。分析測知兩羰基化合物的結構后,就可推知該烯烴的分子結構。由於現代光譜儀器分析測定分子結構方面的迅速進展,用臭氧化來測定烯烴結構的重要性已有所下降。
烯烴的臭氧化反應最早於1840年由Christian Friedrich Schönbein發現。在有機化學發展的早期被廣泛用來作為推測有機物未知結構的重要降解手段。
臭氧與無機化合物或有機化合物反應生成不穩定的臭氧化物的過程。
如乾燥的氫氧化鉀與臭氧作用生成臭氧化鉀、水合氫氧化鉀並放出氧。
乙烯臭氧化生成環臭氧乙烷等。
使水、廢水或空氣與臭氧接觸,利用其強氧化作用,達到除臭、脫色、殺菌、去除有機物的目的。
有機化合物分子與臭氧發生的氧化反應。也稱臭氧化反應,可以測定烯烴的分子結構,也可以合成醛、酮、過氧酸等多種有機化合物。
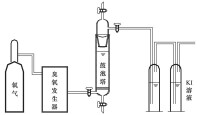
臭氧化反應
因此,在操作過程中要格外小心,在這裡要注意幾點:
②要時刻觀察反應的溫度,充分做好冷卻措施,避免發生彪溫。
③反應結束后,要用足夠多的氮氣排空反應體系內殘留的臭氧,再淬滅。
這一步是臭氧反應中最容易發生危險的步驟,要格外小心,通常要做好防護措施,兩個以上人員來操作。
不過,現在由於科學技術的發展,很多公司開始採用一些專門用來進行臭氧化反應的儀器。現在應用最為廣泛的是由匈牙利ThalesNano公司生產的O-Cube臭氧儀。它將流動化學和臭氧發生裝置結合在一起,從而實現了臭氧在實驗室的安全利用和便利使用。O-Cube由於微量反應體積、物料連續流動與臭氧反應,實現了安全的臭氧化反應,並且反應選擇性和收率比超低溫釜式反應大大提高。