硫化鎳
製作鎳催化劑的原料
硫化鎳晶體呈黃銅黃色,粉末呈黑色。密度:5.3-5.6g/mL,25/4℃。熔點797℃。
中文名稱:硫化鎳
漢語拼音:liúhuàniè
英文名稱:Nickel(II) sulfide
化學式:NiS
式量:90.77
CAS號:16812-54-7
MDL號:MFCD00016266
EINECS號:240-841-2
1、疏水參數計算參考值(XlogP):
2、氫鍵供體數量:0
3、氫鍵受體數量:0
4、可旋轉化學鍵數量:0
5、互變異構體數量:
7、重原子數量:2
8、表面電荷:0
9、複雜度:2
10、同位素原子數量:0
11、確定原子立構中心數量:0
12、不確定原子立構中心數量:0
13、確定化學鍵立構中心數量:0
14、不確定化學鍵立構中心數量:0
15、共價鍵單元數量:1
對水體是危害的,即使小量產品不能接觸地下水、水道或污水系統,未經政府許可勿將材料排入周圍環境。
常溫常壓下穩定
避免的物料:氧化物、酸。
相對密度5.3~5.65(α);5.0~5.6(β);5.34(γ,30℃)。熔點797℃(α);810℃(β);γ-NiS在396℃時轉變為βNiS。α-NiS溶於鹽酸,在空氣中轉變成Ni(OH)S。β-NiS在2mol/L HCl中煮沸,迅速溶解。它們均溶於硝酸和王水。
常溫密閉避光,通風乾燥。
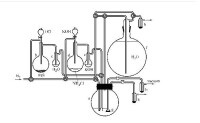
合成方法
e—濃氫氧化鉀溶液;f—洗滌用水;g—玻璃砂芯濾器;h—汞。
用不含O2和CO2的N2氣驅盡儀器中的空氣,同時煮沸各儀器中的液體,然後在N2氣流中冷卻。在b中產生不含CO2的H2S氣體,使a瓶內產生硫化物沉澱。(控制反應,勿使硫化物完全沉澱,否則,後面洗滌時沉澱不易沉降。)將f中的洗滌水用N2壓入a瓶,充分搖動沉澱,待沉澱沉降后,通過抽真空,經g吸出洗滌液。如此反覆洗滌15~20次。
β-NiS:Ni+S=NiS
將化學計量的Ni和S混合物在密封的真空石英管內加熱至900℃,反應6h即得。
γ-NiS:NiSO+HS=NiS+HSO
所用的儀器裝置和製備α-NiS的相同。所不同的是在a瓶中放置用稀硫酸略微酸化的0.5mol/L NiSO4。反應前必須嚴格排出空氣。沉澱的處理方法同α-NiS。
玻璃在製作過程中有時會在其內部殘留一種叫硫化鎳的特殊雜質。之所以說它特殊,是因為它不會像一般物質一樣熱脹冷縮,恰恰相反,它會熱縮冷脹。
由於鋼化玻璃是由普通玻璃高溫驟冷處理之後製成的,在這一過程中,硫化鎳的體積先是受熱縮小,后又冷卻膨脹,這使鋼化玻璃內部出現很大的應力,這就會使鋼化玻璃出現自爆現象。
這樣的鋼化玻璃通常會在製成后不久自爆,但極個別情況時,當硫化鎳恰好位於鋼化玻璃中間時,自爆就會延遲,最長可以延遲到幾年之後。
玻璃中有NiS雜質,也就是硫化鎳,這個玩意無法從玻璃里完全剔除,總有一定量的NiS存在於玻璃里,這種雜質想性質同水比較相似屬於冷脹熱縮的東西,鋼化玻璃在鋼化的過程中他會縮小,冷卻過程中又會變大(伴隨位移的),但是因為冷卻時間很短,不足以讓它還原成常溫的大小,所以在冷卻完成後還會繼續變化,這種變化就可能會造成鋼化玻璃自爆,這是鋼化玻璃不可避免的。
