共找到2條詞條名為離心分離的結果 展開
- 物理學概念
- 化學工業出版社出版圖書
離心分離
物理學概念
離心分離(centrifugal separation):藉助於離心力,使比重不同的物質進行分離的方法。離心分離生物分子是最常用的生化分離方法,因為不同的生物分子有不同的體積和密度,可在不同離心力的作用下沉降分離。隨著生命科學技術的發展,離心分離技術已成為生物化學與分子生物學中不可缺少的分離技術手段。
對於兩相密度相差較小,黏度較大,顆粒粒度較細的非均相體系,在重力場中分離需要很長時間,甚至不能完全分離。若改用離心分離,由於轉鼓高速旋轉產生的離心力遠遠大於重力,可大大提高沉降速率,因此離心分離只需較短的時間即能獲得大於重力沉降的效果。
離心管
若這個在做非直線運動的物體(例如:車)上有乘客的話,乘客由於同樣隨著車子做轉彎運動,會受到車子向乘客提供的向心力,但是若以乘客為參照系,由於該參照係為非慣性系,他會受到與他相對靜止的車子給他的一個指向圓心的向心力作用,但同時他也會給車子一個反向等大,由圓心指向外的力,就好像沒有車子他就要被甩出去一樣,這個力就是所謂的離心力。由於處於非慣性系中,此狀況下物體所感受的力並非真實,所以有些說法會稱這種現象為“離心力”
離心是研究如細胞核、線粒體、高爾基體、溶酶體和微體,以及各種大分子基本手段。一般認為,轉速為10~25Kr/min的離心機稱為高速離心機;轉速超過25Kr/min,離心力大於89Kg者稱為超速離心機。目前超速離心機的最高轉速可達100Kr/min,離心力超過500Kg。
藉助於離心力,使比重不同的物質進行分離的方法。由於離心機等設備可產生相當高的角速度,使離心力遠大於重力,於是溶液中的懸浮物便易於沉澱析出;又由於比重不同的物質所受到的離心力不同,從而沉降速度不同,能使比重不同的物質達到分離。

大型離心機
離心分離密度大於1.3g/cm3的樣品,如DNA、RNA,需要使用密度比蔗糖和甘油大的介質。重金屬鹽氯化銫(CsCl)是目前使用的最好的離心介質,它在離心場中可自行調節形成濃度梯度,並能保持穩定。蔗糖、甘油和氯化銫都是密度離心分離中的介質,它們在性質上、使用上和原理上有什麼不同?
在速度離心時,被分離的分子越小,需要的離心速度越高。但是,離心機中影響速度高低的是轉子的半徑。離心力(g)是表示某種顆粒沉澱的最好方式,一般根據離心力和離心機轉子的半徑決定離心速度。常見細胞器離心沉澱所需的離心力列於表。
結 構 離心力
細胞核800-1000g
線粒體 20,000-30,000g
葉綠體 20,000-30,000g
溶酶體 20,000-30,000g
微體 20,000-30,000g
粗面內質網 50,000-80,000g
質膜和光面內質網 80,000-100,000g
遊離核糖體、病毒粒子 150,000-300,000g
它利用不同的粒子在離心力場中沉降的差別,在同一離心條件下,沉降速度不同,通過不斷增加相對離心力,使一個非均勻混合液內的大小、形狀不同的粒子分部沉澱。操作過程中一般是在離心後用傾倒的辦法把上清液與沉澱分開,然後將上清液加高轉速離心,分離出第二部分沉澱,如此往複加高轉速,逐級分離出所需要的物質。
差速離心的解析度不高,沉澱係數在同一個數量級內的各種粒子不容易分開,常用於其他分離手段之前的粗製品提取。
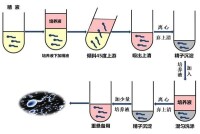
CsCl 密度梯度離心分離
由於ρP>ρm可知S>0,因此該離心法的離心時間要嚴格控制,既有足夠的時間使各種粒子在介質梯度中形成區帶,又要控制在任一粒子達到沉澱前。如果離心時間過長,所有的樣品可全部到達離心管底部;離心時間不足,樣品還沒有分離。由於此法是一種不完全的沉降,沉降受物質本身大小的影響較大,一般是應用在物質大小相異而密度相同的情況。常用的梯度液有Ficoll、Percoll及蔗糖。
等密度離心法是在離心前預先配製介質的密度梯度,此種密度梯度液包含了被分離樣品中所有粒子的密度,待分離的樣品鋪在梯度液頂上或和梯度液先混合,離心開始后,當梯度液由於離心力的作用逐漸形成底濃而管頂稀的密度梯度,與此同時原來分佈均勻的粒子也發生重新分佈。當管底介質的密度大於粒子的密度,即ρm>ρP時粒子上浮;在彎頂處ρP>ρm時,則粒子沉降,最後粒子進入到一個它本身的密度位置即ρP=ρm,此時dx/dt為零粒子不再移動,粒子形成純組份的區帶,與樣品粒子的密度有關,而與粒子的大小和其他參數無關,因此只要轉速、溫度不變,則延長離心時間也不能改變這些粒子的成帶位置。
此法一般應用於物質的大小相近,而密度差異較大時。常用的梯度液是CsCl。
固-固分離
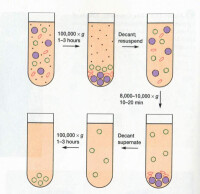
差速離心的原理
液-液分離 不互溶的液體在離心機中因密度不同而很快分離。這種方法比重力分離時間要短得多。常用一種稱為離心萃取機的裝置來分離液體溶液組分。該裝置由放置在圓筒轉鼓中的一系列多孔同心環組成,轉鼓環繞著一個筒形軸以每分鐘2000~5000轉的速度旋轉,液體通過筒形軸進出,以徑向順流方式在轉筒中流動而達到液體溶液組分的分離。
氣-氣分離 同位素研究中常用的手段。在高速旋轉下,氣體狀態的同位素混合物得以相互分離。用離心分離濃縮U是有前景的方法之一。
固-液分離 常量分析中常用過濾法,半微量分析中則用離心分離法。常用的旋轉裝置有手搖離心機和電動離心機(通常轉速為1~4千周/分),分離速度遠比過濾為快。
膠體化學
1924年瑞典的T.斯韋德貝里設計了超速離心機,這是一種以極高的角速度運轉的離心機,1940年獲得的離心加速度30萬倍於重力加速度,它和30年代多層吸附理論的建立,以及40年代疏液膠體穩定理論的建立,可說是近半世紀中膠體化學(見膠體和表面化學)領域內的三大成就。超速離心機的分離原理是,當一個含有聚合物或巨分子的溶液,在離心力是重力的25萬倍時,分子相互分離,純溶劑留在界面以上,這個界面以一定速度向容器低部移動。若溶質的分子量不均勻,這個界面上的濃度梯度也不均勻,則那些分子量低的會落在大分子之後。用光學儀器可觀察出這個界面,從而精確測定沉降速率,而每種成分的沉降速率又與其分子量有關,因而可以計算出各成分的分子量。超速離心機不僅能分離膠粒,更重要的是它能測定膠粒的沉降速率、平均分子量及混合體系的重量分佈,因而在膠體化學研究(尤其是親液膠體)中起了重大的作用。
超速離心機的出現為對高分子溶液的深入了解提供了一種有力的研究手段。1940年斯韋德貝里使用超速離心法測定了分子量及其分佈,可直接測定幾萬至幾百萬的分子量。高分子化合物分子量測定方法的出現,極大地推動了高分子化學的發展,許多天然高分子屬於單一分散體系(所有分子都持同一分子量),對這種系統,超速離心法是最好的分子量測定法,比滲透壓、光散射和粘度等測定法更好。
生物化學
超速離心法同樣為生物化學提供了一種強有力的研究手段。斯韋德貝里應用超速離心法測量了蛋白質分子在水中的沉降速率,從而能計算蛋白質的分子量。他的一些測定結果如下:牛胰島素:46000;人血紅球:63000;人血清球:153000;章血血清:2800000;煙草花葉病毒:31400000。超速離心法還經常用於蛋白質的降解、分離、精製以及分子量分佈測定。細胞研究中常用一種分帶或區域離心機,用一個大容量旋轉室,根據密度梯度離心分離原理來分離細胞。
離心分離法常用於:
①離心過濾,藉助離心作用從漿料中排出液體,漿料被引入一快速旋轉的網籃中,固體留在多孔的網上,液體則受離心作用從濾餅中擠出;或利用旋轉器中的離心力使輕重物質分開,重物質以稠泥漿的形式通過噴嘴流走。常用設備為離心過濾機。
②離心沉降,懸浮固體在離心力作用下移向或離開旋轉中心,這樣就可聚集在一個區域內而被移出,可以使顆粒的沉澱時間從幾小時減至幾分鐘。常用設備為離心沉降器。
③離心捕集,用於從煤煙、空氣流中分離出0.1~1 000微米的小顆粒物質,是治理空氣污染的有效手段之一。常用設備為離心捕集器,也稱微粒收集器、旋風除塵器。
其他應用
工業中常用離心除渣器來凈化紙漿漿料,使漿料高速迴轉或產生迴轉旋渦作用,把塵粒分離出來。還常用離心乾燥機,或稱離心脫水機,依靠離心力將水分脫去。
離心分離法與其他方法相結合,可以產生新的更為有效的分離方法,這是離心分離法的現代發展方向。在這方面,離心分離法與色譜法結合而產生的場流分級法(或稱外力場流動分餾法)就是一個典型例子。1966年J.C.吉丁斯提出一類新的無固定相的色譜分離法,即場流分級法,或稱單相色譜。這種方法的最初構思,是以離心力壓迫分子於柱壁而代替固定相的保留作用,這樣產生的分離方法稱離心色譜,也叫沉積場流分級法。後來依據這一基本思想,以電場、磁場、熱梯度等代替離心力場,得到不同的場流分級法,從而建立了一類分離方法體系。場流分級法不但對大分子和膠體有很強的分離能力,而且它也能分離分子量小於10的物質和大於30微米的遠遠超出膠體範圍的固體顆粒,其可分離的分子量有效範圍約為10~10,這樣寬的連續分離範圍是空前未有的。近年來出現的離心製備薄層色譜法是離心分離法滲透於色譜領域而產生的又一種高效分離法。層析薄板為圓形,樣品注射於圓心四周,從垂直於圓心的方向連續地加入展開劑,薄板旋轉,各不同組分即沿徑向迅速展開。在紫外燈照射下可觀察到譜帶的移動,由於板面設置是傾斜的,可沿斜向直接接收各分開的組分。該法已用於天然產物、合成產物及異構體等的快速分離提純,分離效果優於製備薄層色譜和柱層色譜法,在一定程度上與製備型高壓液相色譜法相似,但在節省時間和溶劑等方面優於後者。
