凝血機制
凝血機制
凝血機制包括凝血和抗凝兩個方面,兩者間的動態平衡是正常機體維持體內血液流動狀態和防止血液丟失的關鍵。機體的正常止凝血,主要依賴於完整的血管壁結構和功能,有效的血小板質量和數量,正常的血漿凝血因子活性。
血液凝固簡稱凝血,是血液由流動狀態變為凝膠狀態的過程,它是止血功能的重要組成部分。凝血過程是一系列凝血因子被徠相繼酶解激活的過程,最終生成凝血酶,形成纖維蛋白凝塊。迄今為止,參與凝血的因子共有12個。其中用羅馬數字編號的有12個(從Ⅰ-XIII,其中因子Ⅵ並不存在)。
人體受物理損傷后,血小板會受到損傷部位激活因素的刺激,出現血小板的聚集,成為血小板凝塊,起到初級止血作用。
接著血小板又經過複雜的變化產生凝血酶,使鄰近血漿中的纖維蛋白原變為纖維蛋白,互相交織的纖維蛋白使血小板凝塊與血細胞纏結成血凝塊,即血栓(見凝血因子)。同時血小板的突起伸入纖維蛋白網內,血小板微絲(肌動蛋白)和肌球蛋白的收縮使血凝塊收縮,血栓變得更堅實,能更有效地起止血作用,這是二級止血作用。
伴隨徠著血栓的形成,血小板釋放血栓烷A2;緻密顆粒和α顆粒通過與表面相連管道系統釋放ADP、5-羥色胺、血小板第4因子、β血栓球蛋白、凝血酶敏感蛋白、細胞生長因子、血液凝固因子Ⅴ、Ⅶ、Ⅻ和血管通透因子等多種活性物質,這些活性物質通過激活周圍血小板,促進血管收縮,促纖維蛋白形成等多種方式加強止血而有些效果。
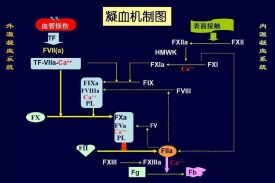
內源性凝血途徑是指參加的凝血因子全部來自血液(內源性)。臨床上常以活化部分凝血活酶時間(APTT)來反映體內內源性凝血途徑的狀況。內源性凝血途徑是指從因子Ⅻ激活,到因子X激活的過程。當血管壁發生損傷,內皮下組織暴露,帶負電荷的內皮下膠原纖維與凝血因子接觸,因子Ⅻ即與之結合,在HK和PK的參與下被活化為Ⅻa。在不依賴鈣離子的條件下,因子Ⅻa將因子Ⅺ激活。在鈣離子的存在下,活化的Ⅺa又激活了因子Ⅸ。單獨的Ⅸa激活因子X的效力相當低,它要與Ⅷa結合形成1:1的複合物,又稱為因子X酶複合物。這一反應還必須有Ca2+和PL共同參與。
外源性凝血途徑:是指參加的凝血因子並非全部存在於血液中,還有外來的凝血因子參與止血。這一過程是從組織因子暴露於血液而啟動,到因子Ⅹ被激活的過程。臨床上以凝血酶原時間測定來反映外源性凝血途徑的狀況。組織因子是存在於多種細胞質膜中的一種特異性跨膜蛋白。當組織損傷后,釋放該因子,在鈣離子的參與下,它與因子Ⅶ一起形成1:1複合物。一般認為,單獨的因子Ⅶ或組織因子均無促凝活性。但因子Ⅶ與組織因子結合會很快被活化的因子Ⅹ激活為Ⅶa,從而形成Ⅶa組織因子複合物,後者比Ⅶa單獨激活因子Ⅹ增強16000倍。外源性凝血所需的時間短,反應迅速。外源性凝血途徑主要受組織因子途徑抑制物(TFPI)調節。TFPI是存在於正常人血漿及血小板和血管內皮細胞中的一種糖蛋白。它通過與因子Ⅹa或因子Ⅶa-組織因子-因子Ⅹa結合形成複合物來抑制因子Ⅹa或因子Ⅶa-組織因子的活性。另外,研究表明,內源凝血和外源凝血途徑可以相互活化。
從因子X被激活至纖維蛋白形成,是內源、外源凝血的共同凝血途徑。主要包括凝血酶生成和纖維蛋白形成兩個階段。
纖維蛋白原被凝血酶酶解為纖維蛋白單體,並交聯形成穩定的纖維蛋白凝塊,這一過程可分為三個階段,纖維蛋白單體的生成,纖維蛋白單體的聚合,纖維蛋白的交聯。纖維蛋白原含有三對多肽鏈,其中纖維蛋白肽A(FPA)和B(FPB)帶較多負電荷,凝血酶將帶負電荷多的纖維蛋白肽A和肽B水解后除去,轉變成纖維蛋白單體。從纖維蛋白分子中釋放出的FPA和FPB可以反映凝血酶的活化程度,因此FPA和FPB的濃度測定也可用於臨床高凝狀態的預測。纖維蛋白單體生成后,即以非共價鍵結合,形成能溶於尿素或氯醋酸中的纖維蛋白多聚體,又稱為可溶性纖維蛋白。纖維蛋白生成后,可促使凝血酶對因子ⅩⅢ的激活,在ⅩⅢa 與鈣離子的參與下,相鄰的纖維蛋白髮生快速共價交聯,形成不溶的穩定的纖維蛋白凝塊。纖維蛋白與凝血酶有高親和力,因此纖維蛋白生成后即能吸附凝血酶,這樣不僅有助於局部血凝塊的形成,而且可以避免凝血酶向循環中擴散。