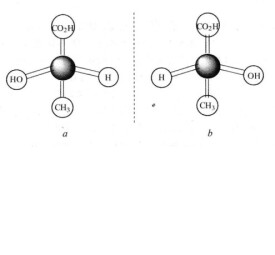
手性碳原子
連有四個不同基團的碳原子
1、手性碳原子一定是飽和碳原子;
2、手性碳原子所連接的四個基團要是不同的。
旋光性:分子的化學結構決定其是否有手性。在有機化合物中,手性分子大多數都含有手性碳原子,所以,一般來說,可以通過判斷分子是否有手性碳原子來斷定分子是否有手性。含有一個手性碳原子的分子一定是個手性分子。一個手性碳原子可以有兩種構型,所以,含有一個手性碳原子的化合物有兩種構型不同的分子,它們組成一對對映異構體,一個使偏振光右旋,另一個使偏振光左旋。因有手性碳原子的存在而存在光學異構體。
手性分子的兩種類型,對其化學性質有很大差別。例如,手性分子的一種構型可以被人體吸收,另一種卻不能被吸收,沒有生理活性,甚至是有害的。
對映異構是指分子式、構造式相同,構型不同,互呈鏡像對映關係的立體異構現象。
分子的手性是對映體存在的必要和充分條件。
對映體——互為物體與鏡象關係的立體異構體。
對映異構體都有旋光性,其中一個是左旋的,一個是右旋的。所以對映異構體又稱為旋光異構體。
含有一個手性碳原子的化合物一定是手性分子。它有兩種不同的構型,是互為實物與鏡象關係的立體異構體,稱 為對映異構體(簡稱為對映體)。
舉例
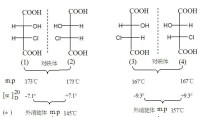
含兩個不同手性碳原子化合物的對映異構
對映體數目—— 2n – 1 = 2(2-1)= 2(對)
舉例
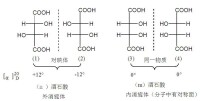
含兩個相同手性碳原子化合物的對映異構
n為偶數:
內消旋體的數目 = 2n / 2 – 1 ,立體異構體總數 = 2 n – 1 + 2 n / 2 – 1
n為奇數:
內消旋體的數目 =2( n – 1 ) / 2 ,立體異構體總數 = 2 n – 1
在這類化合物中兩個手性碳原子所連的四個基團是不完全相同的。含有一個手性碳原子的化合物有一對對映異構體,那麼含有兩個手性碳原子的化合物有幾個對映異構體呢?假使以A和B代表兩個不同的手性碳原子,由於每一個手性碳可以有兩種相反的構型,A+,A-,B+,B-。這樣根據排列組合,整個分子的構型可以有下面四種。
這就是說,含有兩個手性碳原子的化合物,在理論上,可以有四個對映異構體。其中Ⅰ是Ⅳ的鏡象,Ⅱ是Ⅲ的鏡象,所以它們是兩對對映異構體Ⅰ和Ⅱ,或者Ⅲ和Ⅳ,雖然有一部分是呈鏡象關係,但是另一部分是相同的,因此它們不是對映體,而是非對映異構體(Diasteroisomer)。非對映異構體和對映異構體不同,它們之間的性質,不論是物理性質還是化學性質,都不相同。但是由於它們屬於同類化合物,所以化學性質有些相似。
如:氯代蘋果酸,有兩個手性碳原子,它有四個對映異構體,或者兩對對映體。一對對映體的外消旋體的熔點為145°C,從它可以拆分出熔點同為165-166°C比旋光度是+7.1°和-7.5°的兩個氯代蘋果酸。另一對對映體的外消旋體熔點為157°C,從它可以拆分出熔點同為165-166°C,比旋光度是+9.3°和-8.0°的兩個氯代蘋果酸。
一般對映體的比旋光度應該是數值相同,方向相反,可是有的會有些差別,但不太大,這裡就是這個情況。那麼含兩個以上手性碳原子的分子,有多少立體異構體呢?理論推導證明:當分子中含有幾個不相同的手性碳原子時,就可以有2^n個對映異構體,它們可以組成2^n-1個外消旋體。如果分子中含有相同的手性碳原子,其對映異構體的數目可小於2^n。
在這類化合物中,兩個手性碳原子所連的四個基團是完全相同的,如酒石酸,酒石酸分子中兩個手性碳原子都和H,OH,-COOH,四個基團相連接,它也可寫出四個構型的Fischer投影式:Ⅰ和Ⅱ是對映體,它們等量混合可以組成外消旋體。
Ⅲ和Ⅳ也呈鏡象關係,似乎也是對映體,但如果把Ⅲ在紙面上旋轉180°后即得到Ⅳ,因此它們實際上是同一個物質。
從化合物Ⅲ的構型看,如果在下列投影式虛線處放一鏡面,那麼分子上半部分正好是下半部分的鏡象,說明這個分子內有一對稱面。