折點加氯
飲用水消毒方法之一
折點加氯是一種飲用水消毒方法,所屬環境科學。
目錄
當水中有機物主要為氨和氮化物,其實際需氯量滿足后,加氯量增加,余氯量增加,但是後者增長緩慢,一段時間后,加氯量增加,余氯量反而下降,此後加氯量增加,余氯量又上升,此折點后自由性余氯出現,繼續加氯消毒效果最好,即折點加氯。原因:當余氯為化合性氯時,發生反應,使氯胺被氧化為不起消毒作用的化合物,余氯會逐漸減小,但一段時間后,消耗氯的雜質消失,出現自由性余氯時,隨加氯量增加,余氯又會上升。利:當原水受嚴重污染,它能降低水的色度,去除惡臭,降低水中有機物含量,提高混凝效果。弊:水中有機污染物與氯生成三鹵甲烷,必須預處理或深度處理。
廢水中的NH3-N可在適當之pH值,利用氯系的氧化劑(如Cl2、NaOCl)使之氧化成氯胺(NH2Cl、NHCl2、NCl3)之後,再氧化分解成N2氣體而達脫除之目的。此處理方法一般通稱為折點加氯法。氨系廢液及廢水折點加氮法之處理流程如圖所示。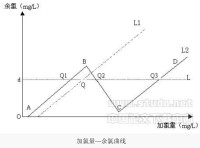

折點加氯
基本原理
NH3 + HOCl → NH2Cl(一氯胺) + H2O
NH2Cl + HOCl → NHCl2(二氯胺) + H2O
NH2Cl + HOCl→ NCl3(三氯胺) + H2O
上述反應與pH值、溫度和接觸時間有關,也與氨和氯的初始比值有關,大多數情況下,以一氯胺和二氯胺兩種形式為主。其中的氯稱為有效化合氯。
