極譜法
極譜法
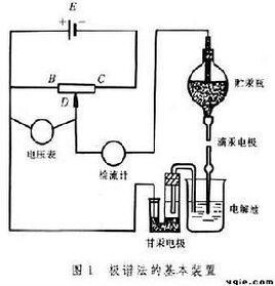
極譜法(polarography)通過測定電解過程中所得到的極化電極的電流-電位(或電位-時間)曲線來確定溶液中被測物質濃度的一類電化學分析方法。於1922年由捷克化學家J.海洛夫斯基建立。極譜法和伏安法的區別在於極化電極的不同。極譜法是使用滴汞電極或其他表面能夠周期性更新的液體電極為極化電極;伏安法是使用表面靜止的液體或固體電極為極化電極。
極譜法和伏安法都是電化學分析法,通過測定電解過程中所得的電流-電壓(或電位-時間)曲線來確定溶液中被測定物質的濃度。它們和同類中其它電化學分析法的區別在於電解池中使用一個極化電極和一個去極化電極。極譜法與伏安法的區別在於極化電極的不同。凡使用滴汞電極或其它表面能夠周期性更新的液體電極者稱極譜法;凡使用表面靜止的液體或固體電極者稱伏安法。
極譜法和伏安法都建立在電解過程的基礎上,電解過程分為兩大類,極譜法和伏安法也相應地分為兩大類:控制電位極譜法和控制電流極譜法。在控制電位極譜法中,極化電極的電位是被控制的對象,是激發訊號;電流是被測量的對象,是響應訊號。在控制電流極譜法中電流是被控制的對象,是激發訊號;電位是被測定的對象,是響應訊號。
控制電位極譜法又細分為恆電位極譜法、交流極譜法、單掃描極譜法、方波極譜法、脈衝極譜法等。控制電流極譜法又細分為計時電位法和示波極譜法等。
極譜法
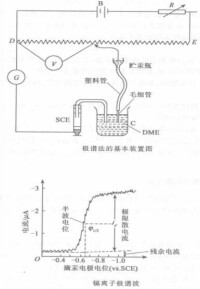
流計G來測量,記錄得到的電流一電壓曲線稱為極譜波。下面以電解氯化鎘的稀溶液為例,說明極譜波產生的過程。將濃度為5×10 mol·L CdCl試液加入電解池中,同時加入約0.1mol·L 的KCl溶液作為支持電解質。通入氮氣或氫氣除去溶解於溶液中的氧,然後使汞滴以每滴3~5s的速度滴下。移動滑線電阻,使兩極上外加電壓從0V到-1V逐漸變化。記下相應的電流值,以電壓為橫坐標,電流為縱坐標繪圖,得到Cd 的電流-電壓曲線,即為鎘離子的極譜波,如圖所示。由圖可見,在未達到Cd 的析出電位時,溶液中只有極微小的電流(殘餘電流)通過。當外加電壓增加到Cd 的析出電位時(在-0.5~-0.6V之間),Cd 開始在滴汞電極上電解;此時在滴汞電極上,Cd 還原為鎘汞齊,在陽極上汞氧化為Hg ,並與溶液中的Cl 生成HgCl:
此時外加電壓稍稍增加,電流就迅速增加,由於濃差極化現象,使Cd 擴散到滴汞電極表面還原,產生電解電流。這種因不斷擴散而引起電極反應所產生的電流稱為擴散電流。但當電壓變化到更負數值時,由於受被測離子擴散速度的限制,電流卻不再增加,而是達到一個極限值,此時的電流稱為極限電流。極限電流減去殘餘電流后,為極限擴散電流,它與溶液中Cd 濃度成正比,以 表達,可作為極譜法定量分析的依據。
極譜圖上的另一特徵是半波電位,即擴散電流為極限擴散電流一半時的滴汞電極的電位。當溶液的組分和溫度一定時,每一種物質的半波電位是一定的,不隨其濃度的變化而改變,可作為定性分析的依據。
極譜法分為控制電位極譜法和控制電流極譜法兩大類。在控制電位極譜法中,電極電位是被控制的激發信號,電流是被測定的響應信號。在控制電流極譜法中,電流是被控制的激發信號,電極電位是被測定的響應信號。控制電位極譜法包括直流極譜法、交流極譜法、單掃描極譜法、方波極譜法、脈衝極譜法等。控制電流極譜法有示波極譜法。此外還有極譜催化波、溶出伏安法。
又稱恆電位極譜法。通過測定電解過程中得到電流-電位曲線來確定溶液中被測成分的濃度。其特點是電極電位改變的速率很慢。它是一種廣泛應用的快速分析方法,適用於測定能在電極上還原或氧化的物質。
將一個小振幅(幾到幾十毫伏)的低頻正弦電壓疊加在直流極譜的直流電壓上面,通過測量電解池的支流電流得到交流極譜波,峰電位等於直流極譜的半波電位E,峰電流 i與被測物質濃度成正比。該法的特點是:①交流極譜波呈峰形,靈敏度比直流極譜高,檢測下限可達到10 mol/L。②解析度高,可分辨峰電位相差40mV的相鄰兩極譜波。③抗干擾能力強,前還原物質不干擾后還原物質的極譜波測量。④疊加的交流電壓使雙電層迅速充放電,充電電流較大,限制了最低可檢測濃度進一步降低。
在一個汞滴生長的後期,其面積基本保持恆定的時候,在電解池兩電極上快速施加一脈衝電壓,同時用示波器觀察在一個滴汞上所產生的電流?電壓曲線。該法的特點是:①極譜波呈峰形,靈敏度比直流極譜法高1~2個數量級,檢測下限可達到10 mol/L。②解析度高,抗干擾能力強。可分辨峰電位相差50mV的相鄰兩極譜波,前還原物質的濃度比后還原物質濃度大100~1000 倍也不干擾測定。③快速施加極化電壓,產生較大的充電電流,故需採取有效補償充電電流的措施。④不可逆過程不出現極譜峰,減小以至完全消除了氧波的干擾。
在通常的、緩慢改變的直流電壓上面、疊加一個低頻率、小振幅(≤50毫伏)的方形波電壓,並在方波電壓改變方向前的一瞬間記錄通過電解池的交流電流的極譜方法稱為方波極譜法。它是極譜法的一種,也是極譜法中靈敏度比較高的方法之一。在合適的情況下,測定的最低濃度可達10 mol/dm ,個別離子的檢出下限達到10 mol/dm 。它所以有很高的靈敏度是由於它在充電電流消失的時刻記錄電流,極譜電流中沒有充電電流,因而可以通過放大電流來提高靈敏度。方波極譜的分辨力好,可以分開Cd波和In波(兩者相差45毫伏)。方波極譜的前面電流對後面電流的影響也小,測定Sn 時,前面Fe 波對Sn 的干擾小,Fe :Sn 可達到20000:1。方波極譜是痕量成分分析的得力的工具。
極譜法的一種,也是目前靈敏度最高的極譜方法。它比方波極譜還要靈敏好幾倍,使用的支持電解質的濃度也比方波極譜低(小至0.02mol/dm )。脈衝極譜有兩種:常規脈衝極譜和示差脈衝極譜。兩者加電壓的方式有差異,極譜圖形也不同。示差脈衝極增加電壓的方式和方波極譜相似,得到的極譜波也相似。和方波極譜不同的是:示差脈衝極譜在一個汞滴的一定時刻,只加上一個方波電壓,ΔE為2一100毫伏,方波電壓持續的時間也比較長,有的長達40一80毫秒,在一個汞滴上只測一次還原電流;而方波極譜在一個汞滴上加很多方波,每一方波持續的時間短,在一個周期中兩次測量電流,既有氧化電流又有還原電流。脈衝極譜加電壓的方式使毛細管雜訊電流得到充分衰減,從而提高了靈敏度。脈衝極譜可檢出10 克/毫升(1ppb)的鎘。分辨力好,兩峰相差25毫伏可以分辨出來。前面極譜電流對後面電流的影響小。
總的說來,用陰極射線示波器來觀察或記錄極譜曲線的極譜方法都可叫示波極譜法。有兩種示波極譜法。一種叫線性變位示波極譜法(單掃描極譜法),另一種叫交流示波極譜法(示波極譜法)。交流示波極譜法,是極譜方法的一種,屬於控制電流極譜法。
常用的示波極譜法的裝置如圖,從這種線路上得到的示波極譜曲線是dE/dt-E曲線。上半部為金屬離子還原得到的曲線(稱陰極支),下半部為金屬氧化得到的曲線(稱陽極支)。切口尖端所對的電位相當於一般極譜波的半波電位。上下兩支的切口對稱,說明該金屬的電極反應是可逆反應。切口的深度反映離子的濃度。利用物質的示波圖形可以鑒定物質,但靈敏度不很高。示波極譜曲線上切口的出現或消失可以指示容量分析的滴定終點,這種滴定方法稱為示波極譜滴定法。
極譜法由於所採用的工作電極和分析測試方式較特殊,因此具有以下一些特點。
氫在汞電極上的超電位很高,即使在酸性介質中,滴汞電極的電位變負至-1.0 V還不致發生氧離子還原的干擾。當滴汞電極作為陽極時,由於汞本身會被氧化,所以其電位變正一般不能超過+0.4 V。在上述適宜電位範圍內,能在電極上還原或氧化的物質,包括無機物和有機物均可以極譜法進行測定,它同時也是一種測定化學反應平衡常數和研究電極反應機理的手段。
一般被測定組分在電解液中的濃度範圍為10 ~10 mol/L,適宜作微量組分的測定。近年也有用它來測定常量組分的。如果採用近代一些極譜分析方法,其可測定的組分在電解液中的濃度可低至10 ~10 mol/L,能進行超微量組分的測定。
由於汞滴不斷更新,工作電極始終保持潔凈,使所得的實驗數據比較準確,重現性也好。一般相對誤差約為1%,使用很精密的儀器其相對誤差可減小到0.5%。
由於工作電極的電位是完全可以控制的,對摺出電位相差約大於50mV的各種金屬離子,可以在工作電極處於不同電極下還原成金屬而產生不相互重疊的極譜波。其既不相互干擾,又可在同一電解液中實現對某些共存金屬離子的連續測定。
還應指出,極譜法工作電極所使用的汞的蒸氣是有毒的,在實驗中應謹防汞的散落和蒸發,用后的汞要及時回收。實驗室要注意通風,並應經常檢查空氣中汞的含量,如超過允許量則應採取措施,可用燃燒碘進行消毒。由於極譜法的這一缺陷,多年來有許多學者致力於尋找其他微電極替代滴汞電極,但效果都不如汞電極。不過,只要在實驗中細心操作,注意改善工作的環境條件,汞電極的這一缺點是完全可以克服的。
極譜法可用來測定大多數金屬離子、許多陰離子和有機化合物(如羰基、硝基、亞硝基化合物,過氧化物、環氧化物,硫醇和共軛雙鍵化合物等)。此外,在電化學、界面化學、絡合物化學和生物化學等方面都有著廣泛的應用。具體應用如下:
1. 金屬元素的測定:Cu、Pb、Cd、Zn、W、Mo、V、Se、Te等元素;
2. 有機物的測定,羰基、亞硝基、有機鹵化物等;
3. 配位化合物的配位數和平衡常數的測定。