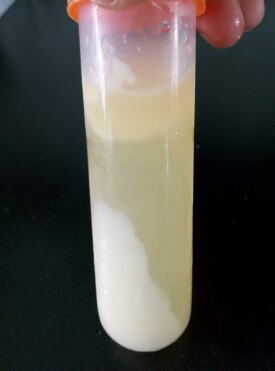
鹽析
溶液加入無機鹽類而使溶解的物質析出的過程
鹽析一般是指溶液中加入無機鹽類而使溶解的物質析出的過程。向某些蛋白質溶液中加入某些無機鹽溶液后,可以降低蛋白質的溶解度,使蛋白質凝聚而從溶液中析出,這種作用叫作鹽析,是物理變化,可復原。但向某些蛋白質溶液中加入某些重金屬鹽,可以使蛋白質性質發生改變而凝聚,進而從溶液中析出,這種作用叫作變性,性質改變,是化學反應,無法復原。
把動物脂肪或植物油與氫氧化鈉按一定比例放在皂化鍋內攪拌加熱,反應后形成的高級脂肪酸鈉、甘油、水形成混合物。往鍋內加入食鹽顆粒,攪拌、靜置,使高級脂肪酸鈉與甘油、水分離,浮在液面。(該反應用以制肥皂)
簡單的說就是利用高濃度中性鹽使蛋白質發生沉澱;蛋白質的溶解度(S)不同,用於沉澱的鹽濃度不同。
(鹽析實驗中的蛋白質溶液不能太稀,而且要現用現配;必須用濃的輕金屬溶液鹽溶液,稀的輕金屬鹽溶液反而能促進蛋白質的溶解。)

鹽析結晶
研究表明,水對陰、陽離子都有較強溶劑化作用,但對陽離子比陰離子有更大的溶劑化作用。因此鹽析劑作用主要表現在鹽析劑陽離子溶劑化作用上。鹽析劑與水結合愈強烈,鹽析效應愈強。由於水合數與離子的大小有關,即離子愈小,水合數就愈大,鹽析效應也愈強。鹽析劑所含陽離子半徑愈小,電荷愈多,則對被鹽析離子的水化層影響愈大,使被鹽析離子脫水愈易,其鹽析效應愈強。所以化工生產中常用的鹽析劑多是離子勢較大的陽離子Li+、Al3+、Fe3+、Mg2+、Sn2+等形成的鹽。我們選擇了這些陽離子所形成的氯化物和硝酸鹽, 並通過探索性實驗,確定選用一種較合適的鹽析劑。
破壞了蛋白質在水中穩定存在的二個因素,從而使蛋白質發生沉澱。
1、破壞了水化層
在高濃度的中性鹽溶液中,由於鹽離子親水性比蛋白質強,與蛋白質膠粒爭奪與水結合,破壞了蛋白質的水化層。在高濃度的中性鹽溶液中,由於蛋白質和鹽離子對溶液中水分子都有吸引力,產生與水化合現象,但它們之間有競爭作用,當大量中性鹽加入時,使得鹽解離產生的離子爭奪了溶液中大部分自由水,從而破壞蛋白質的水化作用,引起蛋白質溶解度降低,故從溶液中沉澱出來。
2、破壞了電荷
由於鹽是強電解質,解離作用強,鹽的解離可抑制蛋白質弱電解質的解離,使蛋白質帶電荷減少,更容易聚集析出。
在中性配合萃取和離子締合萃取體系中,使用鹽析劑可提高被萃取組分的分配係數。鹽析劑是一種不被萃取、不與被萃物結合,但與被萃物有相同的陰離子從而使分配係數顯著提高的無機化合物。通常鹽析劑的陽離子在鹽析過程中,因在水溶液中有強烈的水合作用,能吸引大量自由水分子,降低水溶液中自由水分子濃度,可相對增加被萃物在水相中的濃度,有利於被萃物萃入有機相。一般來說,鹽析劑中的金屬陽離子的電荷數越大,鹽析作用越強。在陽離子的電荷數相同的情況下,鹽析作用與陽離子的半徑成反比,這是因為價態高半徑小的陽離子的水化能力較強,所以使自由水分子減少的作用較大。一般金屬離子的鹽析效應按下列次序遞減:
Al>Fe>Mg>Ca>Li>Na>NH4>K
鹽析劑的選擇除應考慮鹽析作用外,還要考慮不影響下一步的分離和提純、價格便宜、來源充足、水中溶解度大等因素。通常以NH4N03的應用最為普遍。
不會引起蛋白質變性,經透析去鹽后,能得到保持生物活性的純化蛋白質。
鹽析的成敗決定於溶液的pH值與離子強度,PH愈接近蛋白質的等電點,蛋白質就愈易沉澱。不同的蛋白質的溶解度與等電點不同,沉澱時所需的pH值與離子強度也不相同,故改變鹽的濃度與溶液的pH值,便可將混合液中的蛋白質逐個鹽析分開,這種分離蛋白質的方法稱為分段鹽析法(fractional salting out)。例如半飽和硫酸銨可沉澱血漿球蛋白,飽和硫酸銨則沉澱血漿清蛋白。
可以把發黃的白襯衫放在5%食鹽水中浸泡1小時,再慢慢搓乾淨;或將衣服浸於10%的濃鹽水中,泡1-2小時,取出用清水漂洗乾淨。衣領部位的污漬可以單獨加一些細鹽粒輕輕搓洗效果更佳。應當注意的是衣服應當用涼水浸泡,切勿使用熱水。
蛋白質四級結構
| 總覽 | ▪ 球狀蛋白質▪ 纖維蛋白▪ 膜蛋白▪ 捲曲螺旋 |
|---|
| 二聚體 | ▪ 亮氨酸拉鏈▪ 色氨酸阻遏物▪ 谷胱甘肽-S-轉移酶 |
|---|
| 三聚體 | ▪ 膠原蛋白▪ 血球凝集素▪ 鳥氨酸氨甲醯轉移酶 |
|---|
| 四聚體 | ▪ 血紅蛋白▪ 免疫球蛋白G▪ 抗生物素蛋白▪ 血影蛋白 |
|---|
| 六聚體 | ▪ dnaB螺旋酶▪ 血青蛋白▪ 谷氨酸脫氫酶1 |
|---|
| 八聚體 | ▪ 核小體▪ 蚯蚓血紅蛋白 |
|---|
| 原纖維 | ▪ 肌動蛋白▪ 微管蛋白▪ 鞭毛▪ 性菌毛 |
|---|
| 複合物 | ▪ 起始前複合物▪ 免疫球蛋白M |
|---|
| 機器 | ▪ 蛋白酶體▪ 核糖體▪ 三磷酸腺苷合酶▪ RNA聚合酶▪ 剪接體 |
|---|
| 病毒 | ▪ 衣殼 |
|---|
| 沉澱 | ▪ 鹽析▪ 霍夫邁斯特序列 |
|---|
| 技術 | ▪ 超速離心法▪ 分子排阻色譜 |
|---|
三級結構結構測定方法
生物化學與分子生物學方法與技術
| ▪ 鹽溶 | ▪ 鹽析 | ▪ 脫鹽 | ▪ 逆流分配 | ▪ 分級[分離] |
| ▪ 硫酸銨分級 | ▪ 分級沉澱 | ▪ 透析 | ▪ 反向透析 | ▪ 平衡透析法 |
| ▪ 電透析 | ▪ 透析袋 | ▪ 透析液 | ▪ 反相滲透 | ▪ 過濾 |
| ▪ 微孔過濾 | ▪ 超濾 | ▪ 超濾濃縮 | ▪ 超濾膜 | ▪ 超濾器 |
| ▪ 中空纖維 | ▪ 膜片鉗 | ▪ 膜濾器 | ▪ 膜過濾 | ▪ 膜滲透壓計 |
| ▪ 選擇通透膜 | ▪ 表觀相對分子量 | ▪ 截留分子量 | ▪ 超量原子百分數 | ▪ 生理鹽水 |
| ▪ 冷凍蝕刻 | ▪ 冷凍撕裂 | ▪ 凍融 | ▪ 弗氏細胞壓碎器 | ▪ 勻漿器 |
| ▪ 冷凍乾燥 | ▪ 凍干儀 | ▪ 范斯萊克儀 | ▪ 漩渦振蕩器 | ▪ 瓦爾堡呼吸計 |
| ▪ 瓦氏高速搗碎器 | ▪ 黏度計 | ▪ 吸收池 | ▪ 比濁法 | ▪ 波-伊勻漿器 |
| ▪ 旋轉蒸發器 | ▪ 索氏提取器 | ▪ 同步加速器 | ▪ 合成儀 | ▪ 離心 |
| ▪ 離心速度 | ▪ 相對離心力 | ▪ 角轉頭 | ▪ 吊籃式轉頭 | ▪ 垂直轉頭 |
| 其他科技名詞 | ||||