霍夫曼反應
霍夫曼反應
霍夫曼反應按“接近E1cb的E2”的機理進行(見消除反應),但過程中並不生成共軛鹼負碳離子。
四級銨鹼加熱至100℃以上分解成烯烴、三級胺和水的反應。1881年由德國化學家A.W.von霍夫曼首先發現。霍夫曼反應可用於製備某些烯烴,還可用於測定複雜胺類和生物鹼的結構。把未知的含氮化合物與過量碘甲烷作用,使之轉變為四級銨鹽,用濕氧化銀處理即得四級銨鹼,加熱發生分解。根據所消耗碘甲烷和含氮未知物的摩爾比,可判斷該化合物是否為一級、二級或三級胺,並從所生成烯烴的結構推測該化合物的結構。霍夫曼曾用此法研究一些哌啶類化合物的結構。由於在反應中使用過量碘甲烷使未知物轉變為四級銨鹽,故又稱為徹底甲基化反應。
鹼進攻四級銨正離子中的一個 β碳原子上的氫( β氫原子),並促使離去基團三級胺的斷裂和雙鍵的生成。當四級銨正離子中含有結構不等同的幾個 β氫原子時,反應趨向於生成雙鍵上取代基最少的取代乙烯,即被鹼作用的速率以 β碳為CH₃的氫最快,為CH₂R的氫次之,為CHR₂的氫最慢。例如,二級丁胺經霍夫曼反應所得的烯烴中1-丁烯佔95%,而 2-丁烯只佔5%。這種規律性也存在於不同烷基之間的競爭中,例如丁基異丁基胺經霍夫曼反應所得烯烴中1-丁烯佔64%,異丁烯只佔36%。這種規律性稱霍夫曼規則。
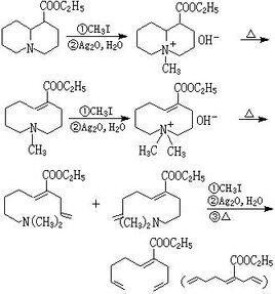
含氮雜環中的二級胺和三級胺可通過兩次或三次霍夫曼反應,生成二烯或三烯,例如: