共找到2條詞條名為酶催化的結果 展開
- 酶催化
- 酶促反應
酶催化
酶催化
酶催化可以看作是介於均相與非均相催化反應之間的一種催化反應。既可以看成是反應物與酶形成了中間化合物,也可以看成是在酶的表面上首先吸附了反應物,然後再進行反應。
酶加速或減慢化學反應的作用。在一個活細胞中同時進行的幾百種不同的反應都是藉助於細胞內含有的相當數目的酶完成的。它們在催化反應專一性,催化效率以及對溫度、pH值的敏感等方面表現出一般工業催化劑所沒有的特性。在許多情況下,底物分子中微小的結構變化會喪失一個化合物作為底物的能力。
尿素酶只能催化尿素,使之水解為氨和二氧化碳,而對結構非常相似的甲基尿素卻毫無 作用。有些酶表現的專一性程度低一些,能作用於具有某種特殊化學基團的多種化合物。酶的催化效率顯然比其他類型催化劑高,在一定條件下,每個過氧化氫酶在一分鐘內能轉化5000000個過氧化氫分子,比其他催化劑效率要高几個數量級。在化學實驗室中需幾天或幾個月才能完成的複雜反應序列,酶能在數秒鐘之內催化完成。
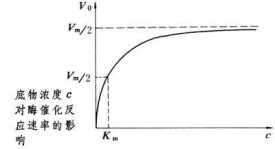
酶催化反應還表現出一種在非酶促反應中不常見到的特徵,即可與底物飽和。當底物濃度增加時,酶反應速率達到平衡並接近一個最大值Vm(見圖)。
1913年L.邁克利斯和L.M.門頓發展了關於酶的作用和動力學的一般理論,假定酶E首先與底物S結合形成酶-底物複合物ES;然後此複合物在第二步反應中分解形成遊離的酶和產物P:
在動力學研究中通常使用的條件下,酶的濃度與底物相比是非常低的。當酶和底物混合后,ES的濃度迅速增加直至到達恆態,這種恆態通常在很短時間內就能達到,並可維持一段時間,在這段時間內,整個反應的速率基本上是恆定的。該速率被稱為反應的初速率V0,它可用產物的生成速率來測量:式中【Et】為總的酶濃度;c為底物的濃度;k1、k2、k3為反應速率常數。當底物濃度無窮大時,初速率接近最大值Vm,。定義,則得:
式中Km稱為邁克利斯常數,代表在給定的酶濃度下,反應速率達到最大值的一半時所需的底物濃度。當k3與k2相比很小時,Km就接近於酶-底物絡合物的離解常數,可作為酶與其底物親和力的量度。
已知有將近2000種不同的酶,其中至少已有 200種已制出結晶物質。大多數酶都是蛋白質,其分子量範圍約從10000到1000000以上。通常按照酶所催化的反應來分類和定名。如氧化還原酶可催化電子傳遞反應,在細胞呼吸和能量產生中起著重要的作用;轉移酶可催化一種化學基團,從一個底物轉移到另一底物;水解酶可催化蛋白質、核酸、澱粉、脂肪、磷酸酯及其他物質的水解;裂合酶可催化底物發生非水解性裂解並生成雙鍵;異構酶可催化異構物相互轉化等。
有些酶類的活性僅由它們的蛋白質結構所決定,而另一些酶類還需要一種或多種的非蛋白質組分,稱為輔助因子。輔助因子可以是金屬離子或金屬絡合物,也可以是被稱為輔酶的有機分子;有些酶類兩者都需要。
在自然界中,大約有三分之一的酶需要金屬離子作為輔助因子或活化劑。有些含金屬的酶,其所含的金屬離子,特別是鐵、鉬、銅、鋅等過渡金屬離子與蛋白質部分牢固地結合,形成酶的活性部位。這種酶稱為金屬酶,例如使大氣中遊離的氮分子固定為氨的、含鉬和鐵的固氮酶;使底物氧化同時將氧分子還原為水的銅氧化酶;使H2(或H+)轉化為H+(或H2)的含鐵、硫的氫酶;一類含鉬的氧化還原酶(如硝酸鹽還原酶、嘌呤脫氫酶、黃嘌呤氧化酶、醛氧化酶、亞硫酸氧化酶和甲酸脫氫酶)等。在這些酶的大分子內部含有由若干金屬原子組成的原子簇,作為活性中心,以絡合活化底物分子。它們使底物絡合活化的方式和通過配位體實現電子與能量偶聯傳遞的原理,與相應的均相絡合催化和多相絡合催化過程有相似的地方。
弄清自然界在億萬年進化過程中巧妙設計的各種酶作用機理,不僅能揭開生物催化過程的奧秒,也能為人類利用其中某些原理來研究開發新型高效催化劑奠定科學基礎,並帶動催化的邊緣學科──光助催化、電催化和光電催化──的發展。