DPPH
用於光度測定生育酚等的化合物
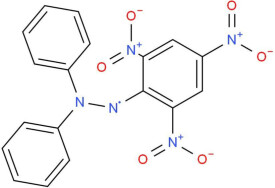
1,1-二苯基-2-三硝基苯肼,別名1,1-二苯基-2-苦肼基(自由基);1,2-二苦基-2-三硝基苯亞肼;1,2-二苯基-2-苦肼基。是一個穩定的自由基,為暗紫色稜柱狀結晶,熔點127~129℃(分解)。最大吸收波長528nm。可用於 光度測定生育酚和脂肪族硫醇類、還原物質的分析試劑,也是常用的阻聚劑。
本品應密封於0℃保存。
1,1-二苯基-2-三硝基苯肼(1,1-Diphenyl-2-picrylhydrazyl radical 2,2-Diphenyl-1-(2,4,6-trinitrophenyl)hydrazyl )
暗紫色大稜柱形晶體。一般試劑含量不小於98%。
該品具有刺激性。吸入、口服或皮膚接觸有害。大量使用應穿適當的防護服和戴手套。
DPPH有兩個主要的應用,都用於實驗室研究中:一是在含有自由基的化學反應中作為一種監測反應的物質,典型的用於抗氧化成分的體外抗氧化性評價;還可以作為電子順磁共振信號位置和強度的標準物質。
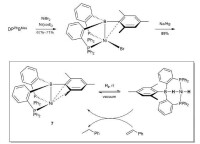
DPPH具有幾個不同結晶形態,它們的晶格對稱性和熔點(m.p.)存在差異。商品化的粉末是不同晶相的混合物,熔點在130℃附近。DPPH-Ⅰ(m.p. 106℃)是正交晶系,DPPH-Ⅱ(m.p. 137℃)是無定形態,DPPH-Ⅲ(m.p. 128-129℃)是三斜晶系。
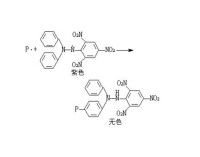
DPPH是一種很穩定的氮中心的自由基,它的穩定性主要來自3個苯環的共振穩定作用及空間障礙,使夾在中間的氮原子上不成對的電子不能發揮其應有的電子成對作用。作為一種穩定的自由基,DPPH可以捕獲(“清除”)其他的自由基。因此通過加入DPPH后觀察某一化學反應的速率是否減慢,來作為這一反應是否具有自由基反應本質的指標。由於DPPH自由基在以300~400之間為中心處具有強烈的吸收,因此在溶液中呈現深紫色,並且在被中和之後會變為無色或淺黃色。利用這一特性可以直觀地檢測反應的過程,通過記錄DPPH在在520nm吸光度值或者EPR信號的變化可以得到初始自由基的量。
DPPH
DPPH
DPPH法於1958年被提出,廣泛用於定量測定生物試樣和食品的抗氧化能力。此法是根據DPPH自由基有單電子,在517nm處有一強吸收,其醇溶液呈紫色的特性。當有自由基清除劑存在時,由於與其單電子配對而使其吸收逐漸消失,其褪色程度與其接受的電子數量成定量關係,因而可用分光光度計進行快速的定量分析。
1.用無水乙醇配置 0.1mmol/L 的DPPH溶液,避光保存。配置 0.5mg/mL 的Vc溶液(作為對照)。將測試樣品稀釋至不同濃度。
2.將2mL測試樣品溶液及 2mL DPPH 溶液加入到同一試管中,搖勻,室溫下暗處靜置 30min 后測定其吸光度A sample,同時測定 2mL DPPH溶液與 2mL 溶劑(蒸餾水或者相應的緩衝溶液)混合后的吸光度 A control,以及2mL測試樣品溶液與2mL無水乙醇混合后的吸光度A blank。
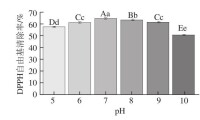
3.自由基清除能力的表示:
DPPH
由於DPPH是脂溶性的,因而與細胞的水性環境不匹配。現已提出了其替代法,即PTIO自由基清除法。該法可以在水溶液(或pH7.4緩衝溶液)中進行,具有較好的生物相關性。