固溶體
固溶體
固溶體是指溶質原子溶入溶劑晶格中而仍保持溶劑類型的合金相。通常以一種化學物質為基體溶有其他物質的原子或分子所組成的晶體,在合金和硅酸鹽系統中較多見,在多原子物質中亦存在。
當溶劑的晶體結構添加溶質后可以穩定存在且保持均相,則該種混合物可以被視作溶液。
一些混合物可以在很多種濃度情況下形成固溶體,而有一些混合物根本不能形成固溶體。兩種物質混合而形成固溶體的傾向是一個複雜的事情,涉及化學、晶體學及量子物理學。
所謂固溶體(solid solution)是指溶質原子溶入溶劑晶格中而仍保持溶劑類型的合金相。
這種相稱為固溶體,這種組元稱為溶劑,其它的組元即為溶質。工業上所使用的金屬材料,絕大部分是以固溶體為基體的,有的甚至完全由固溶體所組成。例如,廣泛用的碳鋼和合金鋼,均以固溶體為基體相,其含量占組織中的絕大部分。因此,對固溶體的研究有很重要的實際意義。
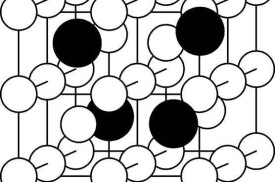
當一種組元A加到另一種組元B中形成的固體其結構仍保留為組元B的結構時,這種固體稱為固溶體.B組元稱為溶劑,A組元稱為溶質。組元A、B可以是元素,可以是化合物。固溶體分成置換式固溶體和間隙式固溶體兩大類。置換式固溶體溶質原子處於溶劑原子的位置上,即置換了溶劑原子,如α黃銅中,鋅置換了銅原子;間隙式固溶體是溶質原子處於溶劑原子的間隙處,如α鐵中,碳原子處在鐵原子排列的間隙處。
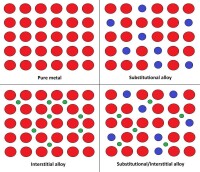
左上:純金屬,右上:置換固溶體, 左下:間隙固溶體,右下:混合。
1、置換固溶體:溶質原子佔據溶劑晶格中的結點位置而形成的固溶體稱置換固溶體。當溶劑和溶質原子直徑相差不大,一般在15%以內時,易於形成置換固溶體。銅鎳二元合金即形成置換固溶體,鎳原子可在銅晶格的任意位置替代銅原子。
2、間隙固溶體:溶質原子分佈於溶劑晶格間隙而形成的固溶體稱間隙固溶體。間隙固溶體的溶劑是直徑較大的過渡族金屬,而溶質是直徑很小的碳、氫等非金屬元素。其形成條件是溶質原子與溶劑原子直徑之比必須小於0.59。如鐵碳合金中,鐵和碳所形成的固溶體――鐵素體和奧氏體,皆為間隙固溶體。
按固溶度來分類:可分為有限固溶體和無限固溶體。無限固溶體只可能是置換固溶體。
按溶質原子與溶劑原子的相對分佈來分;可分為無序固溶體和有序固溶體。
在討論固溶體的概念時,認為溶質質點(原子、離子)在溶劑晶體結構中的分佈是任意的、無規則的,這便是無序固溶體的概念。例如,晶胞參數的測定,實際上是一個平均值;密度的測定也是統計的結果。固溶體中溶質質點無規則分佈的概念,和實驗結果基本一致。
有些固溶體中溶質質點的分佈是有序的,即溶質質點在結構中按一定規律排列,形成所謂“有序固溶體”。例如,Au-Cu固溶體,Au和Cu都是面心立方格子,它們之間可以形成連續置換固溶體。在一般情況下,Au和Cu原子是無規則的分佈在面心立方格子的結點上,這便是一般認為的固溶體(圖5-47(a))。但是,如果這個固溶體的組成為AuCu和AuCu時,並且在適當的溫度下進行較長時間退火,則固溶體的結構可轉變為“有序結構”。這表現為AuCu組成中,所有的Au原子佔有面心立方格子的頂角位置,而Cu原子則佔有面心立方格子的面心位置。因而,從單位晶胞來看組成應為AuCu。同理,如果Au原子和Cu原子分層相間分佈,也形成“有序結構”,其相應的組成應為AuCu。這種有序結構稱為超結構。它除了和組成有關外,還和晶體形成時的溫度、壓力條件有關。
(1)固溶強化:當溶質元素含量很少時,固溶體性能與溶劑金屬性能基本相同。但隨溶質元素含量的增多,會使金屬的強度和硬度升高,而塑性和韌性有所下降,這種現象稱為固溶強化。置換固溶體和間隙固溶體都會產生固溶強化現象。
適當控制溶質含量,可明顯提高強度和硬度,同時仍能保證足夠高的塑性和韌性,所以說固溶體一般具有較好的綜合力學性能。因此要求有綜合力學性能的結構材料,幾乎都以固溶體作為基本相。這就是固溶強化成為一種重要強化方法,在工業生產中得以廣泛應用的原因。
(2)固溶度:是金屬在固體狀態下的溶解度,合金元素要溶解在固態的鋼中,前提是將鋼加熱到奧氏體化后,奧氏體晶格間的間隙較大,能夠溶解更多的合金元素。
(3)固溶熱處理:將合金加熱至高溫單相區恆溫保持,使過剩相充分快速冷卻,以得到過飽和固溶體的熱處理工藝。時效處理可分為自然時效和人工時效兩種。自然時效是將鑄件置於露天場地半年以上,使其緩緩地發生形變,從而使殘餘應力消除或減少,人工時效是將鑄件加熱到550~650℃進行去應力退火,它比自然時效節省時間,殘餘應力去除較為徹底.
根據合金本性和用途確定採用何種時效方法。高溫下工作的鋁合金適宜用人工時效,室溫下工作的鋁合金有些採用自然時效,有些必須人工時效。從合金強化相上來分析,含有S相和CuAl等相的合金,一般採用自然時效,而需要在高溫下使用或為了提高合金的屈服強度時,就需要採用人工時效來強化。比如LY11和LY12,40度以下自然時效可以得到高的強度和耐蝕性,對於150度以上工作的LY12和125-250度工作的LY6鉚釘用合金則需要人時效。含有主要強化相為MgSi,MgZn的T相的合金,只有採用人工時效強化,才能達到它的最高強度。
(4)固溶體的電性能:固溶體的電性能隨著雜質(溶質)濃度的變化,一般出現連續的甚至是線性的變化;然而,在相界上往往出現突變。例如PbTiO3和PbZrO3都不是性能優良的壓電陶瓷。PbTiO是鐵電體,相變時伴隨著晶胞參數的劇烈變化,冷卻至室溫時,一般會發生開裂,所以沒有純的PbTiO陶瓷。PbZrO是反鐵電體。這兩個化合物結構相同,Zr4+和Ti4+尺寸差不多,可生成連續固溶體Pb(ZryTi1–y)O,其中y=0~1。隨著固溶體組成的不同,常溫下有不同的晶體結構。在PbZrO–PbTiO系統中發生的是等價置換,形成的固溶體結構完整,電場基本均衡,電導沒有顯著變化,一般情況下,介電性能也改變不大。但在三方(rhombohedral)結構和四方(tetragonal)結構的晶型邊界(MPB)處,獲得的固溶體PZT的介電常數和壓電性能皆優於純粹的PbTiO和PbZrO其燒結性能也很好。異價置換會產生離子性缺陷,引起材料導電性能的重大變化,而且,這個改變是與雜質缺陷濃度成比例的。
ZrO是一種高溫耐火材料,熔點2680℃,但發生相變時伴隨很大的體積收縮,這對高溫結構材料是致命的。若加入CaO,則和ZrO形成固溶體,無晶型轉變,體積效應減少,使ZrO成為一種很好的高溫結構材料。
形成固溶體后,晶格結構有一定畸變,處於高能量的活化狀態,有利於進行化學反應。如,AlO熔點高(2050℃),不利於燒結,若加入TiO,可使燒結溫度下降到1600℃,這是因為AlO與TiO形成固溶體,Ti置換Al后,帶正電,為平衡電價,產生了正離子空位,加快擴散,有利於燒結進行。
定義:固溶體的強度與硬度往往高於各組元,而塑性則較低,稱為固溶強化。
固溶強化的特點和規律:固溶強化的程度(或效果)不僅取決與它的成分,還取決與固溶體的類型、結構特點、固溶度、組元原子半徑差等一系列因素。
1)間隙式溶質原子的強化效果一般要比置換式溶質原子更顯著。
2)溶質和溶劑原子尺寸相差越大或固溶度越小,固溶強化越顯著。
PbTiO是一種鐵電體,純PbTiO燒結性能極差,居里點為490℃,發生相變時,晶格常數劇烈變化,在常溫下發生開裂。PbZrO是一種反鐵電體,居里點為230℃。兩者結構相同,Zr、Ti離子尺寸相差不多,能在常溫生成連續固溶體Pb(ZrxTi1-x)O,x=0.1~0.3。在斜方鐵電體和四方鐵電體的邊
界組成Pb(Zr0.54Ti0.46)O處,壓電性能、介電常數都達到最大值,燒結性能也很好,被命名為PZT陶瓷。