共找到2條詞條名為氯化金的結果 展開
- 氯化金
- 氯金酸
氯化金
氯化金
氯化金,是最常見的無機金化合物,化學式是AuCl3。名稱中的羅馬數字錶明金的化合價為+3,這是它眾多化合物中最為穩定的價態。金亦會形成另一種氯化物——氯化亞金(AuCl),它沒有AuCl3穩定。另外,把金溶於王水中便會產生氯金酸(HAuCl4),有時也會稱為:“三氯化金”、“四氯合金酸”或是“三水合氯化金(III)”
氯化金(III)吸濕性很強,極易溶於水及乙醇。溫度高於160 °C或光照時會分解,併產生多種有大量配體的配合物。
固態和氣態的三氯化金都是二聚物;金的溴化物—— 也是如此。兩個Au分別位於兩個正方平面的中心。此結構稱為平面型結構,及 也屬於這個結構。中的化學鍵主要是共價的,反映了它的高化合價和相對高的電負性。
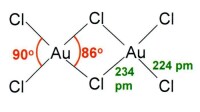
三氯化金的結構
最常用的製備氯化金(III)的方法,是直接在高溫中氯化該金屬:
2Au + 3 → 2
用王水與金反應可得到氯化金:
Au+ +3HCl= +NO↑+2
化學性質極不穩定,加熱極易分解。常溫下水溶液呈無色。能與可溶性鹼反應:
+3NaOH= +3NaCl
+3KOH= +3KCl
而一般不能與酸反應。
金(III)鹽,特別是(由與NaCl反應製得),可取代有毒的汞(II)鹽作為炔烴反應的催化劑。例如,通過終端炔烴的水合作用來製備甲基酮。
一般在這些條件下,酮的產量可達到90%。還有一個用途是在炔烴的胺化反應中作為催化劑。近年,開始引起有機化學家的青睞,因為它可作為其他化學反應的弱酸性催化劑,例如︰芳香烴的烷基化反應,以及把呋喃轉換成苯酚(見下)。有機物的合成以及在製藥工業中也會用到此化學反應。例如︰2-甲基呋喃(斯而烷)可在第5位置與甲基乙烯基酮順利發生烷基化反應。
常溫下,用甲基腈中1 mole%的只需進行40分鐘的反應便可產生91%的產物。這個量量值得注意,因為呋喃和酮通常在酸性環境下極易發生聚合反應等的副反應。有時當炔烴存在時,會生成苯酚。
看法:認為氯金酸和氯化金是同一種物質。
解析:氯金酸是由三氯化金溶於濃鹽酸得到的,氯化金是一種鹽。
氯金酸化學式HAuCl·4HO。分子量411.85。黃色針 狀晶體。有毒! 有腐蝕性。易溶於水,溶於乙醇、乙醚,微 溶於三氯甲烷。受熱分解。曝光生成黑色斑點,熱至120℃ 分解為三氯化金。在鹼性溶液中與KI反應可沉澱出褐色 的金。在酸性溶液中遇二氯化錫則生成“桂皮紫色”。用甲 基橙使其水溶液呈紫色,滴1~3滴鹽酸使變綠色,再遇 金鹽溶液則變成淡紫色;加入冷的氫氧化鉀溶液生成氫 氧化金沉澱,通入二氧化硫則被還原成金粉。製法:將純 金溶於王水(或為氯氣飽和的鹽酸)中經蒸餾、結晶即得。用途:用於電鍍金和照相術,制金粉、紅玻璃、醫治結核病 的藥物,還可用於Rb、Cs的微量分析。
三氯化金刺激性很強,處理三氯化金時應戴上手套及護目鏡,避免直接接觸物料,若不小心沾上應當立即就醫。
