DNA二級結構
J·Watson和F·Crick提出的結構
DNA的二級結構是指兩條多核苷酸鏈反向平行盤繞所生成的雙螺旋結構。兩條多核苷酸鏈以相同的旋轉繞同一個公共軸形成右手雙螺旋,螺旋的直徑2.0nm;兩條多核苷酸鏈是反向平行的,一條5’-3方向,另一條3’-5’方向;兩條多核苷酸鏈的糖-磷酸骨架位於雙螺旋外側,鹼基平面位於鏈的內側;相鄰鹼基對之間的軸向距離為0.34nm,每個螺旋的軸距為3.4nm。
DNA二級結構的穩定作用力有兩條多核苷酸鏈間的互補鹼基對之間的氫鍵;鹼基對疏水的芳香環堆積所產生的疏水作用力,以及堆積的鹼基對間的范德華力;磷酸基團上的負電荷與介質中的陽離子化合物之間形成的鹽鍵。
1951年11月,英國科學家M. Wilkins和R▪Franklin獲得了高質量的DNA分子X線衍射照片。在綜合前人研究結果的基礎上,J▪Watson和F▪Crick提出了DNA分子雙螺旋結構的模型,於1953年發表於《Nature》雜誌。這一發現揭示了生物界遺傳性狀得以世代相傳的分子機制,它不僅解釋了當時已知的DNA理化性質,還將DNA的功能與結構聯繫起來,奠定了現代生命科學的基礎。
1.兩條多核苷酸鏈以相同的旋轉繞同一個公共軸形成右手雙螺旋,螺旋的直徑2.0nm
2.兩條多核苷酸鏈是反向平行的,一條5’-3’,另一條3’-5’
3.兩條多核苷酸鏈的糖-磷酸骨架位於雙螺旋外側,鹼基平面位於鏈的內側
4相鄰鹼基對之間的軸向距離為0.34nm,每個螺旋的軸距為3.4nm
DNA二級結構的穩定作用力
1.兩條多核苷酸鏈間的互補鹼基對之間的氫鍵
2.鹼基對疏水的芳香環堆積所產生的疏水作用力,以及堆積的鹼基對間的范德華力,
3.磷酸集團上的負電荷與介質中的陽離子化合物之間形成的鹽鍵
人們在20世紀初就已經知道基因位於染色體上,科學家也急於搞清楚染色體上的基因的化學本質。起初,大多數科學家認為蛋白質是遺傳物質,而不是DNA,直到1944年 Avery等利用從致病肺炎球菌中提取的DNA使另一種非致病性肺炎球菌的遺傳性狀改變而成為致病菌,證實了遺傳物質是DNA而不是蛋白質。人們才逐漸將核酸化學的研究和細胞的功能聯繫起來。
1951年, Pauling利用X線晶體衍射技術成功發現了蛋白質的α螺旋結構,這一成果的發現對DNA二級結構的發現也起了很重要的啟發作用,引發人們思考DNA分子是否也同樣具有這個類似的螺旋結構。同年, Wilkins和 Frankin利用X線晶體衍射DNA技術成功獲得了高質量的DNA分子結構照片,分析結果表明DNA是螺旋狀分子,並且從密度上也提示了DNA以雙鏈的形式存在。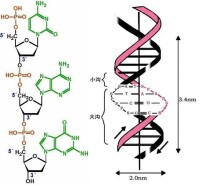

DNA二級結構
1952年, Erwin changan等人採用層析和紫外吸收分析等技術研究了DNA分子的鹼基成分,提岀了以下有關DNA分子的鹼基組成的 Chargaff規則:①腺嘌呤與胸腺嘧啶的摩爾數總是相等(A=T),鳥嘌呤的含量總是與胞嘧啶相等(G=C);②不同生物種屬的DNA鹼基組成不同;③同一個體不同器官、不同組織的DNA具有相同的鹼基組成。預示了DNA分子中的鹼基A與T,G與C以互補配對方式存在的可能性。
1953年,美國生物學家 Watson和英國物理學家 Crick合作在英國劍橋卡文迪許研究所巧妙地綜合了當時所能夠得到的關於DNA結構研究成果,揭示出核酸的化學結構,提岀脫氧核糖核酸(DNA)分子結構的雙螺旋模型,即著名的“Wasn-Cick模型”,這一模型的提出是生物學發展史上的里程碑,後來被譽為“20世紀生物學中最偉大的發現”和“生物學中的決定性突破”,又被視為分子生物學誕生的標誌,為今天生物工程學的蓬勃發展開闢了道路。1989年,美國科學家用“掃描隧道顯微鏡”直接觀察到了脫氧核糖核酸的雙螺旋結構。
Watson和 Crick提出DNA雙螺旋結構模型主要依據:①已知核酸化學結構和核苷酸鍵長與鍵角的數據;② Chargaff規則為DNA二級結構模型的建立提供了一個有力的證據,細胞中的DNA分子幾乎都是由雙鏈分子構成的,對其組成成分的結晶學和物理化學研究表明,A和T、C和G可形成配對關係;③對DNA纖維進行X線衍射分析獲得的精確結果。
1953年,弗朗西斯·克里克、傑姆斯·沃森、莫里斯·威爾金斯、羅莎琳·富蘭克林發現了DNA雙螺旋的結構,開啟了分子生物學時代。分子生物學使生物大分子的研究進入一個新的階段,使遺傳的研究深入到分子層次,“生命之謎”被打開,人們清楚地了解遺傳信息的構成和傳遞的途徑
1962年10月,瑞典卡羅林斯卡醫學院諾貝爾生理學或醫學獎評選委員會宣布,當年的諾貝爾生理學或醫學獎授予英國的莫里斯·威爾金斯、弗朗西斯·克里克和美國的傑姆斯·沃森,理由是他們發現並證明了細胞核DNA的雙螺旋結構,這對於研究和認識生命現象與本質具有重要意義
Watson和Crick提出的DNA雙螺旋結構具有下列特DNA二級結構征。
(1) DNA由兩條反向平行的多聚脫氧核苷酸鏈形成右手螺旋:一條鏈的5’-3方向是自上而下,而另一條鏈的3’-5’方向是自下而上,稱為反向平行,它們圍繞著同一個螺旋軸旋轉而形成右手螺旋。
(2)由脫氧核糖和磷酸基團構成的親水性骨架位於雙螺旋結構的外側,而疏水的鹼基位於內側。
(3)位於DNA雙鏈內側的鹼基以氫鍵結合,形成了互補鹼基對:一條鏈上的腺嘌呤(A)與另一條鏈上的胸腺嘧啶(T)形成了2個氫鍵;一條鏈上的鳥嘌呤(G)與另一條鏈上的胞嘧啶(C)形成了3個氫鍵這種鹼基配對關係稱為互補鹼基對,DNA的兩條鏈則稱為互補鏈
(4)鹼基對平面與雙螺旋的螺旋軸垂直,每兩個相鄰的鹼基對平面之間的垂直距離為0. 34 nm,每一個螺旋含有10.5個鹼基對,螺距為3.54 nm,DNA雙螺旋結構的直徑為2. 37 nm。從外觀上,DNA雙螺旋結構的表面存在一個大溝(major groove)和一個小溝( minor groove),大溝是蛋白質識別DNA鹼基序列發生相互作用的基礎。
(5) DNA雙螺旋結構的穩定主要依靠鹼基對之間的氫鍵和鹼基平面的疏水堆積力共同維持。相鄰的兩個鹼基對平面在旋進過程中會彼此重疊( overlapping),由此產生了疏水性的鹼基堆積力( base stacking interaction)。這種鹼基堆積力和互補鏈之間鹼基對的氫鍵共同維繫著DNA雙螺旋結構的穩定,並且前者的作用更為重要。
一些特定的DNA序列會導致DNA分子形成特殊的空間結構,繼而影響DNA的功能和代謝。例如連續出現的6個腺苷酸會導致DNA發生約18的彎曲,這種彎曲可能在DNA與蛋白質的結合中具有一定功能。當一條單鏈DNA的序列出現了局部的反向互補時,該單鏈DNA可以回折構成髮夾結構。當DNA分子的兩條鏈上同時出現這種局部的反向互補序列時,可以形成“十”字形結構。

DNA二級結構
某些特殊情況下,DNA還能形成三鏈或者四鏈的結構。至今發現的三雙螺旋結構鏈DNA可分為兩大類,即三股螺旋結構和我國科學家白春禮等1990年用掃描隧道電子顯微鏡技術觀察到的三股髮辮結構。三股螺旋結構是在DNA雙螺旋結構的基礎上形成的,區域內的3條鏈的鹼基均為整段嘌呤或嘧啶,形成Pu - Pu - Py和Py - Pu - Py兩型(Pu代表嘌呤鏈,Py代表嘧啶鏈)。其中最常見的是Py - Pu - Py型,它的3條鏈中有2條為正常的雙螺旋,第3條嘧啶鏈位於雙螺旋的大溝中,與嘌呤鏈的方向一致,並隨雙螺旋結構一起旋轉。而第3條鏈既可來源於分子內,也可來源於分子間。例如在低pH值條件下,含(TC)n或(AG)n並形成鏡像重複序列的雙鏈DNA拆開后產生的多聚嘧啶鏈發生回折,並嵌入剩下的雙鏈DNA大溝中形成分子內的三鏈DNA。三鏈中鹼基配對的方式與雙螺旋DNA相同,即其鹼基仍以A-T、G≡C配對,但第3鏈上的胞嘧啶的N-3必須發生質子化,與C≡G中的鳥嘌呤的N-7形成新的氫鍵,同時胞嘧啶的N-4的氫原子可與鳥嘌呤中的O-6形成氫鍵,這樣就形成了C≡G·C的三鏈結構,其中C≡G之間是Watson-Crick氫鍵,而G·C被稱為Hoogsteen氫鍵或者Hoogsteen配對。同理也可以形成T=A·T的三鏈結構。
四鏈DNA的基本結構單位是G四聯體(G tetraplex),即由4個鳥嘌呤通過8個Hoogsteen氫鍵相互連接為一個四角形,再堆積形成分子內或分子間的右手螺旋。四鏈中DNA鏈的方向可以為同向,也可以為反向。真核生物DNA線性分子3'-末端富含GT序列的端粒可形成G四鏈體結構。
Watson和Crick提出的DNA雙螺旋結構模型被稱為B- DNA或B型DNA,是基於與細胞內相似的溫度環境中進行X線衍射所得的分析結果。這是DNA在水性環境下和生理條件下最穩定和最普遍的結構形式。但這種結構不是一成不變的,溶液的離子強度或相對濕度的變化可以使DNA雙螺旋結構的溝槽、螺距、旋轉角度等發生變化。例如降低環境的相對濕度,B型DNA會發生可逆性的構象改變,被稱為A型DNA。儘管兩型都為右手螺旋,但A型DNA較粗,每兩個相鄰鹼基對平面之間的距離為0. 26 nm,每圈螺旋結構含有11個鹼基對,雙螺旋結構的直徑為2. 55 nm,而且比B型DNA的剛性強。1979年,美國科學家A·Rich等在研究人工合成的CGCGCG晶體結構時,發現這種DNA具有左手螺旋(left-handed helix)的結構特徵。後來證明這種結構在天然DNA分子中同樣存在,並稱為Z型DNA。不同結構的DNA在功能上可能有所差異,與基因表達的調節和控制相適應。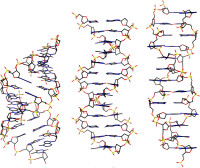

DNA二級結構
