熱化學方程式
表示物質變化和焓變的方程式
熱化學方程式(thermochemical equation)是用以表示化學反應中的能量變化和物質變化。熱化學方程式的意義為熱化學方程式不僅表明了一個反應中的反應物和生成物,還表明了一定量物質在反應中所放出或吸收的熱量。
熱化學方程式是表示化學反應中的物質變化和焓變(或能量變化;熱量變化)。
例如,熱化學方程式: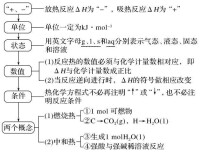

熱化學方程式
方程的意義是在標準態時,完全反應生成,反應放熱。
書寫和應用熱化學方程式時必須注意以下幾點:
(1)反應熱與溫度和壓強等測定條件有關,所以書寫時指明反應時的溫度和壓強,若是標準狀態下,即溫度為、氣壓為時,可以不註明。
(2)各物質化學式右側用圓括弧()表明物質的聚集狀態。可以用g、l、s分別代表氣態、液態、固態。固體有不同晶態(同素異形體)時,還需將晶態(形)註明,例如S(斜方),S(單斜);C(石墨),C(金剛石)等。溶液中的反應物質,則須註明其濃度,以aq代表水溶液,(aq,∞) 代表無限稀釋水溶液。
(5)熱化學方程式是表示反應已完成的數量。由於△H與反應完成物質的量有關,所以方程式中化學式前面的化學計量數必須與△H相對應,當反應逆向進行時,其反應熱與正反應的反應熱數值相等,符號相反。
(6)不標註氣體上升符號和沉澱符號,即“↑”或“↓”。
(7)熱化學方程式無需書寫如△(加熱)和催化劑的反應條件。
(8)即使是有機熱化學方程式或可逆反應也用等號“=”,不用箭頭和可逆符號“→”,“⇌”。
(9)反應熱可分為多種,如燃燒熱、中和熱、溶解熱等,在時,(舊的標準態壓力為,即1標準大氣壓,新的標準態壓力改為。1 mol純物質完全燃燒生成穩定的化合物時所放出的熱量,叫做該物質的燃燒熱.單位為kJ/mol
(10)在稀溶液中,酸跟鹼發生中和反應生成1mol水時的反應熱叫中和熱。書寫中和熱的化學方程式應以生成1mol水為基準。
(11)同一化學反應,隨著化學計量數改變△H的值而改變。若化學計量數相同,當反應物、生成物狀態不同時,的值也不同。
(12)的意義是在標準狀態下,下標r表示反應(reaction),m反應進度為,上標Θ表示標準狀態

熱化學方程式
