晶體
有明確衍射圖案的固體
晶體(crystal)是由大量微觀物質單位(原子、離子、分子等)按一定規則有序排列的結構,因此可以從結構單位的大小來研究判斷排列規則和晶體形態。
(1)自然凝結的、不受外界干擾而形成的晶體擁有整齊規則的幾何外形,即晶體的自范性。

晶體
(3)單晶體有各向異性的特點。
(4)晶體可以使X光發生有規律的衍射。
宏觀上能否產生X光衍射現象,是實驗上判定某物質是不是晶體的主要方法。
(5)晶體相對應的晶面角相等,稱為晶面角守恆。
晶體按其結構粒子和作用力的不同可分為四類:離 子晶體、原子晶體、分子晶體和金屬晶體。
固體可分為晶體、非晶體和准晶體三大類。
具有整齊規則的幾何外形、固定熔點和各向異性的固態物質,是物質存在的一種基本形式。固態物質是否為晶體,一般可由X射線衍射法予以鑒定。
晶體內部結構中的質點(原子、離子、分子、原子團)有規則地在三維空間呈周期性重複排列,組成一定形式的晶格,外形上表現為一定形狀的幾何多面體。組成某種幾何多面體的平面稱為晶面,由於生長的條件不同,晶體在外形上可能有些歪斜,但同種晶體晶面間夾角(晶面角)是一定的,稱為晶面角不變原理。

合成鉍單晶
晶體通常呈現規則的幾何形狀,就像有人特意加工出來的一樣。其內部原子的排列十分規整嚴格,比士兵的方陣還要整齊得多。如果把晶體中任意一個原子沿某一方向平移一定距離,必能找到一個同樣的原子。而玻璃、珍珠、瀝青、塑料等非晶體,內部原子的排列則是雜亂無章的。准晶體是發現的一類新物質,其內部排列既不同於晶體,也不同於非晶體。

晶體
但僅從外觀上,用肉眼很難區分晶體、非晶體與准晶體。那麼,如何才能快速鑒定出它們呢?一種最常用的技術是X光技術。用X光對固體進行結構分析,你很快就會發現,晶體和非晶體、准晶體是截然不同的三類固體。
為了描述晶體的結構,我們把構成晶體的原子當成一個點,再用假想的線段將這些代表原子的各點連接起來,就繪成了像圖中所表示的格架式空間結構。這種用來描述原子在晶體中排列的幾何空間格架,稱為晶格。由於晶體中原子的排列是有規律的,可以從晶格中拿出一個完全能夠表達晶格結構的最小單元,這個最小單元就叫作晶胞。許多取向相同的晶胞組成晶粒,由取向不同的晶粒組成的物體,叫做多晶體,而單晶體內所有的晶胞取向完全一致,常見的單晶如單晶硅、單晶石英。大家最常見到的一般是多晶體。
由於物質內部原子排列的明顯差異,導致了晶體與非晶體物理化學性質的巨大差異。例如,晶體有固定的熔點,當溫度高到某一溫度便立即熔化;而玻璃及其它非晶體則沒有固定的熔點,從軟化到熔化是一個較大的溫度範圍。
類別實例
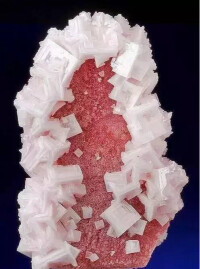
1.立方晶系:鑽石 明礬 金鐵鉛
晶體
3.斜方晶系:硫 碘 硝酸銀
4.單斜晶系:硼砂蔗糖石膏
5.三斜晶系:硫酸銅 硼酸
6.三方(菱形)晶系:砷 水晶 冰 石墨
7.六方晶系:鎂 鋅 鈹 鎘 鈣

晶體
1. 長程有序:晶體內部原子在至少在微米級範圍內的規則排列。
2. 均勻性:晶體內部各個部分的宏觀性質是相同的。
3. 各向異性:晶體中不同的方向上具有不同的物理性質。
4 .對稱性:晶體的理想外形和晶體內部結構都具有特定的對稱性。
5. 自限性:晶體具有自發地形成封閉幾何多面體的特性。
6. 解理性:晶體具有沿某些確定方位的 晶面劈裂的性質。
7. 最小內能:成型晶體內能最小。
8. 晶面角守恆:屬於同種晶體的兩個對應晶面之間的夾角恆定不變。
具體介紹:
均一性和異向性
因為晶體是具有格子構造的固體,同一晶體的各個部分質點分佈是相同的,所以同一晶體的各個部分的性質是相同的,此即晶體的均一性;同一晶體格子中,在不同的方向上質點的排列一般是不相同的,晶體的性質也隨方向的不同而有所差異,此即晶體的異向性。
最小內能與穩定性

晶體
對稱性
晶體的對稱表現在晶體中相等的晶面,晶棱和角頂有規律的重複出現。這是由於它具有規律的格子構造。是其在三維空間周期性重複的體現。既晶體的對稱性不僅表現在外部形態上,而且其內部構造也同樣也是對稱的。
在晶體的外形以及其他宏觀表現中還反映了晶體結構的對稱性。晶體的理想外形或其結構都是對稱圖象。這類圖象都能經過不改變其中任何兩點間距離的操作後復原。這樣的操作稱為對稱操作,平移、旋轉、反映和倒反都是對稱操作。能使一個圖象復原的全部不等同操作,形成一個對稱操作群。

鎵, 一種很容易結成大塊單晶的金屬
(1)晶體結構中只能存在1、2、3、4和6次對稱軸,
(2)空間點陣只能有14種形式。n次對稱軸的基本旋轉操作為旋轉360°/n,因此,晶體能在外形和宏觀中反映出來的軸對稱性也只限於這些軸次。

晶體
晶體的一些性質取決於將分子聯結成固體的結合力。這些力通常涉及原子或分子的最外層的電子(或稱價電子)的相互作用。如果結合力強,晶體有較高的熔點。如果它們稍弱一些,晶體將有較低的熔點,也可能較易彎曲和變形。如果它們很弱,晶體只能在很低溫度下形成,此時分子可利用的能量不多。
有四種主要的晶體鍵。離子晶體由正離子和負離子構成,靠不同電荷之間的引力(離子鍵)結合在一起。氯化鈉是離子晶體的一例。原子晶體(共價晶體)的原子或分子共享它們的價電子(共價鍵)。鑽石、鍺和硅是重要的共價晶體。金屬晶體是金屬的原子變為離子,被自由的價電子所包圍,它們能夠容易地從一個原子運動到另一個原子,可形象的描述為沉浸在自由電子的海洋里(金屬鍵)。當這些電子全在同一方向運動時,它們的運動稱為電流。分子晶體的分子完全不分享它們的電子。它們的結合是由於從分子的一端到另一端電場有微小的變動。因為這個結合力很弱(范德華力和氫鍵),這些晶體在很低的溫度下就熔化,且硬度極低。典型的分子結晶如固態氧和冰。
在離子晶體中,電子從一個原子轉移到另一個原子。共價晶體的原子分享它們的價電子。金屬原子的一端有少量的負電荷,另一端有少量的正電荷。一個弱的電引力使分子就位。
用來製作工業用的晶體的技術之一,是從熔液中生長。籽晶可用來促進單晶體的形成。在這個工序里,籽晶降落到裝有熔融物質的容器中。籽晶周圍的熔液冷卻,它的分子就依附在籽晶上。這些新的晶體分子承接籽晶的取向,形成了一個大的單晶體。藍寶石和紅寶石的基本成分是氧化鋁,它的熔點高,製成一個盛裝它的熔液的容器是困難的。人工合成藍寶石和紅寶石是用維爾納葉法(焰熔法)製成,即將氧化鋁粉和少量上色用的鈦、鐵或鉻粉,通過火焰下滴到籽晶上。火焰將粉熔解,然後在籽晶上重新結晶。
生長人造鑽石需要高於1600℃的溫度和60000倍大氣壓。人造鑽石砂粒小且黑,它們適宜工業應用。區域熔化過程用來純化半導體工業中的硅晶體。一個單晶體垂直懸掛在硅棒的頂端上。在兩者接觸處加熱,棒的頂端熔化,並在單晶體上重結晶,然後將加熱處慢慢地沿棒下移。
晶體缺陷各種偏離晶體結構中質點周期重複排列的因素,嚴格說,造成晶體點陣結構周期勢場畸變的一切因素。
如晶體中進入了一些雜質。這些雜質也會佔據一定的位置,這樣破壞了原質點排列的周期性,在二十世紀中期,發現晶體中缺陷的存在,它嚴重影響晶體性質,有些是決定性的,如半導體導電性質,幾乎完全是由外來雜質原子和缺陷存在決定的,許多離子晶體的顏色、發光等。另外,固體的強度,陶瓷、耐火材料的燒結和固相反應等等均與缺陷有關,晶體缺陷是近三、四年國內外科學研究十分注意的一個內容。
根據缺陷的作用範圍把真實晶體缺陷分四類:
點缺陷:在三維尺寸均很小,只在某些位置發生,隻影響鄰近幾個原子。
線缺陷:在二維尺寸小,在另一維尺寸大,可被電鏡觀察到。
面缺陷:在一維尺寸小,在另二維尺寸大,可被光學顯微鏡觀察到。
體缺陷:在三維尺寸較大,如鑲嵌塊,沉澱相,空洞,氣泡等。
按形成的原因不同分三類:
1熱缺陷(晶格位置缺陷)
在晶體點陣的正常格點位出現空位,不該有質點的位置出現了質點(間隙質點)。
2 組成缺陷
外來質點(雜質)取代正常質點位置或進入正常結點的間隙位置。
3 電荷缺陷
晶體中某些質點個別電子處於激髮狀態,有的離開原來質點,形成自由電子,在原來電子軌道上留下了電子空穴。
符號及反應方程式
1. 缺陷符號及缺陷反應方程式
缺陷符號 以二元化合物MX為例
(1)晶格空位:正常結點位沒有質點,VM,VX
(2)間隙離子:除正常結點位置外的位置出現了質點,Mi ,Xx
(3)錯位離子:M排列在X位置,或X排列在M位置上,若處在正常結點位置上,則MM,XX
(4)取代離子:外來雜質L進入晶體中,若取代M,則LM,若取代X,則LX,若佔據間隙位,則Li。

晶體
(5)電子空穴 h·(代表存在一個正電荷),·表示有效正電荷
如:從NaCl晶體中取走一個Na+,留下一個空位造成電價不平衡,多出負一價。相當於取走Na原子加一個負有效負電荷,e失去→自由電子,剩下位置為電子空穴h·
(7)複合缺陷
同時出現正負離子空位時,形成複合缺陷,雙空位。
VM+VX→(VM- VX)
缺陷反應方程式
必須遵守三個原則
(1)位置平衡——反應前後位置數不變(相對物質位置而言)
(2)質點平衡——反應前後質量不變(相對加入物質而言)
(3)電價平衡——反應前後呈電中性
例:將CaCl2引入KCl中:
將CaO引入ZrO2中
注意:只從缺陷反應方程看,只要符合三個平衡就是對的,但實際上往往只有一種是對的,這要知道其它條件才能確定哪個缺陷反應是正確的。
確定(1)式密度增加,要根據具體實驗和計算。
(晶格位置缺陷)
只要晶體的溫度高於絕對零度,原子就要吸收熱能而運動,但由於固體質點是牢固結合在一起的,或者說晶體中每一個質點的運動必然受到周圍質點結合力的限制而只能以質點的平衡位置為中心作微小運動,振動的幅度隨溫度升高而增大,溫度越高,平均熱能越大,而相應一定溫度的熱能是指原子的平均動能,當某些質點大於平均動能就要離開平衡位置,在原來的位置上留下一個空位而形成缺陷,實際上在任何溫度下總有少數質點擺脫周圍離子的束縛而離開原來的平衡位置,這種由於熱運動而產生的點缺陷——熱缺陷。
熱缺陷兩種基本形式:
a-弗侖克爾缺陷,
b-肖特基缺陷
(1)弗侖克爾缺陷
具有足夠大能量的原子(離子)離開平衡位置后,擠入晶格間隙中,形成間隙原子離子),在原來位置上留下空位。
特點:空位與間隙粒子成對出現,數量相等,晶體體積不發生變化。
在晶體中弗侖克爾缺陷的數目多少與晶體結構有很大關係,格點位質點要進入間隙位,間隙必須要足夠大,如螢石(CaF2)型結構的物質空隙較大,易形成,而NaCl型結構不易形成。總的來說,離子晶體,共價晶體形成該缺陷困難。
(2)肖特基缺陷
表面層原子獲得較大能量,離開原來格點位跑到表面外新的格點位,原來位置形成空位這樣晶格深處的原子就依次填入,結果表面上的空位逐漸轉移到內部去。
特點:體積增大,對離子晶體、正負離子空位成對出現,數量相等。結構緻密易形成肖特基缺陷。
晶體熱缺陷的存在對晶體性質及一系列物理化學過程,導電、擴散、固相反應、燒結等產生重要影響,適當提高溫度,可提高缺陷濃度,有利於擴散,燒結作用,外加少量填加劑也可提高熱缺陷濃度,有些過程需要最大限度避免缺陷產生,如單晶生產,要非常快冷卻。
3. 組成缺陷
主要是一種雜質缺陷,在原晶體結構中進入了雜質原子,它與固有原子性質不同,破壞了原子排列的周期性,雜質原子在晶體中佔據兩種位置(1)填隙位(2)格點位
4. 電荷缺陷(Charge defect)
從物理學中固體的能帶理論來看,非金屬固體具有價帶,禁帶和導帶,當在OR時,導帶全部完善,價帶全部被電子填滿,由於熱能作用或其它能量傳遞過程,價帶中電子得到一能量Eg,而被激發入導帶,這時在導帶中存在一個電子,在價帶留一孔穴,孔穴也可以導電,這樣雖末破壞原子排列的周期性,在由於孔穴和電子分別帶有正負電荷,在它們附近形成一個附加電場,引起周期勢場畸變,造成晶體不完整性稱電荷缺陷。
例:純半導體禁帶較寬,價電帶電子很難越過禁帶進入導帶,導電率很低,為改善導電性,可採用摻加雜質的辦法,如在半導體硅中摻入P和B,摻入一個P,則與周圍Si原子形成四對共價鍵,並導出一個電子,叫施主型雜質,這個多餘電子處於半束縛狀態,只須填加很少能量,就能躍遷到導帶中,它的能量狀態是在禁帶上部靠近導帶下部的一個附加能級上,叫施主能級,叫n型半導體。當摻入一個B,少一個電子,不得不向其它Si原子奪取一個電子補充,這就在Si原子中造成空穴,叫受主型雜質,這個空穴也僅增加一點能量就能把價帶中電子吸過來,它的能量狀態在禁帶下部靠近價帶頂部一個附加能級,叫受主能級,叫P型半導體,自由電子,空穴都是晶體一種缺
點缺陷在實踐中有重要意義:燒成燒結,固相反應,擴散,對半導體,電絕緣用陶瓷有重要意義,使晶體著色等。
線缺陷
實際晶體在結晶時,受到雜質,溫度變化或振動產生的應力作用或晶體由於受到打擊,切割等機械應力作用,使晶體內部質點排列變形,原子行列間相互滑移,不再符合理想晶體的有序排列,形成線狀缺陷。
位錯直觀定義:晶體中已滑移面與未滑移面的邊界線。
這種線缺陷又稱位錯,注意:位錯不是一條幾何線,而是一個有一定寬度的管道,位錯區域質點排列嚴重畸變,有時造成晶體面網發生錯動。對晶體強度有很大影響。
位錯主要有兩種:刃型位錯和螺型位錯。
其形式可以設想為:在一完整晶體,沿BCEF晶面橫切一刀,從BCAD,將ABCD面上半部分,作用以壓力δ,使之產生滑移,距離(柏氏矢量晶格常數或數倍)滑移面BCEF,滑移區ABCD,未滑移區ADEF,AD為已滑移區交界線—位錯線。
正面看簡圖:如上圖
滑移上部多出半個原子面,就象刀刃一樣(劈木材)稱刃型位錯。
特點:滑移方向與位錯線垂直,符號⊥,有多餘半片原子面。
其形成可設想為:在一完整晶體,沿ABCD晶面橫切一刀,在ABCD面上部分沿X方向施一力δ,使其生產滑移,滑移區ABCD未滑移區ADEF,交界線AD(位錯線)
特點:滑移方向與位錯線平行,與位錯線垂直的面不是平面,呈螺施狀,稱螺型位錯。
刃型位錯與螺型位錯
a-正常面網,
b-刃型位錯,
c-螺型位錯
主要從各自特點區別
刃型:滑移方向與位錯線垂直,多半個原子面,位錯線可為曲線。
螺型:滑移方向與位錯線平行,呈螺旋狀,位錯線直線。
由於位錯的存在對晶體的生長,雜質在晶體中的擴散,晶體內鑲嵌結構的形成及晶體的高溫蠕變性等一系列性質和過程都有重要影響。
晶體位錯的研究方法:通常用光學顯微鏡,X光衍射電子衍射和電子顯微鏡等技術進行直接觀察和間接測定。
位錯具有以下基本性質:
(1)位錯是晶體中原子排列的線缺陷,不是幾何意義的線,是有一定尺度的管道。
(2)形變滑移是位錯運動的結果,並不是說位錯是由形變產生的,因為一塊生長很完事的晶體中,本身就存在很多位錯。
(3)位錯線可以終止在晶體的表面(或多晶體的晶界上),但不能終止在一個完事的晶體內部。
(4)在位錯線附近有很大應力集中,附近原子能量較高,易運動。
面缺陷
涉及較大範圍(二維方向)、晶界、晶面、堆垛層錯。
由於晶體表面處的離子或原子具有不飽和鍵,有很大反應活性,表面結構出現不對稱性,使點陣受到很大彎曲變形,因而能量比內部能量高,是一種缺陷。
(1)小角度晶界(鑲嵌塊)
尺寸在10-6-10-8m的小晶塊,彼此間以幾秒到的微小( )角度傾斜相交,形成鑲嵌結構,有人認為是棱位錯,由於晶粒以微小角度相交,可以認為合併在一起,在晶界面是形成了一系列刃型位錯。
(2)大角度晶界,各晶面取向互不相同,交角較大,在多晶體中,晶體可能出現大角度晶界。在這種晶界中,頂點排列接近無序狀態,晶界處是缺陷位置,所以能量較高,可吸附外來質點。晶界是原子或離子擴散的快速通道,也是空位消除的地方,這種特殊作用對固相反應,燒結起重要作用,對陶瓷、耐火材料等多晶材料性能如蠕變、強度等力學性能和極化、損耗等介電性能影響較大。
離子堆垛過程中發生了層次錯動,出現堆垛層錯,如面心立方堆積形式為ABCABCA……→ABCACBABC中間的B層和C層發生了層次錯動,出現缺陷(一般了解)
非化學計量化合物
定義:化合物中各元素的原子數之比不是簡單的整數而出現了分數,如Fe1-xO,Cu2-xO,Co1-xO等。
可偏離化合式的化合物
在基礎化學中學到的化合物的分子式都是符合定比定律的,即元素的原子數之比為簡單整數比,如FeO,Fe/O=1/1,TiO2, Ti/O=1/2等
非化學計量化合物缺陷
(1)陽離子過剩,形成陰離子空位
TiO2,ZrO2會產生這種缺陷,分子式為TiO2-x, ZrO2-x,從化學計量觀念,正負離子比為1:2,由於揣氧不足,在晶體中存在氧空位,而變為非化學計量化合物。從化學觀念看,缺氧TiO2可以看作是四價鈦和三價鈦氧化物的固體溶液,即Ti2O3在TiO2中的固溶體,或從電中性考慮,Ti由四價→三價,原因:Ti4+獲得一個電子→Ti3+,所獲得的電了是由於氧不足脫離。正常TiO2晶格結點放出的,在電場作用下,這一電子可以一個鈦離子位置遷移到另一個鈦離子位置,並非固定在某一鈦離子上,從而形成電子電導,具有這種缺陷的材料稱n型半導體。這種非化學計量化合物缺陷方程可寫成:例:在還原氣氛下TiO2→TiO2-x
(2)也可看成部分O由晶格逸出變成氣體
可見:這種非化學計量化合物的形成多是由變價正離子構成的氧化物,由高價變為低價,形成負離子空位,還有ThO2,CeO2等,與氣氛有關。
陽離子過剩
形成間隙陽離子
如ZnO、CdO→Zn1+xo,Cd1+xO,過剩的金屬離子進入間隙位,為保持電中性,等價電子被束縛在間隙位的金屬離子周圍。例:ZnO在鋅蒸氣中加熱,顏色逐漸加深變化。
負電子過剩
形成間隙負離子。
發現UO2+X,可以看作U3O8在UO2中的固溶體,當負離子過剩進入間隙位置時,結構中必須出現兩個電子空穴,以平衡整體電中性,相應正離子電價升高,電子空穴在電場作用下產生運動,這種材料稱P型半導體。
形成正離子空位
由於存在正離子空位,為保持電中性,在正離子空位周圍捕獲電子空位,因此其也是P型半導體,如Cu2O、FeO即是。例:FeO在氧氣下形成這種缺陷,實際上是Fe2O3在FeO中形成的固溶體(高價取代低價),即2個Fe3+取代3個Fe2+,同時在晶格中形成個正離子空位,在氧氣條件下,氧氣進入FeO晶格結構中,變為氧離子,必須從鐵離子獲得兩個電子,使Fe2+→Fe3+,並形成VFe。
可見,非化學計量化合物缺陷的形成主要受氣氛影響,也與溫度有關,嚴格說,世界上所有化合物都是非化學計量的,只是程度不同而已。
結晶分兩種,一種是降溫結晶,另一種是蒸髮結晶。降溫結晶:首先加熱溶液,蒸發溶劑成飽和溶液,此時降低熱飽和溶液的溫度,溶解度隨溫度變化較大的溶質就會呈晶體析出,叫降溫結晶。
蒸髮結晶:蒸發溶劑,使溶液由不飽和變為飽和,繼續蒸發,過剩的溶質就會呈晶體析出,叫蒸髮結晶。
石英、雲母、明礬、食鹽、硫酸銅、味精
