碲化鈉
碲化鈉
碲化鈉是一種無機化合物,由碲和鈉組成,屬於氫碲酸鹽,其化學式為Na₂Te。
碲化鈉結構像許多相關化合物其化學式為MX,例如:氧化鈉、硫化鈉、硒化鈉、釙化鈉、硫化鉀、硫化銣、硫化銫、碲化鋰等,都是反螢石結構,因此,在碲化鈉結晶每個Te離子周圍有八個鈉離子,每個鈉離子周圍有四個Te離子。
當其遇到水、潮濕的空氣、或醇類,碲化鈉將分解:
正因為如此反應,許多過程歸結為碲化鈉可能涉及碲氫化鈉NaHTe這是比較容易溶解和形成的物質。
作為有機合成試劑
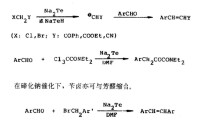
在有機合成中被使用,它既是一種試劑減排和作為源特在合成化合物的有機碲芳基鹵化物對二芳基取代碲化物,如下所示的合成雙萘基碲:
製備碲化銅與碲化鋅
碲化鈉與硫酸銅可以製備碲化銅。
在縮合反應中作為催化劑
在碲化鈉或碲氫化鈉催化下,α-鹵代酮、α-鹵代酯、和α-鹵代腈均可與芳醛順利縮合,生成相應的α、β-不飽和化合物。反應機理是碲化鈉或碲氫化鈉首先進行奪鹵反應,從而生成相應的碳負離子,後者進一步與芳醛縮合。
碲化鈉
通常用碲和鈉發生反應生成碲化鈉,通常在隔絕空氣與濕氣條件下在液氨中進行。
實驗性夠給予吞入碲的化合物,在7-24小時大部分由尿液排出,注射碲鹽后與第一小時排泄最多,24小時中逐漸減少,6天後可排出總量的23.4%,膽汁中的碲含量發現高於血液而低於腎臟排泄量。
有記載檢查接觸碲化合物的空氣濃度為0.00001-0.00005毫克/升,2年左右的工人,尿路中都有發現碲,含量達到0.06毫克/升。碲於尿中含量為0.01毫克/升時,工人即感到口中有金屬氣味。據有的資料報告,接觸碲-銅合金工業工人的碲中毒3例中尿液碲含量為0.008-0.016毫克/升。