D-青黴胺
D-青黴胺
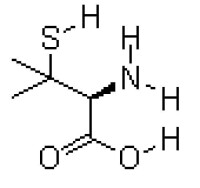
分子結構
英文名稱:D(-)-Penicillamine
英文別名 3,3-Dimethyl-D-cysteine~3-Mercapto-D-valine; D-(-)-Penicillamine; D-minus-penicillamine free base; H-D-Pen-OH; Penicilllamine; 3,3-Dimethyl-D(-)-cysteine
中文別名:青黴胺;二甲基半胱胺酸;D-(-)-青黴胺
CAS RN:52-67-5
EINECS號:200-148-8
分 子 式:C5H11NO2S
分 子 量:149.2113
安全術語:S24/25;
用 途:解毒藥,
S24/25Avoid contact with skin and eyes.
避免與皮膚和眼睛接觸。
熔點 212 ºC
比旋光度 -65 º (C=5, 1M NAOH, ON DRY)
水溶性 11.1 G/100 ML (20 ºC)
【藥物名稱】D-青黴胺
【英文名】Penicillamine
其他名稱:二甲基半胱氨酸鹽酸鹽 青黴胺
主要成分:半胱氨酸。
性狀:片劑。
功能主治:青黴胺用於類風濕性關節炎、慢性活動性肝炎、硬皮病、口眼乾燥、關節炎綜合征等自身免疫性疾病,可見有明顯的療效。對類風濕性關節炎,可減輕關節疼痛、腫脹及滲液情況,晨起關節僵硬、血沈率等臨床癥狀明顯改善,一般需經數周方可顯效,過早停葯易於複發。可使慢性活動性肝炎病人轉氨酶下降或轉為正常。用於治療硬皮病,可使皮膚膠原交叉聯結減少,張力增加。
用法及用量:口服:用於自身免疫性疾病,每日0.8~1.8g,分3~4次服,可連服6個月。
不良反應和注意:1.可有皮膚瘙癢、皮疹、食欲不振、噁心、嘔吐、味覺減退、白細胞及血小板減少、蛋白尿、肌無力等。2.偶見有轉氨酶升高。妊娠婦女大量用藥后可引起胎兒發育異常。
規格:片劑:每片100mg。
是否醫保用藥:非醫保
是否非處方葯:處方
【類別】免疫抑製劑
| 文獻、期刊報道的毒性作用試驗數據 | |||||
|---|---|---|---|---|---|
| 編號 | 毒性類型 | 測試方法 | 測試對象 | 使用劑量 | 毒性作用 |
| 1 | 急性毒性 | 未報告 | 成年男性 | 3200 mg/kg/84W-I | 1.嗅覺毒性——未報告 2.皮膚和附件毒性——皮炎(全身暴露后) |
| 2 | 急性毒性 | 口服 | 成年女性 | 900 mg/kg/26W-I | 1.皮膚和附件毒性——皮炎(全身暴露后) |
| 3 | 急性毒性 | 口服 | 成年女性 | 650 mg/kg/81W-I | 1.行為毒性——肌肉無力 2.骨骼肌毒性——其他變化 |
| 4 | 急性毒性 | 口服 | 成年女性 | 112 mg/kg/1W-I | 1.血液毒性——粒細胞缺乏症 2.皮膚和附件毒性——皮炎(全身暴露后) 3.營養和代謝系統毒性——體溫升高 |
| 5 | 急性毒性 | 口服 | 成年女性 | 105 mg/kg/6W-I | 1.皮膚和附件毒性——皮炎(全身暴露后) |
| 6 | 急性毒性 | 口服 | 成年男性 | 400 mg/kg/4W-I | 1.肺部、胸部或者呼吸毒性——其他變化 2.血液毒性——出血 |
| 7 | 急性毒性 | 口服 | 成年女性 | 150 mg/kg/30D-I | 1.行為毒性——肌肉無力 2.心臟毒性——心律失常 3.胃腸道毒性——運動過度、腹瀉 |
| 8 | 急性毒性 | 口服 | 人類 | 21 mg/kg/D | 1.腎、輸尿管和膀胱毒性——出現蛋白尿 2.血液毒性——白細胞減少 3.血液毒性——血小板減少 |
| 9 | 急性毒性 | 口服 | 人類 | 893 mg/kg/30W-I | 1.行為毒性——肌肉無力 2.肺部、胸部或者呼吸毒性——呼吸困難 3.骨骼肌毒性——其他變化 |
| 10 | 急性毒性 | 口服 | 兒童 | 40 mg/kg/1W-I | 1.血液毒性——白細胞減少 2.皮膚和附件毒性——皮炎(全身暴露后) 3.營養和代謝系統毒性——體溫升高 |
| 11 | 急性毒性 | 口服 | 成年男性 | 482 mg/kg/19W-I | 1.血液毒性——血小板減少 2.皮膚和附件毒性——皮炎(全身暴露后) |
| 12 | 急性毒性 | 口服 | 大鼠 | 6170 mg/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 13 | 急性毒性 | 腹腔注射 | 大鼠 | 2080 mg/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 14 | 急性毒性 | 皮下注射 | 大鼠 | 4020 mg/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 15 | 急性毒性 | 靜脈注射 | 大鼠 | 2 mg/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 16 | 急性毒性 | 口服 | 小鼠 | 720 mg/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 17 | 急性毒性 | 腹腔注射 | 小鼠 | 298 mg/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 18 | 急性毒性 | 皮下注射 | 小鼠 | 3810 mg/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 19 | 急性毒性 | 靜脈注射 | 小鼠 | 3840 mg/kg | 1.肺部、胸部或者呼吸毒性——呼吸困難 |
| 20 | 慢性毒性 | 口服 | 大鼠 | 4480 mg/kg/3W-I | 1.肝毒性——其他變化 2.腎、輸尿管和膀胱毒性——其他變化 |
| 21 | 慢性毒性 | 口服 | 大鼠 | 23400 mg/kg/26W-I | 1.腎、輸尿管和膀胱毒性——尿中成分發生變化 2.血液毒性——正細胞性貧血 3.血液毒性——血清成分發生變化(如TP、膽紅素、膽固醇) |
| 22 | 慢性毒性 | 口服 | 小鼠 | 40320 mg/kg/12W-C | 1.脊髓神經毒性——其他脊髓退行性改變 2.自主神經毒性——交感神經出現問題 3.營養和代謝系統毒性——金屬離子濃度發生變化 |
| 23 | 突變毒性 | 鼠傷寒沙門氏菌 | 20 umol/plate | ||
| 24 | 突變毒性 | 鼠傷寒沙門氏菌 | 1 mg/plate | ||
| 25 | 突變毒性 | 人類淋巴細胞 | 2 gm/L | ||
| 26 | 突變毒性 | 人類淋巴細胞 | 400 mg/L | ||
| 27 | 突變毒性 | 倉鼠肺 | 8 gm/L | ||
| 28 | 突變毒性 | 倉鼠肺 | 1 gm/L | ||
| 29 | 致癌性 | 口服 | 兒童 | 122 mg/kg/3Y-C | 1.致癌性——致癌(根據RTECS標準) 2.血液毒性——白血病 |
| 30 | 致癌性 | 腹腔注射 | 小鼠 | 2 mg/kg/4W-I | 1.致癌性——可能致癌(根據RTECS標準) 2.血液毒性——白血病 3.血液毒性——淋巴瘤,包括霍奇金病 |
| 31 | 生殖毒性 | 未報告 | 成年女性 | 6480 mg/kg,雌性受孕 1-39 周后 | 1.生殖毒性——顱骨和面部發育異常(包括鼻/舌) 2.生殖毒性——皮膚和皮膚附件發育異常 3.生殖毒性——對新生兒有影響 |
| 32 | 生殖毒性 | 口服 | 大鼠 | 9130 mg/kg,雌性受孕 1-22 天后 | 1.生殖毒性——影響胎兒 |
| 33 | 生殖毒性 | 口服 | 大鼠 | 1870 mg/kg,雌性受孕 1-22 天后 | 1.生殖毒性——對新生兒有其他影響 |
| 34 | 生殖毒性 | 口服 | 大鼠 | 41 mg/kg,雄性配種 60 天前 | 1.生殖毒性——交配成功率下降 2.生殖毒性——胚胎植入前死亡率上升 3.生殖毒性——影響生育能力 |
| 35 | 生殖毒性 | 口服 | 大鼠 | 1750 mg/kg,雌性受孕 17-22 天后 | 1.生殖毒性——影響新生兒性別比例 |
| 36 | 生殖毒性 | 口服 | 大鼠 | 1375 mg/kg,雌性受孕 7-17 天后 | 1.生殖毒性——新生兒體重增加量減少 |
| 37 | 生殖毒性 | 口服 | 大鼠 | 9130 mg/kg,雌性受孕 1-22 天后 | 1.生殖毒性——中樞神經系統發育異常 2.生殖毒性——皮膚和皮膚附件發育異常 3.生殖毒性——肌肉骨骼系統發育異常 |
| 38 | 生殖毒性 | 口服 | 大鼠 | 8715 mg/kg,雌性受孕 1-21 天后 | 1.生殖毒性——植入后死亡率增加 2.生殖毒性——胎兒毒性(如胎兒發育不良,但不至死亡) 3.生殖毒性——呼吸系統發育異常 |
| 39 | 生殖毒性 | 腹腔注射 | 大鼠 | 5 mg/kg,雌性受孕 15-19 天后 | 1.生殖毒性——胎兒毒性(如胎兒發育不良,但不至死亡) 2.生殖毒性——肌肉骨骼系統發育異常 |
| 40 | 生殖毒性 | 口服 | 小鼠 | 20160 mg/kg,雌性受孕 1-21 天后 | 1.生殖毒性——其他變化 2.生殖毒性——對新生兒有其他影響 3.生殖毒性——影響新生兒的行為 |
| 41 | 生殖毒性 | 口服 | 小鼠 | 10080 mg/kg,雌性受孕 1-21 天后 | 1.生殖毒性——對新生兒有其他影響 |
| 42 | 生殖毒性 | 口服 | 小鼠 | 20 mg/kg,雌性受孕 10-14 天后 | 1.生殖毒性——植入后死亡率增加 2.生殖毒性——胚胎或胎兒死亡 |
| 43 | 生殖毒性 | 口服 | 小鼠 | 16 mg/kg,雌性受孕 10-14 天后 | 1.生殖毒性——顱骨和面部發育異常(包括鼻/舌) |
| 44 | 生殖毒性 | 口服 | 倉鼠 | 3200 mg/kg,雌性受孕 7 天后 | 1.生殖毒性——胎兒毒性(如胎兒發育不良,但不至死亡) 2.生殖毒性——中樞神經系統發育異常 3.生殖毒性——肌肉骨骼系統發育異常 |
| 45 | 生殖毒性 | 口服 | 倉鼠 | 4 mg/kg,雌性受孕 7 天后 | 1.生殖毒性——植入后死亡率增加 2.生殖毒性——胚胎或胎兒死亡 |
