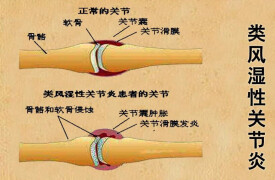
類風濕性關節炎
一種病因未明的慢性、以炎性滑膜炎為主的系統性疾病
類風濕關節炎(RA)是一種病因未明的慢性、以炎性滑膜炎為主的系統性疾病。其特徵是手、足小關節的多關節、對稱性、侵襲性關節炎症,經常伴有關節外器官受累及血清類風濕因子陽性,可以導致關節畸形及功能喪失。
1.骨關節炎
多見於中、老年人,起病過程大多緩慢。手、膝、髖及脊柱關節易受累,而掌指、腕及其他關節較少受累。病情通常隨活動而加重或因休息而減輕。晨僵時間多小於半小時。雙手受累時查體可見Heberden和Bouchard結節,膝關節可觸及摩擦感。不伴有皮下結節及血管炎等關節外表現。類風濕因子多為陰性,少數老年患者可有低滴度陽性。
2.銀屑病關節炎
銀屑病關節炎的多關節炎型和類風濕關節炎很相似。但本病患者有特徵性銀屑疹或指甲病變,或伴有銀屑病家族史。常累及遠端指間關節,早期多為非對稱性分佈,血清類風濕因子等抗體為陰性。
3.強直性脊柱炎
本病以青年男性多發,以中軸關節如骶髂及脊柱關節受累為主,雖有外周關節病變,但多表現為下肢大關節,為非對稱性的腫脹和疼痛,並常伴有棘突、大轉子、跟腱、脊肋關節等肌腱和韌帶附著點疼痛。關節外表現多為虹膜睫狀體炎、心臟傳導阻滯障礙及主動脈瓣閉鎖不全等。X線片可見骶髂關節侵襲、破壞或融合,患者類風濕因子陰性,並且多為HLA-B27抗原陽性。本病有更為明顯的家族發病傾向。
4.系統性紅斑狼瘡
本病患者在病程早期可出現雙手或腕關節的關節炎表現,但患者常伴有發熱、疲乏、口腔潰瘍、皮疹、血細胞減少、蛋白尿或抗核抗體陽性等狼瘡特異性、多系統表現,而關節炎較類風濕關節炎患者程度輕,不出現關節畸形。實驗室檢查可發現多種自身抗體。
5.反應性關節炎
本病起病急,發病前常有腸道或泌尿道感染史。以大關節(尤其下肢關節)非對稱性受累為主,一般無對稱性手指近端指間關節、腕關節等小關節受累。可伴有眼炎、尿道炎、龜頭炎及發熱等,HLA-B27可呈陽性而類風濕因子陰性,患者可出現非對稱性骶髂關節炎的X線改變。
尚未完全明確,認為RA是一種自身免疫性疾病已被普遍承認。具有HLA-DR4和DW4型抗原者,對外界環境條件、病毒、細菌、神經精神及內分泌因素的刺激具有較高的敏感性,當侵襲機體時,改變了HLA的抗原決定簇,使具有HLA的有核細胞成為免疫抑制的靶子。由於HLA基因產生可攜帶T細胞抗原受體和免疫相關抗原的特性,當外界刺激因子被巨噬細胞識別時,便產生T細胞激活及一系列免疫介質的釋放,因而產生免疫反應。
細胞間的相互作用使B細胞和漿細胞過度激活產生大量免疫球蛋白和類風濕因子(RF)的結果,導致免疫複合物形成,並沉積在滑膜組織上,同時激活補體,產生多種 過敏 毒素(C3a和C5a趨化因子)。局部由單核細胞、巨噬細胞產生的因子如IL-1、腫瘤壞死因子a、和白三烯B4,能刺激多形核白細胞移行進入滑膜。局部產生前列腺素E2的擴血管作用也能促進炎症細胞進入炎症部位,能吞噬免疫複合物及釋放溶酶體,包括中性蛋白酶和膠原酶,破壞膠原彈力纖維,使滑膜表面及關節軟骨受損。RF還可見於浸潤滑膜的漿細胞,增生的淋巴濾泡及滑膜細胞內,同時也能見到IgG-RF複合物,故即使感染因素不存在,仍能不斷產生RF,使病變反應發作成為慢性炎症。
RA滑膜的特徵是存在若干由活性淋巴細胞、巨噬細胞和其它細胞所分泌的產物,這些細胞活性物質包括多種因子:T淋巴細胞分泌出如白介素Ⅱ(IL-2)、IL-6、粒細胞-巨噬細胞刺激因子(GM-CSF)、腫瘤壞死因子a、變異生長因子β:來源於激活巨噬細胞的因子包括IL-1、腫瘤壞死因子a、IL-6、GM-CSF、巨噬細胞CSF,血小板衍生的生長因子:由滑膜中其它細胞(成纖維細胞和內長細胞)所分泌的活性物質包括IL-1、IL-6、GM-CSF和巨噬細胞CSF。這些細胞活性物質能說明類風濕性滑膜炎的許多特性,包括滑膜組織的炎症、滑膜的增生、軟骨和骨的損害,以及RA的全身表現。細胞活性物質IL-1和腫瘤壞死因子,能激活原位軟骨細胞,產生膠原酶和蛋白分解酶破壞局部軟骨。
RF包括IgG、IgA、IgM,在全身病變的發生上起重要作用,其中IgG-RF本身兼有抗原和抗體兩種結合部位,可以自身形成雙體或多體。含IgG的免疫複合物沉積於滑膜組織中,刺激滑膜產生IgM、IgA型RF。IgG-RF又可和含有IgG的免疫複合物結合,其激活補體能力較單純含IgG的免疫複合物更大。
1.一般都有輕度至中度 貧血,為正細胞正色素性貧血,如伴有缺鐵,則可為低色素性小細胞性貧血。白細胞數大多正常,在活動期可略有增高,偶見嗜酸性粒細胞和血小板增多。貧血和血小板增多症與疾病的活動相關。多86%E8%83%9E target=_blank class=innerlink>紅細胞沉降率在活動 性病 變中常增高,可為疾病活動的指標。血清鐵、鐵結合蛋白的水平常減低。
2.血清白蛋白降低,球蛋白增高。免疫蛋白電泳顯示IgG、IgA及IgM增多。C反應蛋白活動期可升
3.類風濕因子及其它血清學檢查:類風濕因子包括IgG型RF、IgM型RF、IgA型RF,和IgE型RF等類型。目前臨床多限於檢測IgM-RF,目前國內應用比較廣泛的是聚苯乙烯微粒乳膠凝集試驗(LAT)和羊紅細胞凝集試驗(SCAT),這兩種方法對IgM-RF特異性較大,敏感性較高,重複性好,檢測IgM-RF在成年RA患者中3/4陽性。IgM-RF高滴度陽性病人,病變活動重,病情進展快,不易緩解,預后較差,且有比較嚴重的關節外表現。類風濕因子陰性不能排除本病的可能,須結合臨床。此外RF為自身抗體,也可見於多種自身免疫性疾病及一些與免疫有關的慢性感染如系統性紅斑狼瘡,Sj■gren氏綜合症、慢性 肝炎、結節病,傳染性單核細胞增多症、麻風、結核病、血吸蟲 病等。此外正常人接種或輸血后亦可出現暫時性RF(十)。RA患者的親屬亦可發現RF陽性。正常人尤其是高齡者可有5%呈陽性,故RF陽性,不一定就是類風濕性關節炎,但結合臨床仍為診斷RA的重要輔助方法。
近來發現類風濕性關節炎患者血清中抗類風濕性關節炎協同核抗原抗體(抗RANA抗體)的陽性率(93%~95%),明顯高於其他各種類型關節炎的患者(約19%)及 健康 人(約16%),可作為診斷類風濕性關節炎的一項有力證據。
抗核抗體在類風濕性關節炎的陽性率約10%~20%。血清補體水平多數正常或輕度升高,重症者及伴關節外病變者可下降。
4.關節腔穿刺可得不透明草黃色滲出液,其中中性粒細胞可達1萬~5萬/mm3或更高,細菌培養陰性。疾病活動期可見白細胞胞漿中含有類風濕因子和IgG補體複合物形成包涵體吞噬細胞,稱類風濕細胞(regocyte)。滲出液中補體的相對濃度(與蛋白質含量相比較)降低,RF陽性。
X線檢查:早期患者的關節X線檢查除軟組織腫脹和關節腔滲液外一般都是陰性。關節部位 骨質疏鬆 可以在起病幾周內即很明顯。關節間隙減小和骨質的侵蝕,提示關節軟骨的消失,只出現在病程持續數月以上者。半脫位,脫位和骨性強直是更後期的現象。當軟骨已損毀,可見兩骨間的關節面融合,喪失原來關節的跡象。瀰漫性骨質疏鬆在慢性病變中常見,並因激素治療而加重。無菌性壞死的發生率特別在股骨頭,亦可因用皮質類固醇治療而增多。
(1)X線片關節X線片可見軟組織腫脹、骨質疏鬆及病情進展后的關節面囊性變、侵襲性骨破壞、關節面模糊、關節間隙狹窄、關節融合及脫位。X線分期:①Ⅰ期正常或骨質疏鬆;②Ⅱ期骨質疏鬆,有輕度關節面下骨質侵襲或破壞,關節間隙輕度狹窄;③Ⅲ期關節面下明顯的骨質侵襲和破壞,關節間隙明顯狹窄,關節半脫位畸形;④Ⅳ期上述改變合併有關節纖維性或骨性強直。胸部X線片可見肺間質病變、胸腔積液等。
(2)CT檢查胸部CT可進一步提示肺部病變,尤其高分辨CT對肺間質病變更敏感。
(3)MRI檢查手關節及腕關節的MRI檢查可提示早期的滑膜炎病變,對發現類風濕關節炎患者的早期關節破壞很有幫助。
(4)超聲關節超聲是簡易的無創性檢查,對於滑膜炎、關節積液以及關節破壞有鑒別意義。研究認為其與MRI有較好的一致性。
RA在世界各地均有發病,但各個國家和地區的患病率不同,全世界患病率平均1%左右(0.3%~2.1%)。發病率隨年齡增長而增高,常在40~50多歲發病。我國以東北、華北地區為多。在發病特點,臨床表現以及病變程度上,各地區,各民族間也存在差異。非洲撒哈拉邊緣地區的RA發病率及嚴重程度較低。我國RA患者在病情進展和病變程度上均較西方國家為輕。
類風濕性關節炎病變的組織變化雖可因部位而略有變異,但基本變化相同。其特點有:①瀰漫或局限性組織中的淋巴或漿細胞浸潤,甚至淋巴濾泡形成。②血管炎,伴隨內膜增生管腔狹小、阻塞,或管壁的纖維蛋白樣壞死。③類風濕性肉芽腫形成。
1.關節腔早期變化是滑膜炎,滑膜充血、水腫及大量單核細胞、漿細胞、淋巴細胞浸潤,有時有淋巴濾泡形成,常有小區淺表性滑膜細胞壞死而形成的糜爛,並覆有纖維素樣沉積物。後者由含有少量γ球蛋白的補體複合物組成,關節腔內有包含中性粒細胞的滲出物積聚。滑膜炎的進一步變化是血管翳形成,其中除增生的纖維母細胞和毛細血管使滑膜絨毛變粗大外,並有淋巴濾泡形成,漿細胞和粒細胞浸潤及不同程度的血管炎,滑膜細胞也隨之增生。在這種增生滑膜細胞,或淋巴、漿細胞中含有可用熒光素結合的抗原來檢測出類風濕因子、γ球蛋白或抗原抗體複合物。
血管翳可以自關節軟骨邊緣處的滑膜逐漸向軟骨面伸延,被覆於關節軟骨面上,一方面阻斷軟骨和滑液的接觸,影響其營養。另外也由於血管翳中釋放某些水解酶對關節軟骨,軟骨下骨,韌帶和肌腱中的膠原基質的侵蝕作用,使關節腔破壞,上下面融合,發生纖維化性強硬、錯位,甚至骨化,功能完全喪失,相近的骨組織也產生廢用性的稀疏。
2.關節外病變有類風濕性皮下小結,見於約10%~20%病例。在受壓或摩擦部位的皮下或骨膜上出現類風濕性肉芽腫結節,中央是一團由壞死組織、纖維素和含有IgG的免疫複合物沉積形成的無結構物質,邊緣為柵狀排列的成纖維細胞。再外則為浸潤著單核細胞的纖維肉芽組織。少數病員肉芽腫結節可出現在內臟器官中。
3.類風濕性關節炎時脈管亦常受侵犯,動脈各層有較廣泛炎性細胞浸潤。急性期用免疫熒光法可見免疫球蛋白及補體沉積於病變的血管壁。其表現形式有三種:①嚴重而廣泛的大血管壞死性動脈炎,類似於結節性多動脈炎。②亞急性小動脈炎,常見於心肌、骨骼肌和神經鞘內小動脈,並引起相應癥狀。③末端動脈內膜增生和纖維化,常引起指(趾)動脈充盈不足,可致缺血性和血栓性病變;前者表現為雷諾氏現象、肺動脈高壓和內臟缺血,後者可致指(趾)壞疽,如發生於內臟器官則可致死。
4.肺部損害可以有:①慢性胸膜滲出,胸水中所見"RA"細胞是含有IgG和IgM免疫複合物的上皮細胞。②Caplan綜合征是一種肺塵病,與類風濕性關節炎肺內肉芽腫相互共存的疾病,已發現該肉芽腫有免疫球蛋白和補體的沉積,並在其鄰近的漿細胞中查獲RF。③間質性肺纖維化,其病變周圍可見淋巴樣細胞的集聚,個別有抗體的形成。
淋巴結腫大見於30%的病例,有淋巴濾泡增生,脾大尤其是在FELTy綜合征。
尚未完全明確。類風濕性關節炎是一個與環境、細菌、病毒、遺傳、性激素及神經精神狀態等因素密切相關的疾病。
(一)細菌因素 實驗研究表明A組鏈球菌及菌壁有肽聚糖(peptidoglycan)可能為RA發病的一個持續的刺激原,A組鏈球菌長期存在於體內成為持續的抗原,刺激機體產生抗體,發生免疫病理損傷而致病。支原體所製造的關節炎動物模型與人的RA相似,但不產生人的RA所特有的類風濕因子(RF)。在RA病人的關節液和滑膜組織中從未發現過細菌或菌體抗原物質,提示細菌可能與RA的起病有關,但缺乏直接證據。
(二)病毒因素 RA與病毒,特別是EB病毒的關係是國內外學者注意的問題之一。研究表明,EB病毒感染所致的關節炎與RA不同,RA病人對EB病毒比正常人有強烈的反應性。在RA病人血清和滑膜液中出現持續高滴度的抗EB病毒--胞膜抗原抗體,但到目前為止在RA病人血清中一直未發現EB病毒核抗原或殼體抗原抗體。
(三)遺傳因素 本病在某些家族中發病率較高,在人群調查中,發現人類白細胞抗原(HLA)-DR4與RF陽性患者有關。HLA研究發現DW4與RA的發病有關,患者中70%HLA-DW4陽性,患者具有該位點的易感基因,因此遺傳可能在發病中起重要作用。
(四)性激素 研究表明RA發病率男女之比為1∶2~4,妊娠期病情減輕,服避孕藥的女性發病減少。動物模型顯示LEW/n雌鼠對關節炎的敏感性高,雄性發病率低,雄鼠經閹割或用β-雌二醇處理后,其發生關節炎的情況與雌鼠一樣,說明性激素在RA發病中起一定作用。
寒冷、潮濕、疲勞、營養不良、創傷、精神因素等,常為本病的誘發因素,但多數患者病前常無明顯誘因可查。
類風濕性關節炎至今尚無特效療法,仍停留於對炎症及後遺症的治療,採取綜合治療,多數患者均能得到一定的療效。現行治療的目的在於:①控制關節及其它組織的炎症,緩解癥狀;②保持關節功能和防止畸形;③修復受損關節以減輕疼痛和恢復功能。
(一)一般療法 發熱及關節腫痛、全身癥狀嚴重者應卧床休息,至癥狀基本消失為止。待病情改善兩周后應逐漸增加活動,以免過久??蛋白質和各種維生素要充足,貧血顯著者可予小量輸血,如有慢性病灶如扁桃體炎等在病人健康情況允許下,儘早摘除。
(二)藥物治療
1.非甾體類抗炎葯(NSAIDS)用於初發或輕症病例,其作用機理主要抑制環氧化酶使前列腺素生成受抑制而起作用,以達到消炎止痛的效果。但不能阻止類風濕性關節炎病變的自然過程。本類藥物因體內代謝途徑不同,彼此間可發生相互作用不主張聯合應用,並應注意個體化。
(1)水楊酸製劑:能抗風濕,抗炎,解熱,止痛。劑量每日2~4g,如療效不理想,可酌量增加劑量,有時每日需4~6克才能有效。一般在飯後服用或與制酸劑同用,亦可用腸溶片以減輕胃腸道刺激。
(2)吲哚美辛:系一種吲哚醋酸衍生物,具有抗炎、解熱和鎮痛作用。患者如不能耐受阿斯匹林可換用本葯,常用劑量25mg每天2~3次,每日100mg以上時易產生副作用。副作用有噁心、嘔吐、腹瀉、胃潰瘍、頭痛、眩暈、精神 抑鬱 等。
(3)丙酸衍生物:是一類可以代替阿斯匹林的藥物,包括布洛芬,(ibuprofen)萘普生(naproxen)和芬布芬(fenbufen)作用與阿斯匹林相類似,療效相仿,消化道副作用小。常用劑量:布洛芬每天1.2~2.4g,分3~4次服。萘普生每次250mg,每日2次。副作用有噁心、嘔吐、腹瀉、消化性潰瘍、胃腸道出血、頭痛及中樞神經系統紊亂如易激惹等。
(4)滅酸類藥物:為鄰氨基苯酸衍生物,其作用與阿斯匹林相仿。抗炎酸每次250mg,每日3~4次。氯滅酸每次200~400mg,每日3次。副作用有胃腸道反應,如噁心、嘔吐、腹瀉及食欲不振等。偶有皮疹,腎功能損害,頭痛等。
2.金製劑 目前公認對類風濕性關節炎有肯定療效。常用硫代蘋果酸金鈉(gold, sodium thiomalatemyochrysin)。用法第一周10mg肌注,第二周25mg。若無不良反應,以後每周50mg。總量達300~700mg時多數病人即開始見效,總量達600~1000mg時病情可獲穩定改善。維持量每月50mg。因停葯後有複發可能,國外有用維持量多年,直至終身者。金製劑用藥愈早,效果愈著。金製劑的作用慢,3~6個月始見效,不宜與免疫抑製劑或細胞毒藥物並用。若治療過程中總量已達1000mg,而病情無改善時,應停葯。口服金製劑效果與金注射劑相似。副作用有大便次數增多,皮疹,口腔炎,腎損害等,停葯后可恢復。
口服金製劑金諾芬(Auranofin)是一種磷化氫金的羥基化合物。劑量為6mg每日一次,2~3月後開始見效。對早期病程短的患者療效較好。副作用比注射劑輕,常見為腹瀉,但為一過性,緩解顯效率62.8%。
3.青黴胺 是一種含疏基的氨基酸藥物,治療慢性類風濕性關節炎有一定效果。它能選擇性抑制某些免疫細胞使IgG及IgM減少。副作用有血小板減少,白細胞減少,蛋白尿,過敏性皮疹,食欲不振,視神經炎,肌無力,轉氨酶增高等。用法第一個月每天口服250mg,第二個月每次250mg,每日2次。無明顯效果第三個月每次250mg,每日三次。每次總劑量達750mg為最大劑量。多數在3個月內臨床癥狀可改善,癥狀改善後用小量維持,療程約一年。
4.氯喹 有一定抗風濕作用,但顯效甚慢,常6周至6個月才能達到最大療效。可作為水楊酸製劑或遞減皮質類固醇劑量時的輔助藥物。每次口服250~500mg,每日2次。療程中常有較多胃腸道反應如噁心、嘔吐和食慾減退等。長期應用須注意視網膜的退行性變和視神經萎縮等。
5.左旋咪唑 可減輕疼痛、縮短關節僵硬的時間。劑量為第一周50mg,每日1次,第二周50mg,每日2次,第三周50mg,每日3次。副作用有眩暈、噁心、過敏性皮疹、視力減退、嗜睡、粒細胞減少、血小板減少、肝功能損害、蛋白尿等。
6.免疫抑製劑 適用在其它藥物無效的嚴重類風濕性關節炎患者,停葯情況下或激素減量的患者。常用的有硫唑嘌呤,每次50mg,每日2~3次。環磷醯胺每次50mg,每日2次。待癥狀或實驗室檢查有所改善後,逐漸減量。維持量為原治療量的1/2~2/3。連續用3~6個月。副作用有骨髓抑制、白細胞及血小板下降,肝臟毒性損害及消化道反應、脫髮、閉經、出血性膀胱炎等。
氨甲蝶吟(MTX)有免疫抑制與抗炎症作用,可降血沉,改善骨侵蝕,每周5~15mg肌注或口服,3個月為一療程。副作用有厭食、噁心、嘔吐、口腔炎、脫髮、白細胞或血小板減少、藥物性間質性 肺炎 與皮疹。可能成為繼金和青黴胺之後被選用的另一緩解性藥物。
7.腎上腺皮質激素 腎上腺皮質激素對關節腫痛,控制炎症,消炎止痛作用迅速,但效果不持久,對病因和發病機理毫無影響。一旦停葯短期內即複發。對RF、血沉和貧血也無改善。長期應用可導致嚴重副作用,因此不作為常規治療,僅限於嚴重血管炎引起關節外損害而影響重要器官功能者,如眼部併發症有引起失明危險者,中樞神經系統病變者,心臟傳導阻滯,關節有持續性活動性滑膜炎等可短期應用,或經NSAIDS、青黴胺等治療效果不好,癥狀重,影響日常生活,可在原有藥物的基礎上加用小劑量皮質類固醇。如奏效不著可酌情增加,癥狀控制后應逐步減量至最小維持量。
醋酸氫化潑尼松混懸液可作局部關節腔內注射,適用於某些單個大關節頑固性病變,每次關節腔內注射25~50mg,嚴防關節腔內感染和骨質破壞。去炎舒松特丁乙酸酯,是一種適合關節內給葯的長效皮質類固醇,一次量為10mg,膝關節為30mg。
8.雷公藤 經國內多年臨床應用和實驗研究有良好療效。有非甾類抗炎作用,又有免疫抑制或細胞毒作用,可以改善癥狀,使血沉和RF效價降低,雷公藤多甙60mg/d,1~4周可出現臨床效果。副作用有女性 月經 不調及停經,男性精子數量減少,皮疹,白細胞和血小板減少,腹痛腹瀉等。停葯后可消除。
昆明山海棠,作用與雷公藤相似,每次2~3片,每天3次。療程3~6月以上。副作用頭昏、口乾、咽痛、食慾減退、腹痛、閉經。
9.其它治療 胸腺素、血漿去除療法等尚待探索。
(三)理療 目的在於用熱療以增加局部血液循環,使肌肉鬆弛,達到消炎、去腫和鎮痛作用,同時採用 鍛煉 以保持和增進關節功能。理療方法有下列數種:熱水袋、熱浴、蠟浴、紅外線等。理療后同時配以按摩,以改進局部循環,鬆弛肌肉痙攣。
鍛煉的目的是保存關節的活動功能,加強肌肉的力量和耐力。在急性期癥狀緩解消退後,只要患者可以耐受,便要早期有規律地作主動或被動的關節鍛煉活動。
(四)外科治療 以往一直認為外科手術只適用於晚期畸形病例。目前對僅有1~2個關節受損較重、經水楊酸鹽類治療無效者可試用早期滑膜切除術。後期病變靜止,關節有明顯畸形病例可行截骨矯正術,關節強直或破壞可作關節成形術、人工關節置換術。負重關節可作關節融合術等。
一般說來早期即予積極的綜合性治療,恢復大多較好。起病急的優於起病緩者,男性較女性為好,僅累及少數關節而全身癥狀輕微者,或累及關節不屬對稱分佈者,往往病程短暫,約有10%~20%患者因治療不及時而成殘廢。本病不直接引起死亡,但嚴重晚期病例可死於繼發感染。
發病呈急驟者的病程進展較短促,一次發作后可數月或數年暫無癥狀,靜止若干時后再反覆發作。發作呈隱襲者的病程進展緩慢而漸進,全程可達數年之久,其間交替的緩解和複發是其特徵。約10%~20%的病人每次發作后緩解是完全性的。每經過一次發作病變關節變得更為僵硬而不靈活,最終使關節固定在異常位置,形成畸形。據國外統計,在發病的幾年內勞動力完全喪失者約佔10%。
本病與預后不良有關的一些表現為:①典型的病變(對稱性多關節炎,伴有皮下結節和類風濕因子的高滴度);②病情持續活動一年以上者;③30歲以下的發病者;④具有關節外類風濕性病變表現者。
1.好發人群
女性好發,發病率為男性的2~3倍。可發生於任何年齡,高發年齡為40~60歲。
2.癥狀體征
可伴有體重減輕、低熱及疲乏感等全身癥狀。
(1)晨僵早晨起床時關節活動不靈活的主觀感覺,它是關節炎症的一種非特異表現,其持續時間與炎症的嚴重程度成正比。
(2)關節受累的表現①多關節受累呈對稱性多關節炎(常≥5個關節)。易受累的關節有手、足、腕、踝及顳頜關節等,其他還可有肘、肩、頸椎、髖、膝關節等。②關節畸形手的畸形有梭形腫脹、尺側偏斜、天鵝頸樣畸形、鈕扣花樣畸形等。足的畸形有跖骨頭向下半脫位引起的仰趾畸形、外翻畸形、跖趾關節半脫位、彎曲呈錘狀趾及足外翻畸形。③其他可有正中神經/脛后神經受壓引起的腕管∕跗管綜合征,膝關節腔積液擠入關節后側形成腘窩囊腫(Baker囊腫),頸椎受累(第2、3頸椎多見)可有頸部疼痛、頸部無力及難以保持其正常位置,寰樞關節半脫位,相應有脊髓受壓及椎基底動脈供血不足的表現。
(3)關節外表現①一般表現可有發熱、類風濕結節(屬於機化的肉芽腫,與高滴度RF、嚴重的關節破壞及RA活動有關,好發於肘部、關節鷹嘴突、骶部等關節隆突部及經常受壓處)、類風濕血管炎(主要累及小動脈的壞死性小動脈炎,可表現為指、趾端壞死、皮膚潰瘍、外周神經病變等)及淋巴結腫大。②心臟受累可有心包炎、心包積液、心外膜、心肌及瓣膜的結節、心肌炎、冠狀動脈炎、主動脈炎、傳導障礙,慢性心內膜炎及心瓣膜纖維化等表現。③呼吸系統受累可有胸膜炎、胸腔積液、肺動脈炎、間質性肺疾病、結節性肺病等。④腎臟表現主要有原發性腎小球及腎小管間質性腎炎、腎臟澱粉樣變和繼發於藥物治療(金製劑、青黴胺及NSAIDs)的腎損害。⑤神經系統除周圍神經受壓的癥狀外,還可誘發神經疾病、脊髓病、外周神經病、繼發於血管炎的缺血性神經病、肌肥大及藥物引起的神經系統病變。⑥貧血是RA最常見的關節外表現,屬於慢性疾病性貧血,常為輕至中度。⑦消化系統可因RA血管炎、併發症或藥物治療所致。⑧眼幼年患者可有葡萄膜炎,成人可有鞏膜炎,可能由血管炎所致。還可有乾燥性結膜角膜炎、鞏膜軟化、鞏膜軟化穿孔、角膜溶解。
(4)Felty綜合征1%的RA患者可有脾大、中性粒細胞減少(及血小板減少、紅細胞計數減少),常有嚴重的關節病變、高滴度的RF及ANA陽性,屬於一種嚴重型RA。
(5)緩解性血清陰性、對稱性滑膜炎伴凹陷性水腫綜合征(RS3PE)男性多見,常於55歲以後發病,呈急性發病,有對稱性腕關節、屈肌腱鞘及手小關節的炎症,手背可有凹陷性水腫。晨僵時間長(0.5~1天),但RF陰性,X線多沒有骨破壞。有56%的患者為HLA-B7陽性。治療上對單用NSAIDs藥物反應差,而小劑量糖皮質激素療效顯著。常於1年後自發緩解,預后好。
(6)成人Still病(AOSD)以高熱、關節炎、皮疹等的急性發作與緩解交替出現的一種少見的RA類型。因臨床表現類似於全身起病型幼年類風濕關節炎(Still病)而得名。部分患者經過數次發作轉變為典型的RA。
(7)老年發病的RA常>65歲起病,性別差異小,多呈急性發病,發展較快(部分以OA為最初表現,幾年後出現典型的RA表現)。以手足水腫、腕管和跗管綜合征及多肌痛為突出表現,晨僵明顯,60%~70%RF陽性,但滴度多較低。X線以骨質疏鬆為主,很少侵襲性改變。患者常因心血管、感染及腎功能受損等合併症而死亡。選用NSAIDs要慎重,可應用小劑量激素,對慢作用抗風濕葯(SAARD)反應較好。