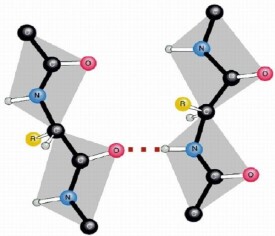
分子間氫鍵
分子間有氫鍵粘度較大的液體
分子間氫鍵是分子間有氫鍵的液體,一般粘度較大。
例甘油、磷酸、濃硫酸等多羥基化合物,由於分子間可形成眾多的氫鍵,這些物質通常為粘稠狀液體。分子內生成氫鍵,熔、沸點常降低。例如有分子內氫鍵的鄰硝基苯酚熔點(45℃)比有分子間氫鍵的間位熔點(96℃)和對位熔點(114℃)都低。
氫鍵
例氫鍵形。HF分子中,由於F的電負性(4.0)很大,共用電子對強烈偏向F原子一邊,而H原子核外只有一個電子,其電子云向F原子偏移的結果,使得它幾乎要呈質子狀態。這個半徑很小、無內層電子的帶部分正電荷的氫原子,使附近另一個HF分子中含有孤電子對並帶部分負電荷的F原子有可能充分靠近它,從而產生靜電吸引作用。這個靜電吸引作用力就是所謂氫鍵。不同種分子之間僅同種分子之間可以存在氫鍵,某些不同種分子之間也可能形成氫鍵。
分子內氫鍵
某些分子內,例如HNO、鄰硝基苯酚分子可以形成分子內氫鍵。分子內氫鍵由於受環狀結構的限制,X-H…Y往往不能在同一直線上。
⑴與電負性很大的原子A形成強極性鍵的氫原子⑵較小半徑、較大電負性、含孤電子對、帶有部分負電荷的原子B(F、O、N)氫鍵的本質:強極性鍵(A-H)上的氫核,與電負性很大的、含孤電子對並帶有部分負電荷的原子B之間的靜電引力。}⑶表示氫鍵結合的通式
氫鍵結合的情況如果寫成通式,可用X-H…Y①表示。式中X和Y代表F,O,N等電負性大而原子半徑較小的非金屬原子。X和Y可以是兩種相同的元素,也可以是兩種不同的元素。⑷對氫鍵的理解氫鍵存在雖然很普遍,對它的研究也在逐步深入,但是人們對氫鍵的定義至今仍有兩種不同的理解。第一種把X-H…Y整個結構叫氫鍵,因此氫鍵的鍵長就是指X與Y之間的距離,例如F-H…F的鍵長為255pm。第二種把H…Y叫做氫鍵,這樣H…F之間的距離163pm才算是氫鍵的鍵長。這種差別,我們在選用氫鍵鍵長數據時要加以注意。不過,對氫鍵鍵能的理解上是一致的,都是指把X-H…Y-H分解成為HX和HY所需的能量。
氫鍵的牢固程度——鍵強度也可以用鍵能來表示。粗略而言,氫鍵鍵能是指每拆開單位物質的量的H…Y鍵所需的能量。氫鍵的鍵能一般在42kJ·mol以下,比共價鍵的鍵能小得多,而與分子間力更為接近些。例如,水分子中共價鍵與氫鍵的鍵能是不同的。
而且,氫鍵的形成和破壞所需的活化能也小,加之其形成的空間條件較易出現,所以在物質不斷運動情況下,氫鍵可以不斷形成和斷裂。
氫鍵通常是物質在液態時形成的,但形成後有時也能繼續存在於某些晶態甚至氣態物質之中。例如在氣態、液態和固態的HF中都有氫鍵存在。能夠形成氫鍵的物質是很多的,如水、水合物、氨合物、無機酸和某些有機化合物。氫鍵的存在,影響到物質的某些性質。
(1)熔點、沸點分子間有氫鍵的物質熔化或氣化時,除了要克服純粹的分子間力外,還必須提高溫度,額外地供應一份能量來破壞分子間的氫鍵,所以這些物質的熔點、沸點比同系列氫化物的熔點、沸點高。分子內生成氫鍵,熔、沸點常降低。例如有分子內氫鍵的鄰硝基苯酚熔點(45℃)比有分子間氫鍵的間位熔點(96℃)和對位熔點(114℃)都低。
(3)粘度分子間有氫鍵的液體,一般粘度較大。例如甘油、磷酸、濃硫酸等多羥基化合物,由於分子間可形成眾多的氫鍵,這些物質通常為粘稠狀液體。
(4)密度液體分子間若形成氫鍵,有可能發生締合現象,例如液態HF,在通常條件下,除了正常簡單的HF分子外,還有通過氫鍵聯繫在一起的複雜分子(HF)n。nHF(HF)n
其中n可以是2,3,4…。這種由若干個簡單分子聯成複雜分子而又不會改變原物質化學性質的現象,稱為分子締合。分子締合的結果會影響液體的密度。
HO分子之間也有締合現象。
常溫下液態水中除了簡單HO分子外,還有(H2O)2,(H2O)3,…,(H2O)n等締合分子存在。降低溫度,有利於水分子的締合。溫度降至0℃時,全部水分子結成巨大的締合物——冰。