共找到2條詞條名為四氟化硅的結果 展開
- 有機硅化合物的合成材料
- 水泥和人造大理石的硬化劑
四氟化硅
有機硅化合物的合成材料
四氟化硅是一種無機物,分子式為SiF4,分子量為104.06。
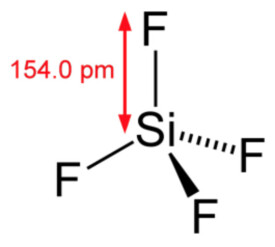
分子結構是Si原子以sp3雜化軌道形成σ鍵,分子形狀為正四面體形,它的分子式為SiF4,分子量為104.06,它的密度是1.590,儲存需要避免強酸,避免潮濕空氣。
儲存注意事項:儲存於陰涼、通風的有毒氣體專用庫房。遠離火種、熱源。庫溫不宜超過30℃。應與酸類、食用化學品分開存放,切忌混儲。儲區應備有泄漏應急處理設備。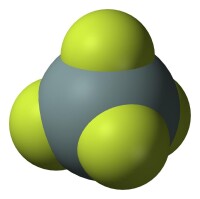

四氟化硅
避免強酸,避免潮濕空氣。在1318mmHg(1mmHg=133.322Pa)壓力下的熔點(三相點)為-90.2℃。在-95.7℃升華。液體的相對密度為1.590(-88℃)。吸濕性非常強,但如果完全無濕氣時,並不腐蝕玻璃、汞、活塞上的潤滑脂、橡膠等。加壓下變成液體,可以利用這一特點進行分餾提純。
四氟化硅的製備裝置A-派熱克斯玻璃反應器;B-電爐;C-杜瓦斯;D-接收器;E-耐壓瓶(50ml);F-汞儲槽;G-乾冰-丙酮;H-液氮。

abundance
1.將25g BaCl·2HO溶於70mL水中,再向其中加入30% HSiF,直到BaSiF完全沉澱出來。過濾,用水反覆洗滌,直到無氯離子。加熱至110~120℃進行乾燥,再放入裝有P2O5的乾燥器中乾燥。將製得的BaSiF用圖所示裝置使其熱分解。四氟化硅的製備裝置A—派熱克斯玻璃反應器;B—電爐;C—杜瓦瓶;D—接收器;E—耐壓瓶(50mL);F—汞儲槽;G—乾冰?丙酮;H—液氮將BaSiF放入反應管內,一邊進行真空脫水,一邊升溫至200℃,使其完全乾燥。將第一接收器放入乾冰?丙酮中,接收生成的雜質氟硅酸及氟化氫等。當溫度升至300℃,就開始產生四氟化硅,在插入液氮中的第二接收器中接收。繼續升溫至500℃,就轉為激烈的熱分解,於是可得到白色固體四氟化硅。收率為75%,純度在98%以上。
2.將25g粉碎的硅膠(含有37.5%水)放入250mL燒瓶中,燒瓶上裝有攪拌器、滴液漏斗、疏鬆填裝玻璃棉的迴流冷凝器。把燒瓶的溫度升到100℃,在45min內,緩慢滴加100g氟代磺酸。由於立即有氣體產生,所以首先使之通過浸沒在乾冰-丙酮中的捕集器。在此除去混入的氟代磺酸,然後在用液氮冷卻的捕集器中捕集。當氣體不再產生以後,仍要在100℃保持2h。收率84%,可得到21.8g四氟化硅。在氟化鈣和石英砂的混合物中加入濃硫酸使之反應的方法也可製得四氟化硅。但因混入了許多氟化氫和氟硅酸,所以並不理想。
四氟化硅中文名稱:四氟化硅
英文名稱: silicon tetrafluoride
中文名稱2:氟化硅
分子結構:
Si原子以sp3雜化軌道形成σ鍵。分子形狀為正四面體形。
英文名稱2: silicon fluoride
CAS No.: 7783-61-1
分子式: SiF4
分子量: 104.06
理化特性
主要成分:純品
健康危害:本品對眼、皮膚、粘膜和呼吸道有嚴重損害。局部腐蝕作用強。嚴重中毒者可致肺炎、肺水腫。
燃爆危險:本品不燃,有毒,具腐蝕性、刺激性,可致人體灼傷。
危險特性:在潮濕空氣中產生白色有腐蝕性和刺激性的氟化氫煙霧。遇水緩慢水解硅酸及氟化氫。
二氧化硅與氫氟酸反應則生成氣態四氟化硅:SiO2(s) + 4 HF(aq) → SiF4(aq) + 2 H2O(l)
與碳酸鈉溶液發生不完全水解反應:3SiF4+2Na2CO3+2H2O=H4SiO4↓+2Na2SiF6↓+2CO2
與 氫氧化鈉反應較為徹底;SiF4+6NaOH=Na2SiO3+4NaF+3H2O
與氫氟酸生成氟硅酸(六氟合硅酸)SiF4+2HF=H2SiF6
後者為強酸,酸性與硫酸相當。
危險運輸編碼:1859
危險品標誌:極毒
安全標識:S23S26S45S36/S37/S39
危險標識:R14R31R34R26/27/28
1、疏水參數計算參考值(XlogP):2.1
2、氫鍵供體數量:0
3、氫鍵受體數量:1
4、可旋轉化學鍵數量:2
5、互變異構體數量:2
6、拓撲分子極性表面積(TPSA):17.1
7、重原子數量:11
8、表面電荷:0
9、複雜度:152
10、同位素原子數量:0
11、確定原子立構中心數量:0
12、不確定原子立構中心數量:0
13、確定化學鍵立構中心數量:1
14、不確定化學鍵立構中心數量:0
15、共價鍵單元數量:1