靶向藥物
瞄準病變部位發揮藥效
靶向藥物(也稱作靶向製劑)是指被賦予了靶向(Targeting)能力的藥物或其製劑。其目的是使藥物或其載體能瞄準特定的病變部位,並在目標部位蓄積或釋放有效成分。靶向製劑可以使藥物在目標局部形成相對較高的濃度,從而在提高藥效的同時抑制毒副作用,減少對正常組織、細胞的傷害。
對於普通藥物而言,通常在進入體內后僅有極少一部分才能夠真正作用於病變部位。這是制約藥物療效,並導致藥物毒副作用的根本原因。獲取具有像導彈一樣精準靶向能力的藥物是人類的一個夢想,也是藥物開發的終極目標。
對於普通藥物而言,通常在進入體內后僅有極少一部分才能夠真正作用於病變部位。這是制約藥物療效,並導致藥物毒副作用的根本原因。獲取具有像導彈一樣精準靶向能力的藥物是人類的一個夢想,也是藥物開發的終極目標。
靶向藥物是指被賦予了靶向(Targeting)能力的藥物或其製劑。其目的是使藥物或其載體能瞄準特定的病變部位,並在目標部位蓄積或釋放有效成分。靶向製劑可以使藥物在目標局部形成相對較高的濃度,從而在提高藥效的同時抑制毒副作用,減少對正常組織、細胞的傷害。
靶向藥物
1、組織器官水平
使藥物選擇性的蓄積在腫瘤組織、炎症部位、或心肝脾肺等特定器官內,從而減少全身性的不良反應。目前針對腫瘤組織的靶向化療藥物是研究的一大熱點,如針對腫瘤缺氧、低pH、新生血管密集等特定環境設計的靶向藥物能夠提高腫瘤組織內的藥物濃度,顯著改善腫瘤化療的效果。
2、細胞水平
利用病變細胞表面的某些特定受體,在藥物或其載體表面修飾與該受體特異性結合的配體(如抗體、多肽、糖鏈、核酸適配體、或其他小分子等),使藥物能夠精確地定位到病變細胞並將其殺傷,而對正常細胞則不產生明顯的毒害作用。
3、亞細胞水平
很多藥物(如核酸藥物、大多數蛋白藥物、及部分小分子藥物)需要進入細胞內部,或者在特定細胞器(如線粒體、細胞核)內才能發揮作用。穿膜肽、核定位序列(Nuclearlocalizationsequence)等是目前研究較多的靶向組件。
根據靶向機理的不同,藥物靶向可分為被動靶向、主動靶向、物理靶向等幾類:
1、被動靶向
被動靶向製劑是指利用特定組織、器官的生理結構特點,使藥物在體內能夠產生自然的分佈差異,從而實現靶向效應。被動靶向多依賴於藥物或其載體的尺寸效應:如大於7μm的微粒通常會被肺部的小毛細管以機械濾過方式截留,被單核細胞攝取進入肺組織或肺氣泡;大於200nm的微粒則易被脾臟和肝臟的網狀內皮系統吞噬。被動靶向中最廣為人知的是EPR效應(EnhancedPermeabilityandRetentioneffect),其基於實體腫瘤與正常組織中微血管結構的不同:正常微血管內皮間隙緻密、結構完整,大分子及大尺寸顆粒不易透過血管壁;而實體瘤組織中的新生血管較多且血管壁間隙較寬、結構完整性差,淋巴迴流缺失。這種差異造成直徑在100nm上下的大分子類藥物或顆粒物質更易於聚集在腫瘤組織內部,從而實現靶向效果;除此之外,利用腫瘤部位特殊的pH、酶環境,以及細胞內的還原環境等,也可以實現藥物在特定部位的釋放,達到靶向給葯的目的。
2、主動靶向
主要是指賦予藥物或其載體主動與靶標結合的能力,主要手段包括將抗體、多肽、糖鏈、核酸適配體等能夠與靶標分子特異性結合的探針分子通過化學或物理方法偶聯到藥物或其載體表面,從而實現靶向效果。
3、物理靶向
利用光、熱、磁場、電場、超聲波等物理信號,人為調控藥物在體內的分佈及釋葯特性,實現對病變部位的靶向。
靶向藥物的特點決定了其尤其適合身體虛弱的晚期患者使用,因為這類患者的身體狀況無法承受化療放療帶來的副作用(身體虛弱,副作用很可能會成為壓垮患者的最後一根稻草),又不能通過手術對病灶進行清除(病灶已經發生擴散,很難徹底排查並切除)。

靶向藥物
例如用於治療HER2基因陽性(過量表達)的乳腺癌的赫塞汀(Herceptin,通用名Trastuzumab)、以EGFR為靶點的結腸癌和非小細胞肺癌治療藥物愛必妥(Erbitux,通用名Cetuximab)等。這類藥物是通過抗原抗體的特異性結合來識別腫瘤細胞的。
從通用名的後綴上來看,單克隆抗體類靶向藥物以“-mib”為後綴,而酪氨酸激酶類靶向藥物以“-nib”為後綴。
除上述列舉的已經進入臨床使用的靶向藥物外,另外還有多種靶向藥物正在開發中。
靶向藥物一般單獨使用或和化療藥物配合使用。對於已經經過充分臨床驗證的靶向藥物,在臨床上可用作一線、二線、三線治療,而對於新的靶向藥物,儘管已有資料表明其有效性,但還未經過充分的臨床驗證,一般用於二線、三線治療(即常規化療無效后的治療)。靶向藥物的使用,應該在醫生的指導下科學用藥。當臨床上已經顯示靶向藥物已經沒有明顯效果時(例如連續用藥一年後),說明癌細胞已經產生了耐藥性,這時應停止使用靶向藥物或更換治療方案。
靶向藥物的價格仍高於常規化療藥物,這在一定程度上限制了靶向藥物的推廣。但相信隨著科技的進步,其價格會降低,種類會增加,靶向藥物將會成為一類能夠帶來更好療效、更少痛苦的癌症治療藥物。
FDA已經批准的以藥物基因組學為基礎的抗瘤藥物的靶向治療藥物名單列舉如下: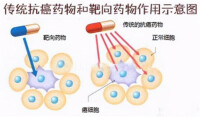

靶向藥物
1997年11月,利妥昔單抗(抗CD20單克隆抗體)獲准用於治療複發性或頑固性低度或濾泡性非霍奇金淋巴瘤。這也是FDA獲准治療腫瘤的第一個單克隆抗體;
1998年9月,曲妥珠單抗(抗HER2單克隆抗體)獲准用於治療轉移性乳腺癌;
2001年10月,甲磺酸伊馬替尼(酪氨酸激酶抑製劑)獲准用於治療慢性粒細胞性白血病(CML);
2002年9月,Tarceva獲准作為標準方案治療無效的晚期NSCLC的二線或三線治療方案。
2003年5月,吉非替尼(抗表皮生長因子單克隆抗體)獲准用於治療晚期非小細胞肺癌(NSCLC);
2004年2月,西妥昔單抗(抗表皮生長因子單克隆抗體)獲准用於治療轉移性結直腸癌。
靶向藥物中,肺癌靶向藥物易瑞沙、特羅凱和慢性髓性白血病治療藥物格列衛賣得最火。但據了解,這些抗癌藥物目前在中國國內並沒有生產,完全依靠從歐美醫藥公司進口。據一家正規國營藥店的報價,易瑞沙每盒5400多元,一個月需3盒至少15000元;特羅凱每盒19800多元,一個月需服用一盒;格列衛每盒11500多元,一個月服2盒至少23000元。
相比之下,“印度版”抗癌藥就便宜得多。印度第一大葯業公司Natco生產的易瑞沙、特羅凱、格列衛等,價格大約是正版歐美藥物的1/5~1/10。如“印度版”的易瑞沙,價格約為1800元一盒,特羅凱為4500元一盒,格列衛則為1800元一盒,且每盒均為30天的藥量。
這種價格上的明顯差異,就造成了印度版抗癌藥物在中國國內市場上的非法流通。“印度版”抗癌藥的銷售大多通過網路代購的形式進行,負責代購的主要是在印度工作的中國人,中間商販基本都活躍在網路上,不與客戶直接接觸。但是這些代購網站都沒有“網際網路藥品經營許可證”,並沒有在網上售葯的資格。
事實上,“印度版”抗癌藥的問題並不僅僅在於法律上,它們的療效到底有沒有保障,各方面都無法做出判斷。多名接受記者採訪的三甲醫院腫瘤科專家均不願評價“印度版”藥物的療效,他們認為,由於無法掌握這些葯的臨床試驗數據,別說療效,就連安全性都不敢保證。近年來,他們已陸續碰到因為使用不正規藥物而出現副作用的病人。按照印度醫學界做的臨床研究顯示,這些葯對於某些患者不僅沒有療效,甚至還可能誘發第二腫瘤。
故此,醫學專家呼籲患者及家屬,靶向藥物的選擇,一定要慎之又慎。
使藥物選擇性的蓄積在腫瘤組織、炎症部位、或心肝脾肺等特定器官內,從而減少全身性的不良反應。目前針對腫瘤組織的靶向化療藥物是研究的一大熱點,如針對腫瘤缺氧、低pH、新生血管密集等特定環境設計的靶向藥物能夠提高腫瘤組織內的藥物濃度,顯著改善腫瘤化療的效果。
利用病變細胞表面的某些特定受體,在藥物或其載體表面修飾與該受體特異性結合的配體(如抗體、多肽、糖鏈、核酸適配體、或其他小分子等),使藥物能夠精確地定位到病變細胞並將其殺傷,而對正常細胞則不產生明顯的毒害作用。
很多藥物(如核酸藥物、大多數蛋白藥物、及部分小分子藥物)需要進入細胞內部,或者在特定細胞器(如線粒體、細胞核)內才能發揮作用。穿膜肽、核定位序列(Nuclear localization sequence)等是目前研究較多的靶向組件。
被動靶向製劑是指利用特定組織、器官的生理結構特點,使藥物在體內能夠產生自然的分佈差異,從而實現靶向效應。被動靶向多依賴於藥物或其載體的尺寸效應:如大於7μm的微粒通常會被肺部的小毛細管以機械濾過方式截留,被單核細胞攝取進入肺組織或肺氣泡;大於200nm 的微粒則易被脾臟和肝臟的網狀內皮系統吞噬。被動靶向中最廣為人知的是EPR效應(Enhanced Permeability and Retention effect),其基於實體腫瘤與正常組織中微血管結構的不同:正常微血管內皮間隙緻密、結構完整,大分子及大尺寸顆粒不易透過血管壁;而實體瘤組織中的新生血管較多且血管壁間隙較寬、結構完整性差,淋巴迴流缺失。這種差異造成直徑在100nm上下的大分子類藥物或顆粒物質更易於聚集在腫瘤組織內部,從而實現靶向效果;除此之外,利用腫瘤部位特殊的pH、酶環境,以及細胞內的還原環境等,也可以實現藥物在特定部位的釋放,達到靶向給葯的目的。
主要是指賦予藥物或其載體主動與靶標結合的能力,主要手段包括將抗體、多肽、糖鏈、核酸適配體等能夠與靶標分子特異性結合的探針分子通過化學或物理方法偶聯到藥物或其載體表面,從而實現靶向效果。
利用光、熱、磁場、電場、超聲波等物理信號,人為調控藥物在體內的分佈及釋葯特性,實現對病變部位的靶向。