正向滲透法
正向滲透法
正向滲透法,實質就是“滲透法”,是與逆滲透、反滲透相對的方法,互反的方法。正向滲透法或“正向滲透技術”是利用膜兩側溶液的滲透壓差,使水分子從高化學勢一側滲透到低化 學勢一側的新型膜分離技術。
“正向滲透法”是低濃度溶液中的水或其他溶液通過半透性膜進入較高濃度溶液中的現象。如植物細胞的原生質膜、液泡膜都是半透性膜。植物的根主要靠滲透作用從土壤中吸收水分和礦物質等。
“正向滲透”是指水分子以及溶劑通過半透性膜的自然擴散滲透。熵增的過程。水的擴散同樣是從自由能高的地方向自由能低的地方移動,如果考慮到溶質的話,水是從溶質濃度低的地方向溶質濃度高的地方流動。更準確一點說,是從蒸汽壓高的地方擴散到蒸汽壓低的地方。
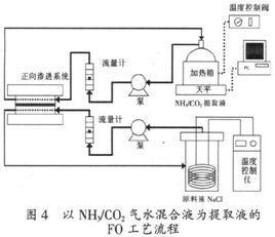
當純水和鹽水被理想半透膜隔開,理想半透膜只允許水通過而阻止鹽通過,此時膜純水側的水會自發地通過半透膜流入鹽水一側,這種現象稱為滲透,若在膜的鹽水側施加壓力,那麼水的自發流動將受到抑制而減慢,當施加的壓力達到某一數值時,水通過膜的凈流量等於零,這個壓力稱為滲透壓力,當施加在膜鹽水側的壓力大於滲透壓力時,水的流向就會逆轉,此時,鹽水中的水將流入純水側,上述現象就是水的反滲透(RO)處理的基本原理。
雖然這個問題太深奧,至今科學家們給出了一些解釋。其實把“滲透現象”理解清楚就可以。學界對於“滲透分離機理”的解釋主要流行以下四種理論:
既近代統一化的,最新的模型上世紀90年代鄧宇們的“干閉濕開模型”
干閉濕開模型
膜濕時,膜材料溶脹,膜的孔隙被溶劑溶脹,孔打開。合併就是“干閉濕開”脫鹽模型。
及早期的代表性的
正向滲透膜分離的原理和特徵
正向滲透法
正向滲透過程水分子從選擇性透過膜化學勢高的一側擴散到化學勢低的一側,而壓力延緩滲透是正向滲透和反滲透的中間過程,水壓作用於滲透壓梯度的反方向,水的凈通量仍然是向濃縮液方向。
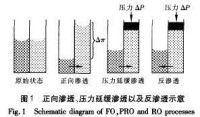
隨著科技的飛速發展,壓力驅動反滲透膜分離技術(RO)在膜、膜組器、設備和工藝等方面都有了較大創新和改進,但人們也越來越意識到RO技術在節能、環保領域存在的局限,而且就脫鹽來講,RO技術可認為已接近發展的頂峰。因此,近年來國外已經開展了“正向滲透膜分離技術(FO)”的相關研究,並取得了一定的成果,在海水淡化、污水處理、食品加工、醫藥等領域得到了應用,特別是“壓力延緩滲透(PRO)海水發電”,更是一項極具前景的清潔再生能源開發技術J。但是國內目前對正向滲透膜分離技術關注得很少,相關研究和論文也不多。雖然,上個世紀90年代我國有了創造性的發明“非加壓吸附滲透法海水淡化”(CN92110710.2)。
正向滲透分離技術很早就得到了應用。很久以前,人們就採用食鹽來長期貯存食物,因為在高鹽環境下多數細菌、黴菌和病原菌由於滲透作用會脫水死亡或暫時失去活性。如今,人們已經開始利用正向滲透膜分離技術進行 海水淡化、工業廢水處理、垃圾滲透液處理等研究;食品工業在實驗室利用正向滲透膜分離來濃縮飲料;緊急救援時的生命支持系統利用正向滲透膜分離技術製取淡水。近來隨著材料科學的發展,正向滲透技術已經應用於人體的藥物控制釋放。
非加壓滲透吸附法(90年代)
非加壓吸附滲透海水淡化法,或稱為“正向滲透法”,讓水通過多孔膜正向滲透進入一種超強吸水的吸附劑或鹽濃度甚至超過海水的溶液或固態物,不需要外界加壓,但溶液里的特殊鹽分"提取液"很容易蒸發,不需要加太多的熱(加熱能與反滲透加壓的能量比?)。分固態鹽、液態鹽方向。固態鹽解吸附耗能更小。
海水淡化技術:非加壓吸附滲透海水淡化法(CN92110710.2)1992年:上個世紀90年代鄧宇的發明,《美國化學文摘》收錄。
另外兩種方法都在薄膜結構上有了創新和改進
碳納米管薄膜
一種用碳納米管來做薄膜的小孔,另一種
活細胞的蛋白質膜
薄膜的孔用引導水分子通過活細胞的細胞膜的蛋白質來構成。
滲透、反滲透-逆滲透中的重要成員。
滲透劑的廣義概念是指一類能夠幫助需要滲透的物質滲透到需要被滲透物質的化學品,工業上一般是使用表面活性劑(可以是陰離子或非離子的)或有機或無機溶劑。
溶質是溶液中被分散的物質稱為溶質,溶質分散其中的介質稱為溶劑。這種區分實質上是以其在混合物中相對含量的多少為依據,不很嚴格,因此也就不是絕對的。不過對氣體或固態物質同液體組成的溶液,則不論液體的多少,一般均稱液體為溶劑。溶質一般以分子、原子或離子形態均勻地分佈於溶劑中。溶質粒子(如糖水中的蔗糖分子、氯化鈉溶液中的氯離子和鈉離子、碘酒中的碘分子)的直徑一般小於1 nm。像砂糖等被溶解的物質稱為溶質。都包括固體,液體,氣體。
溶質分散其中的介質稱為溶劑。溶質和溶劑是相對而言的。兩種液體互相溶解時,通常把量多的一種叫溶劑,量少的一種叫溶質。例如酒精和水互相溶解時,一般來說酒精是溶質,水是溶劑,如果少量水溶解在酒精里,也可把水作為溶質,酒精作為溶劑。一般在水溶液里總是把水作為溶劑。應用最廣的溶劑是水。溶劑分極性溶劑(高介電常數)和非極性溶劑(低介電常數)兩類。最典型的極性溶劑是水,非極性溶劑如烴類。芳香烴(如苯)的溶解能力強於脂肪烴(如汽油)。很多有機物也作為溶劑使用,常稱為有機溶劑,如醇、醚、酮和鹵代烴,化學工業生產大量的有機溶劑,它們在塗料、塑料、合成橡膠中有廣泛的應用。
滲透劑(JFC)的全稱是脂肪醇聚氧乙烯醚,屬非離子表面活性劑。滲透劑顧名思義是起滲透作用,也是具有固定的親水親油基團,在溶液的表面能定向排列,並能使表面張力顯著下降的物質。
滲透劑一般分為非離子很陰離子兩類。非離子的有JFC、JFC-1、JFC-2、JFC-E等;陰離子的有快速滲透劑T、耐鹼滲透劑OEP-70、耐鹼滲透劑AEP、高溫滲透劑JFC-M等等。
滲透作用(osmosis)兩種不同濃度的溶液隔以半透膜(允許溶劑分子通過,不允許溶質分子通過的膜),水分子或其它溶劑分子從低濃度的溶液通過半透膜進入高濃度溶液中的現象。或水分子從水勢高的一方通過半透膜向水勢低的一方移動的現象。植物細胞的液泡充滿水溶液,將液泡膜及質膜視為半透膜,則細胞與細胞之間,或細胞浸於溶液或水中,都會發生滲透作用。實際上,生物膜並非理想半透膜,它是選擇透性膜,既允許水分子通過也允許某些溶質通過,但通常使溶劑分子比溶質分子通過要多得多,因此可以發生滲透作用。植物細胞由於細胞壁的存在,可以產生壓力而逐漸使細胞內外水勢相等,細胞停止滲透吸水。所以植物細胞放在水中一般不會破裂。動物細胞如紅細胞放入水中即會破裂。
滲透現象發生的條件
半透膜、細胞內外濃度差
滲透實驗
把蠶豆種皮緊縛在漏鬥上,注入蔗糖溶液,然後把整個裝置浸入盛有清水的燒杯中,漏斗內外液面相等。由於蠶豆種皮是接近半透膜(semipermeable membrane)(即讓水分子通過而蔗糖分子不能透過的一種薄膜),所以整個裝置就成為一個滲透系統。在一個滲透系統中,水的移動方向決定於半透膜兩邊溶液的水勢高低。水勢高的溶液的水,流向水勢低的溶液。實質上,半透膜兩邊的水分子是可以自由通過的,可是清水的水勢高,蔗糖溶液的水勢低,從清水到蔗糖溶液的水分子比從蔗糖溶液到清水的水分子多,所以在外觀上,燒杯中清水的水流入漏斗內,漏斗內的玻璃管內液面上升,靜水壓也開始增高。隨著水分逐漸進入玻璃管內,液面越上升,靜水壓也越大,壓迫水分從玻璃管內向燒杯移動速度就越快,膜內外水分進出速度越來越接近。最後,液面不再上升,停留不動,實質上是水分進出的速度相等,呈動態平衡。水分從水勢高的系統通過半透膜向水勢低的系統移動的現象,就稱為滲透作用(osmosis)。
滲透作用與吸脹作用與滲透機理
滲透作用與吸脹作用
吸脹作用(imbibition)親水凝膠吸附水分子,並使其膨脹的過程。為非生命的物理過程。植物組織中含有很多這類物質如纖維素、果膠物質、澱粉和蛋白質等,它們具有很強的親水性,在未被水飽和時,就潛伏著很強的吸水能力。最明顯的例子是風乾種子,因為其內貯存著大量蛋白質或澱粉。蛋白質與水結合的趨勢大於澱粉,因此,豆類種子吸脹作用極為明顯。吸脹物體由於吸附水分子而膨脹,其壓力是很大的,如將干種子塞滿岩石裂縫,借其吸水產生的吸脹壓力能使岩石破裂。
植物吸收水分的方式
植物吸收水分的方式有兩種:吸脹作用和滲透作用。
吸脹作用是沒有液泡的植物細胞吸收水分的方式,如生長點的細胞、干種子細胞等,原理是細胞中有大量親水性物質,這些親水性能夠從外界吸收大量的水分,活細胞、死細胞都能通過吸脹作用吸收水分。
滲透作用是具有液泡的成熟的植物細胞吸收水分的方式,原理是:原生質層具有 選擇透過性,原生質層內外的溶液存在著濃度差,水分子就可以從溶液濃度低的一側通過原生質層擴散到溶液濃度高的一側。溶液滲透壓的高低與溶液中溶質分子的物質的量的多少有關,溶液中溶質分子物質的量越多,滲透壓越高,反之則越低。在比較兩種溶液滲透壓高低時以兩種溶液中的溶質分子的物質的量為標準進行比較。如果溶質分子相同,也可以質量分數比較。能夠通過滲透作用吸水的細胞一定是一個活細胞。一個成熟的植物細胞是一個滲透系統。驗證通過滲透作用吸水或失水的最佳實例是質壁分離和質壁分離復原的實驗。一次施肥過多引起“燒苗”,是由於土壤溶液的濃度突然增高,導致植物的根細胞吸水發生困難或不能吸水所至。鹽鹼地里大多數農作物不能正常生長的原因之一也是土壤溶液濃度過高造成的。淹制的魚、肉等不易變質,是由於高濃度的鹽溶液使細胞等微生物失水死亡之故。