共找到2條詞條名為乙硼烷的結果 展開
- 化學式為B2H6的無機化合物
- 二硼烷
乙硼烷
化學式為B2H6的無機化合物
乙硼烷是化學式為B2H6的無機化合物,是目前能分離出的最簡單的硼烷。乙硼烷在室溫為無色氣體,可以與空氣形成爆炸性混合物,並且在潮濕空氣中自燃。用於製取純硼或合成其他硼烷和含硼與氮、磷、砷鍵等地化合物的原料。常作有機反應還原劑、燃料添加劑和p型半導體材料的摻雜劑。
國標編號: 21049
蒸汽壓: 29.86kPa/-112℃
穩定性:穩定
危險標記: 4(易燃氣體)
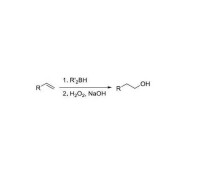
化學性質:缺電子體,有強親電性,可以與乙烯反應制乙醇,產物為反馬氏產物。
乙硼烷離解
乙硼烷(分子式:B2H6)又稱硼乙烷、二硼烷,為無機化合物,是目前能分離出的最簡單的硼烷。在常溫常壓下為具有令人厭惡難聞窒息臭(維生素B味)的無色氣體。易溶於二硫化碳、乙烷、戊烷、乙醚等。很不穩定,具有較高的化學活性,容易與各種無機分子和有機分子起反應。這不僅是因為乙硼烷生成熱為正值(即所謂吸熱化合物),還由於硼對氟、氧、氮、磷等電負性強的元素有很大的親合力。乙硼烷商品通常都用氮、氬、氦或氫氣稀釋。空氣中能自燃,但是在室溫乾燥狀態下一般不燃燒,但只要與潮濕空氣接觸,即使在低溫也能發生爆炸性燃燒,發生綠色火焰,生成氧化硼和水,並放出大量熱。與水作用,分解為硼酸和氫。乙硼烷的熱分解可用來在金屬和陶瓷表面塗敷硼層,有硬度高、抗氧化和耐腐蝕等特性。
乙硼烷在室溫能緩慢分解成氫和高級硼烷。溫度越高越不穩定,分解加速。分解產物也隨溫度高低而變化,到500℃時完全分解成氫和硼。
乙硼烷分子具有D2h點群。兩個硼原子各用兩個sp2雜化軌道與兩個氫原子的1s軌道重疊形成B-Hσ鍵的同時,每個硼原子又用第三個sp2雜化軌道和餘下的一個p軌道組合成兩個軌道Φ,分別位於平面上下。兩個軌道分別與兩個氫原子的1s軌道成兩個垂直於平面的三中心兩電子BHB鍵,正好用上餘下的4個價電子。因此乙硼烷分子不能自由旋轉。
用質子進行陽離子取代:MnB+3H+→1/2B2H6+Mn3+
用單質氫進行氫化:BCl3+3H2→1/2B2H6+3HClR3B+3H2→1/2B2H6+3RH
用金屬氫化物和複合氫化物進行H-取代:2BF3+6NaH→B2H6+6NaF4BCl3+3LiAlH4→2B2H6+3LiAlCl43LiBH4+(C2H5)2O.BF3-(C2H5)2O→2B2H6+3LiF+(C2H5)2O(純度90-95%)3NaBH4+4BF3-二甘醚→2B2H6+3NaBF4
通過質子遷移或電解,從BH4-離子中脫去H-:KBH4+H+-無水酸→1/2B2H6+K++H2LiBH4-電解→Li+1/2B2H6+1/2H2NaBH4+H2PO3F-真空→1/2B2H6+NaHPO3F+H2(產率79%)
高級硼烷熱解:B4H10-△→B2H6+高級硼烷和聚合物B4H10+B5H11-△→2B2H6+B5H9
通過配位使高級硼烷降解:B4H10+2(CH3)2O→(CH3)2O.BH3+(CH3)2O.B3H7(CH3)2O.BH3→1/2B2H6+(CH3)2O
用硼氫化鈉還原氯化亞汞:2NaBH4+Hg2Cl2-二甘醚→B2H6+H2+2NaCl+2Hg
在乙醚或四氫呋喃溶液中的下列反應:8BF3+6LiH→B2H6+6LiBF42BF3+6NaH→B2H6+6NaF4BCl2+3LiAlH4—→2B2H6+3AlCl3+3LiCl
金屬硼氫化物的分解。2NaBH4+2HCl—→B2H6+2NaCl+2H2
硼酸或無水硼酸的還原。2B(OH)3+3Al+3H2—→B2H6+2Al(OH)3
● ● 該產品可由硼氫化鈉與H2SO4反應生成,再經純化、液化製得。
● ● 2.用四氫硼酸鉀及磷酸製備。乙硼烷的製備裝置如圖XIII-2,在一個500mL的雙口燒瓶中,放入一個高效磁性攪拌棒,一個口安裝肘形管加料,另一個口連接與真空系統連接的四個串聯的U形管捕集器,用以從中取出反應生成物。為了觀察反應期間的氣體壓力,最好安裝水銀壓力計。將30mL磷酸(85%)放入容器內,1.6g(0.0297mol)新製備的不含碳酸根離子的KBH4放進加料管中。然後,將反應容器抽真空排氣30min后,將最靠近反應容器的捕集器冷卻到-78℃(用乾冰丙酮冷卻),其餘三個捕集器冷卻到-196℃(液氮冷卻)。仔細地旋轉加料管並輕輕敲叩,使粉末狀KBH4撒落在激烈攪動著的磷酸液面上,這時開始生成乙硼烷,為使泡沫少、產量高,必須十分緩慢地加入KBH4(將全部KBH4加完,需用1.5h),反應系統內的壓力最好不要超過667Pa(5mmHg),泡沫層厚度不超過2.5cm。KBH4加完后,再繼續排氣15~30min,使乙硼烷完全排出。在-78℃的捕集器中冷凝下來的主要是水,也還有痕量乙硼烷存在,可棄掉。對-196℃的捕集器中冷凝的乙硼烷,可通過在-1116℃的捕集器(二硫化碳漿冷卻)蒸發,在-196℃捕集器中冷凝收集進行提純。用這個反應可以製得6~7mmol的乙硼烷。可將這個反應的規模放大,但不得超過3倍。
● ● 注意!製備和使用硼烷,有機硼化物或其溶液應特別注意安全。應在通風櫥內並在氮氣或氫氣中中進行操作。儀器要乾燥,溶劑和試劑不能含水。尾氣排放前,應先通過能與硼烷反應的物質(丙酮等)以除去可能逸出的硼烷氣體。需用較大量的二硼烷,並將其直接通入反應混合物中時,可用此製備法。兩個三頸燒瓶分別作二硼烷發生瓶和接收瓶(下一步反應的反應瓶),都放入電磁攪拌棒。發生瓶中加入1.9摩爾三氟化硼乙醚配合物,中頸安裝盛有950毫升濃度為1摩爾的氫化硼鈉在二甘醇二甲醚的溶液的恆壓漏斗,漏斗頂接上帶有汞計泡器的氮氣導入管,側頸用聚四氟乙烯管與洗氣瓶連接。洗氣瓶盛氫化硼鈉的二甘醇二甲醚溶液以除去三氟化硼蒸氣。洗氣瓶與盛有500毫升四氫映喃〔無水無過氧化物)的接收瓶的導入管連接。管端熔合有砂晶元,使氣體分散,易於吸收。接收瓶一頸用橡皮帽蓋緊(可以用注射針筒取樣),中頸裝迴流冷凝器,頂端通到另一汞計泡器,汞上加一層丙酮,以除去可能逸出的二硼烷。將接收瓶置冰浴中,通入氮氣沖洗,慢慢滴加氫化硼鈉溶液到三氟化硼溶液中,生成的二硼烷被四氫映喃吸收。氫化硼鈉加完后,維持約1小時以使吸收完全。若接收瓶中事先加入待反應的底物,則可直接進行下一步反應。經分析,所得二硼烷四氫映喃溶液的濃度約為1摩爾/升。該溶液在0℃和氮氣下可保存幾星期。
● ● 注意了本法不適合於在大氣壓下在流動系統中製備。必須在真空管路中或在無氧反應體系中進行操作。需用小量二硼烷時可採用此製備法。在500毫升二頸燒瓶中加入30毫升85%磷酸和電磁攪拌棒。必須通過磨口活塞與真空管路連接,使揮發性的反應產物經四個串連的U形捕集器加以分離,考塞內塞有一團玻璃毛以防止痕量的非揮發物質被夾帶到真空管路中。另一頸與盛有1.6克〔0.0297摩爾)新開瓶並不含碳酸鹽的氫化硼鉀的加料側管連接。將反應器抽空0.5小時后,將緊鄰反應器的一隻捕集器冷凍到-78℃(乾冰一丙酮),J仁餘三隻捕集器則冷凍到一196℃(液氮)。小心地轉動並輕敲加料側管慢慢將粉末狀氫化硼鉀加入迅速攪拌著的磷酸上面,立即放出氣體併產生泡沫。為了提高產率,減少起泡現象,應小心避免突然加入大量的氫化硼鉀。慢慢地在1-1.5小時內將氫化硼鉀加完,使反應系統內的壓力不超過5毫米,泡沫層厚度不超過2.5毫米,乖續抽空15-30分鐘后可拆卸反應系統。在一78℃捕集器中凝集物主要是水和痕量的二硼烷,可以廢棄。凝集在一196℃捕集器中的二硼烷,可以通過另一個一116℃的捕集器(二硫化碳凍膏)進入一個一196℃的捕集器而進行提純。凝集在一111.6℃捕集器中的痕量物質可以棄去,總計可獲得6~7毫摩爾的二硼烷。二硼烷長期存放后,可用下法除去其中所含分解產物;將二硼烷冷凍至一196℃,抽空,然後蒸餾,使二硼烷通過一130℃捕巢器(正戊烷凍膏)而進入一個一196℃捕集器。
健康危害:急性中毒時一般出現胸部緊束感、咳嗽、呼吸困難、前胸痛、噁心、嘔吐等癥狀。有時,這些癥狀在中毒后24小時才呈現出來。長期接觸低濃度乙硼烷時,除了呼吸系統輕度刺激癥狀之外,還會出現頭痛、喪失嗅覺、暈眩、嗜眠、神經官能症、驚厥、肌弛緩、震顫、痙攣、昏迷、腳部緊張感、寒冷等癥狀。吸入的患者,應立即轉移至通風良好的無污染區,安置休息並蓋毛毯等保暖。如果呼吸微弱或停止,應馬上進行輸氧或人工呼吸,同時,速叫醫生來診治。當眼睛或皮膚觸傷時,立即用水沖洗患處,至少要衝洗15分鐘。也可用3%氨水或1%~5%三乙醇胺(三羥基代三乙胺)沖洗受傷的皮膚,然後進一步求醫診治。
亞急性和慢性毒性:狗及大鼠長期暴露於1.1~2.2mg/m3濃度下無死亡;在5.6mg/m3濃度下,每天吸入6小時,動物不久開始發生死亡。
危險特性:極易燃,與空氣混合能形成爆炸性混合物。遇熱源和明火有燃燒爆炸的危險。在室溫下遇潮濕空氣能自燃。與氟、氯、溴等鹵素會劇烈反應。並能與氟氯烷滅火劑猛烈反應。與水或水蒸氣反應會釋出易燃的氫氣,並且會腐蝕橡膠和某些塑料。
燃燒(分解)產物:氧化硼。對粘膜有較強的刺激作用,吸入後會很快侵襲至肺部並引起肺水腫和出血。長時間接觸會損傷肝和腎。接觸皮膚能引起嚴重的局部炎症並能導致皮炎。乙硼烷還能使嗅覺器官失靈。其毒性比光氣和HCN還大。
1.在室溫乾燥狀態下一般不燃燒,與潮濕空氣接觸,即使在低溫也能發生爆炸性燃燒,產生綠色火焰。在室溫下也能分解,分解產物隨溫度高低而變化,到500℃時完全分解成氫和硼。能與氨、甲醇、乙醛、乙醚及鋰、鈉、鉀、鈣、鋁等金屬激烈反應。
2.遇水分解變成氫及硼酸。蒸氣壓(3.00×104±133)Pa(-111.6℃)。紅外光譜帶3670(w)、2625(s)、2558(s)、2353(w)、1853(m)、1602(vs)、1197(s)、1178(s)、1154(s)。可以儲存,但長期存放時就轉變為氫及高級硼烷。
3.穩定性:穩定
4.禁配物:強氧化劑、鹼、氟、氯、溴等鹵素、水、四氯化碳
5.避免接觸的條件:潮濕空氣
6.聚合危害:不聚合
迅速撤離泄漏污染區人員至上風處,並立即進行隔離,小泄漏時隔離300米,大泄漏時隔離450米,嚴格限制出入。切斷火源。建議應急處理人員戴自給正壓式呼吸器,穿防毒服。從上風處進入現場。儘可能切斷泄漏源。合理通風,加速擴散。噴霧狀水稀釋。漏氣容器要妥善處理,修復、檢驗后再用。
吸入:迅速脫離現場至空氣新鮮處。保持呼吸道通暢。如呼吸困難,給輸氧。如呼吸停止,立即進行人工呼吸。就醫。
滅火方法:切斷氣源。若不能立即切斷氣源,則不允許熄滅正在燃燒的氣體。噴水冷卻容器,可能的話將容器從火場移至空曠處。滅火劑:二氧化碳。禁用水柱和泡沫。
(1)用水或鹼溶液吸收。
(2)在嚴格控制下燃燒。
(3)把燃燒產物B2O3用活性碳吸附或用水吸收。
(4)用專用吸附劑吸附。
(5)用惰性氣體稀釋後排放。
庫房通風低溫乾燥;輕裝輕卸
滅火劑
霧狀水
職業標準
TWA0.1毫克/立方米;STEL0.3毫克/立方米
1.氣體鋼瓶要存放在通風良好的室外或強制通風的室內,遠離火源,並且使其溫度始終保持在20℃以下。不可與鹵素、氧化劑、氧及水接近。乙硼烷一旦燃燒,一般很難撲滅,最有效的處理方法是及時阻止硼烷泄露,並防止火災向周圍蔓延。
2.儲存注意事項[20] 儲存於陰涼、通風良好的專用庫房內,實行“雙人收發、雙人保管”制度。遠離火種、熱源。庫溫不超過25℃,相對濕度不超過75%。應與氧化劑、鹼類、鹵素、食用化學品分開存放,切忌混儲。採用防爆型照明、通風設施。禁止使用易產生火花的機械設備和工具。儲區應備有泄漏應急處理設備。
用作高純度硼單晶及十硼氫的原料,也用作半導體工業的摻雜源
● ● 用作高純度硼單晶及十硼氫的原料,也用作半導體工業的摻雜源。
2.乙硼烷是半導體製造中用作硅材料的p型摻雜源,在半導體工業中得到廣泛應用,用於半導體生產,硅和鍺的外延生長、鈍化、擴散和離子注入。隨著大規模集成電路集成度的提高,對B2H6純度的要求也越來越高。還可用作火箭和導彈的高能燃料。
3.可用作火箭和導彈的高能燃料,也可用於半導體生產,硅和鍺的外延生長、鈍化、擴散和離子注入。用於製藥、金屬焊接和有機合成等領域。
4.用作聚合催化劑、火箭和導彈的高能燃料,也用於有機合成。
