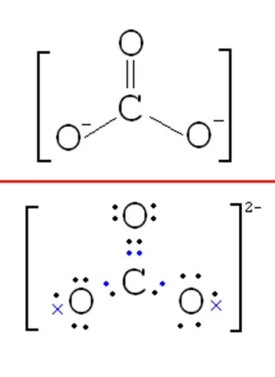
碳酸根
一種弱酸根
碳酸根的化學式為CO3(離子CO3),相對分子質量60。雖然含碳,但含碳酸根的物質卻多是無機物。碳酸根是一種弱酸根,在水中很容易水解產生碳酸氫根離子和氫氧根離子,從而使水偏向鹼性。
碳酸根,化學式為CO3,呈-2價,其中碳為最高價+4價,氧為-2價。

碳酸根
碳酸根雖然含碳,但含碳酸根的物質多是無機物。碳酸根是一種弱酸根,在水中電離后很容易和氫離子結合產生碳酸氫根離子和氫氧根離子,從而使水偏向弱鹼性。
離子結構
C原子以sp2雜化軌道成鍵、離子中存在3個σ鍵,由C的3個sp2雜化軌道和三個O原子的2p軌道結合,離子為正三角形,而C中與分子平面垂直的另一個p軌道會與3個O原子中與分子平面垂直的p軌道結合成大π鍵,再加上所帶兩電荷,大π鍵中共有6個電子,從而形成π(6,4)鍵。碳酸根的離子半徑小於次氯酸根,但是碳酸根可極化性也很強,能被極化。
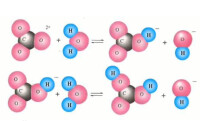
碳酸根
碳酸根對於調節人體酸鹼平衡、維持人體內環境穩態有重要作用。碳酸鈉和碳酸氫鈉混合而成的鹼性緩衝也,可以維持人體胃pH相對穩定;碳酸氫鈉為弱鹼性物質,當胃酸(主要是鹽酸)過多時,碳酸鈉與鹽酸反應生成碳酸氫鈉,可以增高pH;當胃酸較少,胃環境pH較高時,碳酸氫鈉又可與強鹼性物質反應生成碳酸鈉,碳酸鈉呈弱鹼性,因此可以降低胃環境的pH,達到雙向調節作用,以保持胃環境pH相對穩定。
因為碳酸根離子易與氫離子結合生成二氧化碳氣體,所以可用酸來檢驗。
實驗室一般用稀鹽酸與澄清石灰水來檢驗。
取樣,加入鹽酸生成的氣體通入澄清的石灰水中。
加入鹽酸有無色無味的氣體生成,將生成的氣體通入澄清的石灰水中有白色沉澱生成。
說明含有碳酸根離子或者碳酸氫根離子或亞硫酸根離子或亞硫酸氫根離子。
另取試樣,加入氯化鈣有沉澱生成,即可證明含有碳酸根離子。
其實也可以直接加入氯化鈣產生白色沉澱,加入稀鹽酸,產生無色無味的氣體,通入澄清石灰水中出現白色沉澱,即可證明。
可以觀察到有無色無味的氣體生成,且該氣體通入澄清的石灰水中有淺黃色沉澱生成的現象。則說明該物質中含有碳酸根離子或者碳酸氫根離子或亞硫酸根離子或亞硫酸氫根離子。另取試樣,加入氯化鈣有沉澱生成,即可證明含有碳酸根離子。其實也可以直接加入氯化鈣產生淺黃色沉澱,加入稀鹽酸,產生無色無味的氣體,通入澄清石灰水中出現淺黃色沉澱,即可證明。
目前(2010年)油田主要用化學滴定法測定碳酸根和碳酸氫根,可以鹽酸為滴定劑,用電導滴定法快速測定工業水中HCO3含量。因為水中電導率會隨著鹽酸滴入而發生變化,所以通過測電導率值可繪製出滴定曲線,確定滴定終點,進而求出HCO3-的含量。此方法簡單快速、結果準確、精密度高,滴定終點極易確定,適合於水質檢驗、環境監測和工業生產監控。滴定法是比較傳統且非常成熟的一種測定方法,能夠簡單快捷地測得水樣中HCO3-的含量,但主要適合於實驗室臨時操作。
離子選擇電極是20世紀60年代發展起來的一種新的電化學分析工具,設備簡單、測量方便、易於自動化、分析準確、快捷,在國外已廣泛應用於工業分析。採用雙電極法來測定碳酸根和碳酸氫根,電極為測氫離子濃度的離子選擇電極和502型二氧化碳氣敏電極,並把整個測試系統設計成測量HCO3和CO3的自動化儀錶,該系統以單片機為核心進行控制和信號處理,採用高輸入阻抗的測量電路與高內阻的CO2相匹配,信號放大電路實現信號放大,溫度補償電路以保證溶液溫度的穩定。整個測試過程只需十多分鐘,並可長時間連續工作,但對外界環境的穩定性和電極測量的重現性要求較高。實現測量的準確性、快速性,並實現儀器的小型化、智能化,可方便地用於在線測定。
有學者提出了基於氣態進樣技術的電感耦合等離子體原子光譜法對水樣中 HCO3和 CO3含量進行測定。將試樣與一定量的稀鹽酸反應生成的CO2以氣態進樣方式導入儀器進行檢測,測定CO2氣體中碳含量的分析譜線波長為247.86nm。實驗將同一份試樣溶液與不同體積的0.01mol/L 鹽酸溶液反應,繪製出CO2的釋放量與相應的鹽酸消耗量(mL)之間的曲線,即可計算出樣品中CO3和HCO3的含量,HCO3和 CO3的檢出限分別為0.21mg/L和0.82mg/L。
概述
1、碳酸是一種弱酸,不穩定,易分解為水和二氧化碳,通常有碳酸生成的化學反應寫成水和二氧化碳的形式。碳酸常用於製作汽水。
常見的碳酸鹽及其用途
碳酸鈣是石灰石和大理石的主要成份,重要的工業原料和建築材料,經常用於工業製取二氧化碳和生石灰,實驗室用碳酸鈣與稀鹽的反應製取二氧化碳。碳酸鈣也常用於補鈣劑中。
碳酸鉀草木灰的主要成分,重要的鉀肥。
碳酸氫鈉俗稱小蘇打,用作食品工作的發酵劑、汽水和冷飲中二氧化碳的發生劑、黃油的保存劑等。
碳酸鹽中有如下幾個沉澱及難溶物,但這些難溶物均溶於酸:碳酸鈣,碳酸鋇。
製革業
製革離不開水,特別是濕操作工段,製革用水的硬度對成品革的質量影響非常大。如果製革用水的硬度偏高,高於飲用水允許的最高硬度,則經濕操作工段后出現松面、炸面的革坯往往撕裂強度較低;炸面的革坯身骨扁薄僵硬,塗飾時不吸漿、易掉漿等,因此測定製革用水的碳酸氫根(HCO3)和碳酸根(CO3)含量,對製革生產具有重要的實際意義。
油田鑽井
HCO3和 CO3是原油分離水中的主要的陰離子,測定油田地層水中的 HCO3和 CO3的濃度有助於我們了解地層水的種類、硬度等指標。隨著鑽探領域的擴大,在很多區塊鑽井過程中會遇到 CO3和 HCO3離子對鑽井液造成污染的問題,使常用鑽井液處理劑,尤其是稀釋劑不能有效地發揮作用,致使鑽井液黏度和切力急劇增大,處理困難。按一般的處理方法,加人鐵鉻鹽鹼液或者磺化單寧鹼液不但不能實現降粘效果,反而會出現越加稀釋劑,鑽井液的粘切會越高的反常現象。如果對 CO3離子造成的污染認識不足,就會給鑽井液性能的控制帶來很大困難,影響鑽井作業的正常進行。測定油田地層水中的碳酸根和碳酸氫根的含量有助於了解地層水的種類、硬度等指標,同時可以監測它們在管路腐蝕中所起的作用。
農田土壤
CO3是土壤可溶鹽分的組份之一,土壤所含的可溶鹽分達一定數量后,會直接影響作物的發芽和正常生長。就鹽分組成而言,蘇打鹽分(碳酸鈉、碳酸氫鈉)對作物的危害最大。所以測土壤的CO3根離子的含量十分重要。石灰性土壤地區灌溉水中 HCO3濃度較高時對作物生長十分不利,原因之一是 HCO3能減少根系吸收的養分由莖向葉片和生殖器官的轉移,對P、Ca、Mg、Fe、Mn的影響極大;石灰性土壤地區的水稻田中發生的缺Zn現象,通常是水中存在HCO3的緣故。過多的HCO3既影響蛋白質合成和呼吸作用,也降低養分的吸收量,導致不少植物發生失綠。因此,測量生活用水、河水、灌溉水等與植物生存密切相關的水源中HCO3的含量,對研究植物的生存狀況有重要意義。
人體pH調節
血清HCO3是血漿中重要的緩衝體系,也是判斷體內酸鹼失衡的重要指標,對診斷和治療呼吸性酸中毒和慢性呼吸性鹼中毒起著非常重要的作用。因此測定血漿中HCO3含量具有極為重要的臨床意義:HCO3主要由碳酸氫鹽解離而來。當其它的陰離子缺乏時,為保持與陽離子含量的平衡,HCO3就會增多以代替其它減少的陰離子含量。因此,HCO3對維持體內陰陽離子平衡具有重要意義。體內HCO3實際含量的增減可直接影響pH 的穩定。當體內出現代謝性酸鹼失衡時,由於緩衝作用,HCO3濃度會在體內較多的固定酸或固定鹼影響下隨之改變。當出現代謝性酸中毒時,血漿中HCO3含量會下降;而出現代謝性鹼中毒時,血漿中HCO3含量則會增加。因此血漿中的HCO3含量是體內代謝性酸鹼失衡的一個重要指標。