次氟酸
次氟酸
次氟酸是一種無機物,化學式為HOF,淡黃色液體或白色固體,遇水分解,但在乙腈中可以較為穩定地存在,次氟酸是很好的氧化劑,可以和很多難以被氧化的有機物反應,且反應條件溫和。
通常所認為的次氟酸是指化學式為HOF的化合物。實際上,該名稱並不準確,由於電負性的緣故,HOF中的氟仍為-1價,而氧則為0價,故認為其名稱應為“氟氧酸”。它可由氟氣緩緩通過細冰表面氧化得到,是唯一可分離出固態的“次鹵酸”,具爆炸性,會分解為氟化氫氣體和氧氣。1971年由美國科學家斯圖爾傑和阿佩里曼首次製得。次氟酸是很好的氧化劑,可以和很多難以被氧化的有機物反應,且反應條件溫和。
在1971年,美國的兩位科學家成功地合成了HOF,動搖了長期以來人們認為氟的含氧酸不存在的觀點。於是大量有關HOF的文章及試題紛至沓來,有的高校無機教材中也對HOF做了介紹,它們都冠HOF為次氟酸,甚至連一些化合物含有-OF基團的也稱之為次氟酸鹽。
在一般的含氧酸當中,氧元素的氧化數為-2,成酸元素的氧化數均為正值,比如亞磷酸(H3PO3)、次磷酸(H3PO2)中,磷的氧化數分別為+3、+1;而在HOF中,由於F非金屬性較之O更強,所以在HOF分子中,O、F之間共用電子對偏向於F原子,因此F的氧化數為-1,而O的氧化數為0,所以可以說,HOF不是普遍意義上的含氧酸,而應另屬其它類,故其命名也應有別於一般含氧酸的命名,而不能因為HOF的分子式,電子式與次氯酸類似,便不去考察含氧酸的命名原則及物質的性質,靠直覺將其稱為次氟酸。
1971年美國的斯圖爾傑和阿佩里曼在0℃以下,用被氮氣稀釋的氟氣在細冰上緩慢通過製得。
F2 + H2O → HOF + HF
該物質極為不穩定,容易爆炸分解。氟氧酸在室溫下便會分解,帶有刺激性的氣味,並且有劇毒。
2HOF → 2HF + O2
在氟氧酸中,氧的化合價為0價,生成的氧氣的化合價也為0價,氫和氧的化合價前後也沒變,但是氟氧酸的分解反應屬於氧化還原反應。原因是氧原子的電子發生了偏移。在氟氧酸中,O-F鍵電子對偏向F,而在氧氣中,O-O鍵電子對沒有偏向。所以HOF分解成O2時,電子對有偏移。(根據氧化還原反應的定義:電子轉移或者電子發生偏移的反應)
根據X射線晶體學的研究,固態氟氧酸分子為角形,鍵角為101°,O-F和O-H距離分別為1.442A和0.78A,分子間有O-H…O鍵連成的鏈。
次氟酸
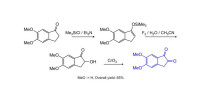
化合物與1,2-茚二酮都可用於檢驗指紋
次氟酸還可與富電子的叔碳反應
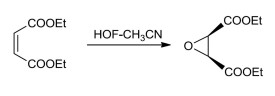
製取α-羥基羰基化合物對α-羥基羰基化合物的研究一直吸引著有機化學家的興趣。用次氟酸作氧化劑氧化烯醇醚(通常為三甲硅基)製得α-羥基羰基化合物的方法,避免了其他方法殘留的重金屬廢料,減少了對環境的污染。一般認為該反應中次氟酸先對烯醇的雙鍵進行環氧化,然後發生氟離子和水分子對環碳原子的親核進攻,引入羥基,三元環打開。而後氟/羥基及硅基離去,恢復羰基,得到α-羥基羰基化合物。
次氟酸在室溫下與苯乙酮的三甲硅基烯醇醚反應時,反應在5-10分鐘內完成,產物為α-羥基苯乙酮,產率高於90%。次氟酸還可與富電子的叔碳反應,生成構型保持的叔醇。
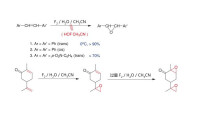
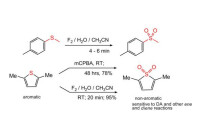
氧化硫醚為碸
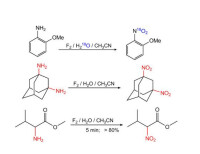
無論脂肪族還是芳香族的胺類都可以被次氟酸氧化為硝基化合物,通常反應很快且產率不俗。所有的氨基酸都可以通過此反應被轉化為硝基酸,下圖中,纈氨酸的甲基酯與次氟酸乙腈溶液反應,成功以超過80%的產率得到了2-硝基-3-甲基丁酸甲酯。
此外,次氟酸可將膦和胺分別氧化為氧化膦和氧化胺。它與鄰菲羅啉反應成功得到了1,10-二氧化鄰菲羅啉。