羥基
常見的極性基團
羥基化學式為-OH,是一種常見的極性基團。羥基主要分為醇羥基,酚羥基等。
羥基與水有某些相似的性質,羥基是典型的極性基團,與水可形成氫鍵,在無機化合物水溶液中以帶負電荷的離子形式存在(OH-),稱為氫氧根。
羥基
羥基可以分為兩類:醇羥基和酚羥基
醇羥基與伯、仲或叔碳原子相連為伯醇、仲醇或叔醇,按醇分子中所含羥基數目可分為一羥醇(一元醇)和多羥醇(多元醇),多元羥醇中的羥基在相鄰碳原子上時,叫做鄰醇羥基,具有與一羥醇相似的性質,也有一定的特性。
醇羥基的酸性按伯、仲、叔醇的順序減弱,因此,在-OH鍵斷裂的反應中,其反應速度依次下降,在R—OH鍵斷裂反應中,叔醇的反應速度比伯、仲醇快,在控制下,伯醇氧化成醛(但用較強的氧化劑會使生成的醛轉化成羧酸);仲醇氧化為酮(通常穩定.不會進一步氧化);一般叔醇不易被氧化。
酚羥基(-OH)為酚類的官能團。在C—O—H結構中,氧原子含有孤對p電子,p電子云和苯環的大π電子云從側面有所重疊,使氧原子上的p電子云向苯環轉移,使氫氧原子間的電子云向氧原子方向轉移,結果C—O鍵更牢固,O—H鍵更易斷裂。羥基中氫原子較易電離,使苯酚顯示一定的酸性,能和強鹼發生中和反應(乙醇則不能)。
在有機物中,在有機化學的系統命名中,在簡單烴基後跟著羥基的稱作醇,而糖類多為多羥基醛或酮。
羥基直接連在苯環上的稱作酚。
醇羥基不體現出酸性(阿倫尼烏斯酸鹼理論中),酚羥基和羧羥基體現出弱酸性(因而苯酚可與鈉反應),酚羥基酸性比碳酸弱,強於碳酸氫根;羧羥基(羧基),比碳酸強。
常見化合物的乙醇(俗名:酒精)為非電解質,不顯酸性。乙醇中只有羥基上的氫可以電離,因而與鈉反應時1mol乙醇只產生0.5mol氫氣。
在無機物中,通常含有氫氧根的物質為鹼或其它的鹼式鹽。
含氫氧根的物質溶解於水會電離出氫氧根離子,因此含氫氧根的物質水溶液多體現鹼性,但是氫氧根是離子,帶負電,與羥基有著本質區別,只有極少數弱鹼(共價化合物)自帶羥基。
1.還原性,可被氧化成醛或酮或羧酸。
3.可發生消去反應,如乙醇脫水生成乙烯。
4.可發生置換反應,醇羥基與金屬鈉反應置換了羥基中的氫原子,生成了氫氣。
5.可發生取代反應,分子間脫水成醚(R-O-R”)R與R“為烴基。
在很多情況下,由於在示性式中,羥基和氫氧根的寫法相同,因此很容易和氫氧根混淆。
區別:1、電子數不同:氫氧根為十電子,羥基為九電子;2、二者電子式不同:氫氧根的氧原子有8個電子包圍,羥基的氧原子外有7個電子包圍。
雖然氫氧根和羥基均為原子團,但羥基為官能團,而氫氧根為離子。而且含氫氧根的物質在水溶液中呈鹼性,而含羥基的物質的水溶液則多呈偏酸性。氫氧根和羥基在有機化學上的共性是親核性。
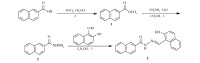
羥基是有機化學中最常見的官能團之一,無論是醇羥基還是酚羥基均容易被多種氧化劑所氧化。因此在多官能團化合物的合成過程中,羥基或者部分羥基需要先被保護,阻止它參與反應,在適當的步驟中再被轉化。