化學變化
化學變化
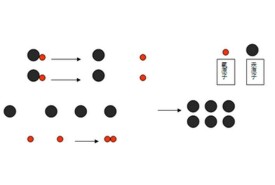
化學變化是指相互接觸的分子間發生原子或電子的轉換或轉移,生成新的分子並伴有能量的變化的過程,其實質是舊鍵的斷裂和新鍵的生成。
化學變化過程中總伴隨著物理變化。在化學變化過程中通常有發光、放熱、也有吸熱現象等。按照原子碰撞理論,分子間發生化學變化是通過碰撞完成的,要完成碰撞發生反應的分子需滿足兩個條件:(1)具有足夠的能量;(2)正確的取向。因為反應需克服一定的分子能壘,所以須具有較高的能量來克服分子能壘。兩個相碰撞的分子須有正確的取向才能發生舊鍵斷裂。
化學變化(chemical change)在生產和生活中普遍存在。產生了新物質的變化是化學變化。如鐵的生鏽、節日的焰火、酸鹼中和,鎂條的燃燒等等。宏觀上可以看到各種化學變化都產生了新物質,這是化學變化的特徵。總結:有新物質產生的變化即為化學變化。
化學變化種類較多,可根據不同方面將其分類。
從反應物和生成物的種類及數量進行劃分,可以把化學變化分為四種基本反應類型:化合反應、分解反應、置換反應和複分解反應。
(1)化合反應:;
(2)分解反應:;
(3)置換反應:;
(4)複分解反應:。
氧化反應:
還原反應:
氧化劑(反應物)→得電子或共用電子對偏向→化合價降低→被還原→發生還原反應→生成還原產物。
氧化-還原反應(oxidation-reduction reaction,,也作redox reaction)是化學反應前後,元素的氧化數有變化的一類反應。氧化還原反應的實質是電子的得失或共用電子對的偏移。氧化還原反應是化學反應中的三大基本反應之一,另外兩個為(路易斯)酸鹼反應與自由基反應。自然界中的燃燒、呼吸作用、光合作用、生產生活中的化學電池、金屬冶鍊、火箭發射等等都與氧化還原反應息息相關。研究氧化還原反應,對人類的進步具有極其重要的意義。
若從反應中是否有離子參加的角度看,可分為離子反應和非離子反應。離子反應的本質是某些離子濃度發生改變。
離子反應的本質是某些離子濃度發生改變。常見離子反應多在水溶液中進行。有離子參加的化學反應,根據反應原理,離子反應可分為複分解、鹽類水解、氧化還原、絡合4個類型;也可根據參加反應的微粒,分為離子間、離子與分子間、離子與原子間的反應等。極濃的電解質跟固態物質反應時,應根據反應的本質來確定是否屬於離子反應。例如,濃硫酸跟銅反應時,表現的是硫酸分子的氧化性,故不屬於離子反應;濃硫酸跟固體亞硫酸鈉反應時,實際上是氫離子跟亞硫酸根離子間的作用,屬於離子反應。此外,離子化合物在熔融狀態也能發生離子反應。
在化學反應中,反應物總能量大於生成物總能量的反應叫做放熱反應。包括燃燒、中和、金屬氧化、鋁熱反應、較活潑的金屬與酸反應、由不穩定物質變為穩定物質的反應。
吸熱反應指的就是化學上把最終表現為吸收熱量的化學反應。吸熱反應中反應物的總能量低於生成物的總能量。吸熱反應的逆反應一定是放熱反應。
從微觀上可以理解化學變化的實質:化學反應前後原子的種類、個數沒有變化,僅僅是原子與原子之間的結合方式發生了改變,原子是化學變化的最小微粒。例如對於分子構成的物質來說,就是原子重新組合成新物質的分子。物質的化學性質需要通過物質發生化學變化才能表現出來,因此可以利用使物質發生化學反應的方法來研究物質的化學性質,製取新的物質。
化學變化,具有特徵;
新的物質,一定生成;
放熱發光,顏色改變;
放出氣體,生成沉澱;
化變同時,物變發生。