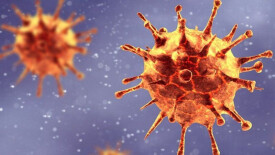
刺突
病毒包膜的糖蛋白
刺突即病毒包膜的糖蛋白。有些病毒除了具有包膜外,還有包膜突起。病毒包膜突起的化學本質大多為糖蛋白,其功能各不相同。有的是病毒粒子的吸附蛋白.與病毒的吸附有關;有的是病毒的融合蛋白,它可以促進病毒包膜與細胞膜融合,與病毒的侵入有關。
在包膜(envelope)表面有病毒膜蛋白質規則地排列著,似如形成某種形態學的單位,稱此為刺突。但是也還沒有象殼微粒(capsomere)那樣的作為已經搞清楚了的構造物賦以應有的定義,實際上可明確顯示刺突的電子顯微鏡照片也並不多。
 2張
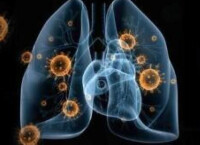
2張刺突
刺突有些病毒粒子表面,尤其是在有囊膜的病毒粒子表面具有突起物,稱刺突,也稱囊膜突起。囊膜對衣殼有保護作用,並與病毒吸附宿主細胞有關。有些病毒囊膜表面具有呈放射排列的突起,稱為纖突(又稱囊膜粒或刺突),放射狀排列的糖蛋白刺突(囊膜突起)。這些刺突有的是病毒的凝血素(能凝集紅細胞),用於起動病毒感染過程,具有誘生免疫保護作用以及中和抗體的能力。有的具有神經氨酸酶的活力,可促使病毒從宿主細胞上釋放。
(1)2012年以來中東呼吸綜合症病毒流行以來刺突蛋白氨基酸序列呈現出一定的地域性特點,其中來自法國的人源刺突蛋白序列之間的同源性為99.70%~100%,來自阿拉伯聯合大公國的刺突蛋白序列之間的同源性為99.63%~100%,來自2014年阿拉伯聯合大公國的刺突蛋白序列在同一進化樹分枝上。
(2)來自沙烏地阿拉伯的人源刺突蛋白序列未表現出時間上的差異,2013、2014和2015年分離株刺突蛋白的同源性為99.63%~100%,但是來自沙烏地阿拉伯的刺突蛋白與來自法國和阿拉伯聯合大公國的刺突蛋白區別明顯;在進化樹上,來自沙烏地阿拉伯的呼吸綜合症病毒刺突蛋白氨基酸序列並沒有完全聚在相同的進化分枝上,而是分散在相對集中的不同分枝上。
(3)2014年3、5、6月來自美國的3條刺突蛋白序列之間的同源性為99.70%~99.85%低於和來自沙烏地阿拉伯的人源刺突蛋白之間的同源性(99.70%~100%)。
(4)不同宿主間來源株的刺突蛋白序列之間無明顯區別,其中單峰駝來源的刺突蛋白序列間的同源性為98.15%~100%,其與人源刺突蛋白序列之間的同源性為99.56%~100%,單峰駝源的刺突蛋白序列在進化樹上分散在沙烏地阿拉伯人源刺突蛋白分枝上。
(5)英格蘭分離株刺突蛋白之間的同源性為99.70%~99.933%,低於和分離較晚的幾條源於沙烏地阿拉伯的人源刺突蛋白之間的同源性(100%),而與分離較早的來自沙烏地阿拉伯的刺突蛋白氨基酸序列的同源性較低(99.78%~99.93%),且分散在不同的分枝上。
(6)來源於韓國分離株的一刺突蛋白與其他刺突蛋白之間的同源性最高為99.78%,處於單獨分支上。
(7)來自中國分離株的刺突蛋白序列與來自英格蘭以及沙烏地阿拉伯部分人源刺突蛋白序列同源性為100%。
地區間中東呼吸綜合症病毒刺突蛋白的同源性很高,達98.15%~100%,說明刺突蛋白氨基酸序列非常保守。流行的中東呼吸綜合症冠狀病毒在同一地域內有多種不同的病毒株流行,多地可能同時存在中東呼吸綜合症流行,也同時存在地區間輸入性快速傳播;同一地區不同年份病毒的刺突蛋白變異不明顯,不同宿主間的病毒刺突蛋白序列無顯著差別。
嚴重急性呼吸系統綜合征(severeacuterespiratorysyndrome, SARS),又稱傳染性非典型性肺炎(atypicalpneumonia,簡稱“非典”),是2002年11月爆發流行的一種新的傳染病,該病傳染性強,潛伏期短,進展快,死亡率高,是由嚴重急性呼吸系統綜合征冠狀病毒(SARScoronavirus,SARS-CoV)引起的呼吸系統疾病。自從SARS大規模爆發之後,關於這種新型人類冠狀病毒的各項研究,如病原學、流行病學、病毒基因組結構、病毒蛋白的重組表達、臨床檢測、疫苗的研製、公共衛生管理學等等,也隨之快速開展了起來,並取得了很大的進展。
S蛋白
SARS-CoV的刺突蛋白(spike,S)是Ⅰ型跨膜糖蛋白,也是病毒最大的結構蛋白,由1255個氨基酸殘基組成,包含了病毒的主要抗原決定簇,能夠刺激機體產生中和抗體和介導免疫反應,由球狀的受體結合亞基S1和棒狀的融合亞基S2兩部分組成。近N端的S1和近C端的S2是兩個獨特的功能結構域,決定了冠狀病毒的組織嗜性(受體特異性)和膜融合特性(使病毒進入細胞)。
研究發現,SARS-CoV的S蛋白可以單獨完成包膜病毒顆粒的細胞侵入的全過程,其中包括:(1)識別並結合靶細胞受體;(2)病毒與靶細胞融合,將遺傳物質釋放到胞內。因為S蛋白是病毒識別宿主細胞表面受體――血管緊縮素轉化酶2(angiotensin-convertingenzyme2,ACE2)的關鍵分子,表達S蛋白的細胞可以與表達ACE2的細胞結合併誘導細胞融合。可見S蛋白在病毒入侵機體時的作用是關鍵的。另外,S蛋白暴露於病毒表面,含有大量的抗原決定簇,可以產生針對病毒的保護性抗體。據檢測表明,SARS康復病人的血清中普遍存在著抗刺突蛋白的抗體,同時SARS-CoV的S蛋白也能夠有效地誘導中和抗體的產生。因此S蛋白是進行疫苗和抗體研究的一個比較理想和有效的靶點。
研究表明,位於刺突蛋白N端的S1段(17~672aa)是同受體結合的關鍵部位,也是中和抗體作用的主要作用靶點,考慮到整個Spike蛋白的分子量較大,結構複雜,進行重組表達較為不便,選擇其關鍵的S1段進行研究是一種可行的方法。邵紅偉等選取刺突蛋白的S1段進行抗原表位分析,對其中259~565aa的區段進行了原核重組表達,並對表達產物進行了純化、復性和抗原性檢測。結果發現S1蛋白同陽性對照(滅活病毒)一樣能夠被SARS抗血清所特異性地識別,而正常人的陰性血清則沒有顯示出反應信號,表明重組表達的S1蛋白具有很強的抗原性。S1蛋白259~565aa段是誘導機體免疫反應的重要區域,同時還是病毒識別受體的關鍵區域,他們認為可針對這一區域設計重組疫苗或者製備治療性抗體。李燕等通過生物信息學分析,在原核表達系統中表達了SARS病毒S1蛋白。利用SARS流行前正常人血清和SARS患者恢復期的血清,對純化的重組S1蛋白進行血清學分析。結果發現克隆表達的重組蛋白序列與公布的SARS病毒S1蛋白的序列相同。這表明:獲得的重組S1蛋白具有與天然SARS病毒S1蛋白相同的序列,並具有與之相似的血清學反應性,為研究SARS病毒感染免疫應答的過程及其機制和製備SARS病毒的重組疫苗提供了良好的物質基礎。
S2蛋白研究
有研究發現,S2蛋白雖然不是病毒識別受體的必要結構,但針對S2的抗體也能阻斷SARS病毒感染宿主,而且通過對多個國家和地區的SARS冠狀病毒分離株S蛋白的編碼基因及氨基酸序列進行同源性分析,發現SARS冠狀病毒S蛋白比較保守,變異率低,其中S2比S1更保守,鑒於S2蛋白的保守及其結構特點,S2區現已成為研製保護性疫苗的重要靶位。黃紅平等用利用基因重組的方法,將S2基因2170~3162bp段重組到原核和真核表達載體中,構建S2基因相應的表達載體,在原核系統中誘導表達重組SARS-CoV-S2蛋白,並使用金顆粒包裹DNA疫苗後用基因槍免疫小鼠。結果發現小鼠產生了針對誘導表達的重組SARS-CoV-S2蛋白的特異性抗體。
研究發現,動物源性的SARS相似病毒S蛋白與人源性SARS病毒S蛋白有高度同源性,為SARS病毒的動物起源和人畜共患的可能性提供了新的依據。S1和S2是兩個獨特的功能結構域,它們雖然在感染過程中的作用不相同,但是在SARS康復病人血清中,它們的特異性抗體滴度都增高,研究者也可以通過試驗獲得多克隆抗體,Huang等通過研究也認為S蛋白有利於研發非典疫苗。多數研究學者針對S2蛋白的保守及其結構特點認為S2區是研製保護性疫苗的重要靶位。S蛋白的研究對非典疫苗的研究、生產和預防及對SARS的治療非常有價值,對將來面對突發事件提供了有利的引導,對醫學事業的發展也有重要意義。