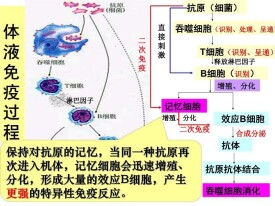
體液免疫
體液免疫
所謂體液免疫(humoral immunity),即以效應B細胞產生抗體來達到保護目的的免疫機制。負責體液免疫的細胞是B細胞。體液免疫的抗原多為相對分子質量在10,000以上的蛋白質和多糖大分子,病毒顆粒和細菌表面都帶有不同的抗原,所以都能引起體液免疫。
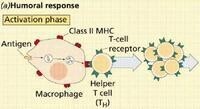
體液免疫
B細胞B細胞產生漿細胞和記憶細胞
第一步:B細胞表面的受體分子與互補的抗原分子結合后,活化、長大,並迅速分裂產生一個有同樣免疫能力的細胞群——克隆(clone)、無性繁殖系。其中一部分成為漿細胞,產生抗體;一部分發展為記憶細胞(memory cell)。
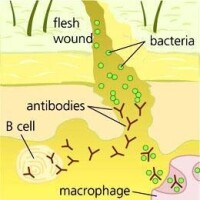
免疫細胞
漿細胞漿細胞產生抗體。漿細胞一般停留在各種淋巴結。每一個漿細胞每秒鐘能產生2000個抗體,它們壽命很短,經幾天大量產生抗體之後就死去,而抗體則進入血液循環發揮生理作用。漿細胞產生的抗體“Y”兩短臂末端高變區與抗原結合,抗體的柄端(FC)可與吞噬細胞(如巨噬細胞)上的受體結合而使抗原—抗體複合物被吞噬。
記憶細胞記憶細胞與二次免疫反應,記憶細胞不能分泌抗體,只能通過產生漿細胞,由漿細胞產生抗體。它們壽命長、對抗原十分敏感,能“記住”入侵的抗原。
當同樣抗原第二次入侵時,能更快的做出反應,很快分裂產生新的漿細胞和新的記憶細胞,漿細胞再次產生抗體消滅抗原。這就是二次免疫反應。它比初次反應更快,也更強烈。
體液免疫的兩個關鍵
產生高效而短命的漿細胞,由漿細胞分泌抗體清除抗原.
產生壽命長的記憶細胞,發生二次反應立即消滅再次入侵的同樣抗原。
臨床上一個反覆發作的化膿感染,常使醫生想到患者是否有免疫缺陷病,一般原發免疫缺陷發病年齡很小,而繼發性免疫缺陷病人多在30歲以上。絕大多數免疫缺陷病人多表現為體液和細胞免疫同時受損,所以應全面檢查這兩方面的功能。遺憾的是,目前應用的檢測方法的局限性,其結果常難以得出明確結論。
1、血清免疫球蛋白的測定
免疫細胞
體液免疫功能缺陷首先考慮患者血清Ig水平,如果所有類別Ig水平均降低,即稱為一般性聯低丙種球蛋白血症。如果免疫球蛋白水平極度低下,或IgG、IgM、IgA,三類Ig總量低於2mg/ml則稱為嚴重低丙種球蛋白血症或無丙種球蛋白血症(agammaglobulinemia)。如果只一種或兩種Ig水平降低,則稱為異常丙種球蛋白血症(dysgammaglobulinemia)。
一般性低丙種球蛋白血症多見於繼發性免疫缺陷病。無丙種球蛋白血症常見於原發免疫缺陷病。但是常有約50%IgA缺陷病人無臨床癥狀,伴有反覆感染的IgA缺陷病人常同時有IgG的缺陷。常規的定量檢測血中Ig的方法是單向免疫擴散和免疫比濁法。
2、分泌型IgA(SIgA)的測定
SIgA是粘膜抗感染的重要因素,但是粘膜抗感染還包括少量滲出的IgM和IgG,還有細胞免疫的作用。由SIgA缺陷病人常可檢測出針對牛奶或其他食物蛋白的沉澱抗體和自身抗體,說明機體對抗原蛋白質吸收異常,同時也存在免疫調節系統的功能紊亂。一般來說血清IgA缺陷病人常伴有SIgA缺陷,反之亦然。說明在機體中血清IgA和SIgA之間有某種生物相關性。
最近也有報導少數SIgA缺陷病人的血清IgA水平正常,因而分別檢查血清中和分泌液中IgA水平還是有必要的。目前用免疫比濁法可較精確地測定分泌液中IgA時和IgM和IgC水平。在用單向免疫擴散和免疫比濁法定量IgA時,因抗血清是針對這兩型共有的α鏈的,故不能區分SIgA和血清來源的IgA。而應用抗分泌小體的抗體用酶免疫分析法,可區分血清IgA和分泌型IgA,並可對SIgA進行定量。
3、常見抗體的測定
在嚴重免疫缺陷病人缺乏上述抗體,常見抗體的缺損可驗證或支持免疫蛋白測定的結果。然而對於比較複雜的免疫缺陷,由於這類抗體主要反映過去的免疫應答能力,此外這種初次應答能力持續期短,易於消退,所以對新近發生的繼發性免疫缺陷的診斷幫助不大。
原發性免疫缺陷和繼發性免疫缺陷均可導致體液免疫功能下降。原發性體液免疫功能缺陷可能由於B細胞分化障礙,細胞內合成Ig功能紊亂或由於抑制性細胞功能過強。繼發性體液免疫功能降低可能由於蛋白質大量丟失,蛋白質吸收障礙、營養不良、免疫抑制治療的副作用,病毒感染(艾滋病)等。在診斷原發性體液免疫功能缺損中可檢查B細胞的數目和功能以確定造成缺損的原因。
1.外周血B細胞數目的檢測首先進行常規的外周血白細胞總數和分類計數檢查,這些結果是評價病人免疫系統功能狀態的基本資料。由於在全血中淋巴細胞所佔比例很少,而T細胞和B細胞不能藉形態學特徵分類,所以外周血B細胞數檢測需先從全血分離出富含淋巴細胞的單個核細胞(peripheral blood mononuclear cell,PBM)。再依靠B細胞表面有免疫球蛋白分子或其他特徵來檢查B細胞。常用的方法是將待檢者的PBM用FITC標記的免疫抗人Ig作直接免疫熒光染色,在熒光顯微鏡下顯熒光的細胞為帶有表面免疫球蛋白的B細胞。正常人B細胞的約佔PBM的10%。
2.外周血B細胞功能的檢測 分離受檢者血液PBM細胞,體外培養時加入B細胞刺激物如RWM(美洲商陸刺激素)或SAC(金黃色莆萄球菌來源的刺激物)後由B細胞變成Ig分泌細胞的數量。體液免疫功能缺損患者,其PBM對PWM和SACA刺激的反應降低,產生Ig分泌細胞數正常人顯著減少。在進一步檢查這種免疫缺損的原因,則應檢查是由B細胞或TH細胞缺損所致,還是由於TS細胞數量或活性增強引起的。
抗體形成細胞計數:檢查人類Ig分泌細胞是用反向溶血空斑檢測(reversed hemolytic plaque assay)法。將待檢人的PBM、用SPA包被的SRBC(SPA-SRBC)、兔抗人Ig抗體、補體四種成分混合,灌入用兩張玻片做成的小室,密封好,放入溫箱培養1-3小時,,在此期間,作為抗人Ig抗體的免疫IgG的FC段可與SRBC表面SPA結合,當Ig分細胞分泌出遊離的Ig分子時,這些人Ig分子與SRBC表面的抗人Ig抗體結合形成免疫複合物,即可活化補體,使SPA-SRBC溶解,因此在Ig分泌細胞周圍形成一個圓形的溶血區,稱為溶血空斑,每一個溶血的空斑就代表一個Ig分泌細胞。
檢查小鼠Ig分泌細胞應用的溶血空斑試驗比較簡單,即SRBC免疫注射小鼠,4天後取脾製成單個細胞懸液,加入一定量SRBC(靶細胞)混合,在補體參加下,產生抗體的細胞分泌出的Ig與SRBC(抗原)結合在補體作用下,溶血,表現肉眼可見的溶血空斑。計數空斑數代表分泌抗體的細胞數。
體液免疫是一個相當複雜的連續過程,大體上可以分為三個階段。
抗原進入機體后,除少數可以直接作用於淋巴細胞外,大多數抗原都要經過吞噬細胞的攝取和處理,經過處理的抗原,可將其內部隱蔽的抗原決定簇暴露出來。然後,吞噬細胞將抗原呈遞給T細胞,刺激T細胞產生淋巴因子,淋巴因子刺激B細胞進一步增殖分化成漿細胞和記憶細胞。少數抗原可以直接刺激B細胞。
B細胞接受抗原刺激后,開始進行一系列的增殖\分化,形成效應B細胞。在這個過程中,有一小部分B細胞成為記憶細胞,該細胞可以在體內抗原消失數月乃至數十年以後,仍保持對抗原的記憶。當同一種抗原再次進入機體時,記憶細胞就會迅速增殖、分化,形成大量的效應B細胞,繼而產生更強的特異性免疫反應,及時將抗原清除。
在這一階段,抗原成為被作用的對象,效應B細胞產生的抗體可以與相應的抗原特異性結合,發揮免疫效應。例如,抗體與入侵的病菌結合,可以抑制病菌的繁殖或是對宿主細胞的黏附,從而防止感染和疾病的發生;抗體與病毒結合后,可以使病毒失去侵染和破壞宿主細胞的能力。在多數情況下,抗原抗體結合後會發生進一步的變化,如形成沉澱或細胞集團,進而被吞噬細胞吞噬消化,等等。
指B細胞在T細胞輔助下,接受抗原刺激后形成效應B細胞和記憶細胞。效應B細胞產生的具有專一性的抗體 與相應抗原特異性結合后完成的免疫反應。體液免疫的關鍵過程是產生高效而短命的效應B細胞,由效應B細胞分泌抗體清除抗原。產生壽命長的記憶細胞,在血液和淋巴中循環,隨時“監察”,如有同樣抗原再度入侵,立即發生免疫反應以消滅之(二次反應)。
指T細胞在接受抗原刺激后形成效應T細胞和記憶細胞。效應T細胞與靶細胞特異性結合,導致靶細胞破裂死亡的免疫反應。
而且還相互配合共同發揮免疫效應。病毒感染過程中,往往是先通過體液免疫來阻止病毒在機體內傳播,若病毒已經侵染到寄主細胞中,就要通過細胞免疫。這是效應T細胞與靶細胞結合,使靶細胞通透性改變,滲透壓發生變化,最終導致靶細胞破裂死亡。
體液免疫先起作用,阻止寄生物的散播感染;當寄生物進入細胞后細胞免疫將抗原釋放;再由體液免疫最後清除。若細胞免疫不存在時,體液免疫也將大部分喪失。
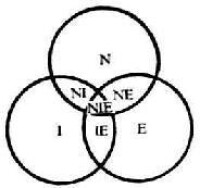
機體內各系統可抽象地以集合概念表明,則神經,免疫和內分泌三系統間的關係可以圖10-1中的集合群表示。其中三個集合兩兩重疊處可分別代表神經(N)與免疫(I),免疫(I)與內分泌(E)及神經(N)與內分泌(E)間的共同範疇,而三重疊部應視為神經、免疫和內分泌的共同內容(NIE)。集合間各有種組合方式可羅列如表10-1和圖10-2。
圖10-1神經(N)、免疫(I)和內分泌(E)系統的關係
體液免疫
機體關係
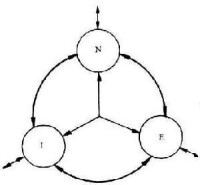
圖10-2N、I、E間作用方式
由表10-1可見,神經免疫內分泌學(NIE)與神經內分泌學(NE)、神經免疫學(NI)和免疫內分泌學(IE)相比,涉及更為複雜的系統間影響和作用。內內涵廣泛,並以NE、NI和IE間的聯繫為基礎。系統間作用方式,既有直接和間接之分,亦要同時和先後之別,系統間交互作用的性質可為增強、減弱、修飾、允許或協同,借變頻、變時和變力等方式體現。系統間作用的屬性,可有生理和病理性之分,是質和量的互變過程。上述關係圖示為二維描述,實際應為立體過程,結合時間變數,則三大系統間的交互影響即為四維圖象,這難以直觀圖示。
鑒於目前描述神經,免疫和內分泌系統間關係的術語較多且易混淆,缺乏統一性,故應確定術語的範疇及相互關聯繫,以決定相應學科內容及領域。
當抗原(病菌或病毒)第一次感染人體時,會被先天免疫的細胞所吞噬、清除,而其中一部分細胞特稱APC——在刺激B細胞方面主要為樹狀細胞(dendritic cells),APC抗原遞呈現細胞(antigen.presenting cell),它們除了能吞噬、分解抗原,還能將分解后的碎片(一小段peptides)呈現(present)給B cell,使之活化、分裂,並經clonoal selection(細胞細選擇、株落選擇)節選出對抗原最具親和力的抗體,(此時為lgm),抗體的變異區(variable region)能與抗原產生專一性的結合,阻止它感染正常細胞,並用另一端的FC portion與巨噬細胞結合,使巨噬細胞吞噬抗原,達到消菌的目的。
活化的B細胞在過一段時日(通常大於四周)後會把分泌的抗體由lgm轉變為lgG。lgG在人體的壽命遠較lgm長,約六個月。受過第一次刺激的B細胞在四周后變為記憶B細胞(memory cells),除了分泌lgG外,它還能在第二次感染時以更快的時間產生更多的抗體,同時,memory B cell在人體特定抗原的感染而言是具有終身的保護作用的。這也是打疫苗能保護一個人免疫受特定病菌感染的原因。
在現代內分泌學的理論體系中,“內分泌”概念應包括內分泌、神經內分泌、旁分泌和自分泌等方式;而激素的內涵亦大為增加,諸如局部激素、循環激素、神經激素等,而許多免疫因子如淋巴因子和單核因子等均符合激素的標準;嚴格地講,神經系統和免疫系統既與內分泌系統有種種區別,又有諸多共性,這也是系統間相互影響的基礎。表10-1N、I、E間的作用和聯繫方式及相應學科劃分。
細胞免疫和體液免疫是藉助於血液循環、淋巴循環或組織液而進行和實現的生理過程,而神經內分泌調控也最終由循環血液或組織液完成,故在此交匯路途上難免發生交叉性影響和作用。所以神經內分泌或免疫內分泌聯繫在活體內必將受到免疫或神經源性因素的影響。已研究的神經免疫學領域和內容,絕大多數發現有內分泌因素或成份的參與。精神和心理活動以及行為的共同基礎是中樞神經系統的高級功能活動,由此可把精神神經免疫學(psychoneuroimmunology)及行為神經免疫心理學(behaviouralneuroimmunololgy)划入神經免疫內分泌學(neuroimmunoendocrinology),作為其重要的分支學科。
神經免疫內分泌學可直接引用神經科學、免疫學和內分泌學的相關概念和理論,其研究方法應是跨學科的,研究工作應採用多重指標,全面觀察,對相關臨床問題的考察,更應從多方面入手,分清主次矛盾,並應考慮與其它系統的聯繫和影響,以期在不同水平上全面而完整地反映機體的真實生理過程。