CD4
人體免疫系統中的重要免疫細胞
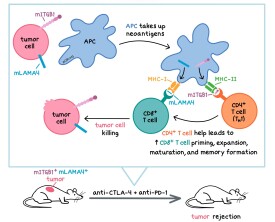
CD4細胞是人體免疫系統中的一種重要免疫細胞,CD4 主要表達於輔助T(Th)細胞,是Th細胞TCR識別抗原的共受體,與MHCⅡ類分子的非多肽區結合,參與Th細胞TCR識別抗原的信號轉導,CD4也是HIV的受體,由於艾滋病病毒攻擊對象是CD4細胞,所以其檢測結果對艾滋病治療效果的判斷和對患者免疫功能的判斷有著重要作用。
正常成人的CD4細胞在每立方毫米500個到1600個,艾滋病病毒感染者的CD4細胞出現進行性或不規則性下降,標誌著免疫系統受到嚴重損害,當CD4細胞小於每立方毫米200個時,可能發生多種機會性感染或腫瘤。
艾滋病的感染原理:淋巴細胞是具有抗感染和腫瘤免疫的細胞,它主要含CD4分子與CD8分子。CD4細胞起到“通風報信”的作用,CD8細胞有殺傷被感染細胞和癌細胞的作用。當艾滋病毒進入人體后,它只會感染表面CD4陽性的淋巴細胞,這樣CD8細胞就無法殺傷被感染細胞和癌細胞,導致機會性感染和癌症。
CD4細胞
分化
初始CD4+T 細胞接受抗原刺激后,在不同的條件下可分化成不同亞型的T 細胞,執行不同的功能。其分化方向受抗原的性質、局部環境中的激素及細胞因子等多種因素的調控,其中細胞因子的種類和細胞因子之間的平衡對T h 細胞的分化具有重要的調節作用。初始CD4+T細胞在IL-12和g干擾素(interferon-g, IFN-γ)的誘導下分化為Th1細胞,分泌IFN-γ,參與細胞介導的免疫應答;在IL-4 的誘導下分化為Th2細胞,分泌IL-4、IL-5和IL-13,參與體液免疫應答;在b 轉化生長因子(Transforming growth factor beta, TGF-β)單獨誘導下分化為Treg細胞,分泌TGF-β,參與免疫調節;在TGF-β 和IL-6 的共同誘導下分化為Th17,分泌IL-6和IL-17,參與炎症反應和自身免疫性疾病。在此過程中,T 細胞上的相關受體分子及轉錄子都發揮著重要的作用。Th1、Th2 和Treg 的發育和分化分別受轉錄因子T-bet、GATA-3和Foxp3 等的特異性調控。Langrish等研究發現了IL-12家族的新成員IL-23,它與IL-12有著共同的P40亞單位,但是,IL-12二聚體由IL-12P40和IL-12P35組成,而IL-23由IL-12P40和IL-23P19 組成。進一步研究發現,在IL-23缺陷型小鼠中幾乎沒有Th17 細胞產生,IL-23 缺乏不影響Th17 細胞的正常產生,卻使其不能擴展和存活。因此IL-23 不是Th17 分化的必需因子,卻Th17 細胞存活、繁殖的重要因子。在誘導Treg 細胞和Th17 細胞分化的過程中,TGF-β 起著重要的作用。在TGF-β 單獨的作用下,活化的初始CD4+T 細胞分化為Foxp3+Treg 細胞,而在TGF-β 和IL-6 的共同誘導下分化為Th17 細胞,由此說明IL-6抑制了Foxp3+Treg細胞的分化。Veldhoen等將CD25+CD4+T 細胞、初始T 細胞和樹突狀細胞共同培養。在IL-6 存在時,初始T 細胞可以有效分化為Th17 細胞,且具有TGF-β1 依賴性;而在誘導的過程中加入抗IL-6 中和抗體則可促進Foxp3+Treg 細胞的分化。當機體處在穩定狀態下或沒有炎症損傷的情況下,免疫系統產生的TGF-β1 抑制著效應T 細胞的增殖,誘導Treg 細胞表達,從而維持機體的免疫耐受;但當存在感染或炎症時,急性期蛋白IL-6 大量產生,抑制了Treg 細胞表達,與TGF-β1 共同誘導Th17 細胞的分化,從而介導機體的前炎症反應
對於癥狀性艾滋病或CD4<200個/ul的患者建議開始治療,基本上沒有任何的爭論。但是對於CD 4>200個/ul的情況何時開始實施高效抗逆轉錄病毒治療,目前仍有爭論。早期治療的益處和危險性分述如下:
(1)潛在的益處
①及早控制病毒複製和變異,明顯降低體內病毒載量。
②防止免疫損傷的進展,有利於維持或重建正常的免疫功能。
③推遲AIDS的發展,從而延長壽命。
④減少由於複製過程中病毒選擇生長而產生耐葯突變株的危險。
(2)潛在的危險性
①由於長期用藥后,藥物的毒副作用和服藥所帶來的不便,影響生活質量。
②早期發生耐葯現象,並導致將來用藥受限。
③尚不清楚長期用藥對免疫功能的影響。
④因葯價昂貴長期用藥不勝負荷。
4、我國艾滋病抗病毒治療方案:
臨床分期
CD4細胞計數(個/mm3)
推薦意見
急性感染期
無論CD4細胞計數為多少
考慮治療
無癥狀感染期
>350/mm3,無論血漿病毒載量的值為多少
定期複查,暫不治療
200—350/mm3之間
定期複查,出現以下情況之一即進行治療:
1)CD4細胞計數1年內下降大於30%;
2)血漿病毒載量>100000/mL;
3)患者迫切要求治療,且保證有良好的依從性。
HIV病毒會附著在CD4細胞上,使得病毒進入CD4細胞並感染它。當一個人被HIV病毒感染時,病毒便在感染者體內免疫系統內製造更多的病毒細胞,把它變成製造HIV病毒的工廠。HIV病毒會不斷複製,CD4細胞會被破壞殆盡!免疫系統會再製造新的免疫細胞替代死亡的免疫細胞,但是新製造出的免疫細胞仍免除不了被HIV病毒感染。即使感染HIV病毒者感覺身體良好,沒有任何癥狀,可能有上億的CD4 T細胞被破壞。CD4為最重要的免疫細胞,感染者一旦失去了大量CD4細胞,就可能出現嚴重的疾病危險,這些疾病我們稱之為隨機性感染疾病。
在人體的血液里,白細胞是非常重要的一類血細胞,簡單的說,白細胞起到的就是免疫作用。而白細胞本身可以劃分為數個類別,這包括:
大家都知道,HIV病毒主要破壞和侵犯人體的CD4細胞。CD4細胞,也可以表示為CD4+T細胞,是T淋巴細胞的一種(T淋巴細胞可以根據其表面的某種特異蛋白質分子來劃分為不同種類或亞群,不同亞群的T淋巴細胞就是根據這些特異蛋白質分子的名稱而得名,這樣,CD4細胞,就是表面有CD4分子的T淋巴細胞。另外,CD本身是cluster difference的首字母縮寫,可以解釋為“分化分形”之意,因此,CD4細胞檢查也稱為淋巴細胞亞群檢查)。
當病原體進入人體后,一種免疫反應的過程是這樣的。首先,巨噬細胞會開始將病原體吞噬,同時隨著吞噬作用的進行,巨噬細胞會釋放出抗原信息(一個分子,常為病原體表面的蛋白質並被免疫系統作辨別之用)並傳遞給CD4細胞,進一步,抗原的傳遞會導致抗體的產生,這些抗體可以容易的依附到病原體上,使病原體更容易的被巨噬細胞所捕獲并吞噬。從這個過程來看,不難體會到CD4細胞的重要之處,他就像免疫系統的幫手和眼睛,來傳遞病原信息。正因如此,CD4細胞也稱之為輔助型T淋巴細胞。而HIV病毒對CD4細胞的破壞,則打斷了完整的免疫反應鏈條。
當HIV病毒進入人體后,由於病毒可以識別出CD4細胞表面的特異蛋白質分子,因此也就可以識別並侵入CD4細胞。病毒侵入后,就將自己的基因整合到進了CD4細胞的DNA中,這樣,隨著CD4細胞的複製和繁殖,實際上病毒也就完成了複製和繁殖。而當病毒從CD4細胞中“破壁而出”時,細胞本身也就凋亡了...。
在CD4檢查的報告單上,還可以看到一種CD8+T細胞。而這又是另一種T淋巴細胞,也稱之為細胞毒性T細胞,其功能就像一個“殺手”或細胞毒素,可以消滅受感染的細胞,這也包括受HIV病毒感染的CD4細胞。這樣,就會出現報告單上CD4細胞數和CD8細胞數倒置的情況,即CD4和CD8的數量比值小於1。而未受HIV病毒感染的人體,這兩者的比值通常是大於1的。CD4細胞的絕對計數通常會隨生理情況的不同而有較大的波動,而CD4和CD8的比值則相對比較穩定。
在感染HIV病毒后,起初在免疫應答的建立前,由於沒有抗體的產生,病毒的複製快速進行,感染者就會出現急性感染期的癥狀,而病毒數量會快速達到一個很高的數值,同時CD4細胞數量則會快速下降到一個低點。隨著抗體的產生,免疫系統開始清除病毒,病毒數量開始下降,而CD4細胞數量則逐漸上升。可惜的是,由於部分病毒在複製過程中會很快變異,而這些變異的病毒就得以在體內存留並繼續複製,這就逐步進入了無癥狀潛伏期。在潛伏期里,由於抗體的存在,病毒複製相對維持在一個比較低的水平,但CD4細胞的破壞卻仍在繼續,直到當CD4細胞數量降低到不能繼續抑制病毒複製水平時,病毒數量又會開始快速增長,而潛伏期就結束了。