共找到2條詞條名為鋦的結果 展開
- 呈銀白色的放射性人造金屬元素
- 漢語漢字
鋦
呈銀白色的放射性人造金屬元素
鋦(Curium)金屬元素,原子序數為96,元素符號Cm。是一种放射性人造元素。呈銀白色,有延展性。由人工核反應獲得。在化合物中呈正三價。在一般社會生活中極不常見,在放射化學實驗及特殊的同位素能源中使用較為廣泛。1944年,美國加州大學伯克利分校教授西博格帶領團隊在伯克利發現鋦元素。
鋦為銀白色金屬,熔點1340°C,鋦有兩種同素異形體,其密度分別是13.51克/厘米3和19.26克/厘米3。金屬鋦易溶於稀的無機酸;研究過的鋦的固體化合物主要有鹵化物、氫化物和氧化物。用途最大的鋦同位素石鋦242和鋦244,主要用作同位素能源;鋦244還是在高通量反應堆中製造超鋦元素的原料。
元素序號:96
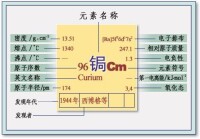
(圖)鋦
元素原子量:[247]
相對原子質量:[247]
核內質子數:96
核外電子數:96
核電核數:96
質子質量:1.60608E-25
質子相對質量:96.672
所屬族數:IIIB
摩爾質量:192
氫化物:——
氧化物:——
最高價氧化物:——
密度:13.511
沸點:——
外圍電子排布:5f7 6d1 7s2
核外電子排布:2,8,18,32,25,9,2
原子半徑:——
離子半徑/Å:0.97
常見化合價:+3,+4
顏色和狀態:金屬
為紀念居里夫婦(皮埃爾·居里Pierre Curie和瑪麗·居里Marie Curie)而命名。發現人:西博格(G.T.Seaporg)、詹姆斯(R.A.Jamse)和吉奧索(A.Ghiorso)發現年代:1944年發現過程:1944年由西博格、詹姆斯和吉奧索用人工方法合成製得。1947年,維爾納(L.B.Werner)和珀爾曼(I.Perlman)用中子照射241Am製得較重要的242Cm。1944年,也就是發現鎇的同一時期里,西博格和他的同事們用高能量α粒子轟擊鈈的同位素鈈-239,得到96號元素。為了紀念居里夫婦,就命名這個元素為curium,元素符號定為Cm。
物理性質密度為13.5克/厘米3。室溫下為雙一六方密堆積;較高溫度時為面心立方結構。熔點為1340±40℃。銀白色金屬。在空氣中銀白色金屬光澤會變暗。銀白色的放射性人造金屬元素,有延展性。鋦為銀白色金屬,熔點1340°C,鋦有兩種同素異形體,其密度分別是13.51克/厘米³和19.26克/厘米³。金屬鋦易溶於稀的無機酸;元素名稱:鋦元素原子量:[247]氧化態:Main Cm+3Other Cm+2, Cm+4原子體積:(立方厘米/摩爾)18.28晶體結構:晶胞為六方晶胞。晶胞參數:a = 349.6 pmb = 349.6 pmc = 1133.1 pmα = 90°β = 90°γ = 120°元素類型:金屬相對原子質量: 247.07 常見化合價: +3,+4 電負性: 1.3外圍電子排布: 5f7 6d1 7s2 核外電子排布: 2,8,18,32,25,9,2同位素及放射線: Cm-241[32.8d] Cm-242[162.8d] Cm-243[29.1y] Cm-244[18.1y] Cm-245[8500y] Cm-246[4760y] Cm-247(放 α[15600000y]) Cm-248[348000y] Cm-249[1.1h] Cm-250[9700電子親合和能: 0 KJ·mol-1第一電離能: 588 KJ·mol-1 第二電離能: 0 KJ·mol-1 第三電離能: 0 KJ·mol-1單質密度: 13.511 g/cm3單質熔點: 1340.0 ℃ 單質沸點:約3000 ℃原子半徑: 0 埃 離子半徑:埃 共價半徑: 0 埃熔 點(℃): 1067沸 點(℃): 3110密度(g/cc,300K): 13.5比 熱/J/gK :蒸發熱/KJ/mol :熔化熱/KJ/mol: 15導電率/106/cm :導熱係數/W/cmK: 0.1
化學性質易溶於普通的無機酸中,多是三價化合物。化學性質與稀土元素極相似,有多種同位素。主要的有242Cm、244Cm、247Cm、248Cm等。研究過的鋦的固體化合物主要有鹵化物、氫化物和氧化物。
通過用氦核轟擊鈈原子製得。鋦的放射性如此強烈,以至於在黑暗中會閃閃發光。鋦,原子序數96,因紀念著名科學家居里夫婦而得名。1944年美國科學家西博格、詹姆斯等用32兆電子伏特的α粒子轟擊鈈239時發現鋦242,現已發現質量數為238~251的全部鋦同位素。鋦的發現先於95號元素鎇。
鋦僅有的幾個用途都與它極強的放射性有關:攜帶型α粒子源和放射性同位素熱電偶發電機。後者利用放射性衰變所產生的熱能向儀器提供電力。這些儀器必須在遠離人類和其他電源的條件下長期工作,例如太空探測器。[1] 因鋦是放射性金屬,輻射能量很大。常用作人造衛星和宇宙飛船中用來不斷提供熱量的熱源。用途最大的鋦同位素是鋦242和鋦244,主要用作同位素能源;鋦244還是在高通量反應堆中製造超鋦元素的原料。
鋦在地球上沒有單質或化合物礦藏存在,只能人工來合成。
金屬鋦易溶於普通的無機酸中,多是三價化合物。化學性質與稀土元素極相似,有多種同位素。主要的有Cm、Cm、Cm、Cm等。
研究過的鋦的固體化合物主要有鹵化物、氫化物和氧化物。
同位素 半衰期
242Cm 106d
243Cm 29.1y
244Cm 18.1y
245Cm 8500y
246Cm 4730y
247Cm 1.56x10^7y
248Cm 3.40x10^5y
250Cm 9000y
鋦-242是重要的超杯核素, 最早由西博格( GT.Seaborg) 等人於1944年人工製成。隨著核工業發展,鋦的產量及應用與日俱增。鋦是儀輻射體, 比放高、毒性大。一旦進入人體內,長期存留,不易排出。按國際放射防護委員會推薦,它們在人體內的最大容許積存量均為0.05微居里。為了保證從事開放性操作的工作人員身體健康, 除了減少放射性核素造成內污染外,還必須經常對工作人員進行內照射常規監測,估算每個工作人員體內放射性物質積存量,以便及時採取相應的措施,防止工作人員體內放射性物質積存量超過最大容許積存量。
UNSCEAR2000報道,切爾諾貝利核事故在1996年估算的242Cm釋放活性總量約為0.9PBq。242Cm為α放射性核素,主要通過食入、吸入、皮膚及傷口途徑造成內污染。
(1)吸收。
①呼吸道吸收。有關鋦在人肺組織中的轉運資料極為罕見。從1例事故性吸入244CmO2和AmO2的內污染案例來看,244CmO2由肺臟的半廓清期為28d。ICRP第48號出版物指出,基於鋦由肺臟的清除速度快,所有化合物M類的半廓清期約為數十天。
②胃腸道吸收。關於鋦在人胃腸道吸收的資料極罕見。動物資料表明,鋦由胃腸道的吸收率介於3×10−5~4×10−3。
(2)分佈。鋦自血液中的清除速度相當快,在靜脈注入后0.25~1h,血液鋦含量占注入量的21%,而在注入后2.5~10h,則降低到注入量的1%。在血液中,鋦主要存在於血漿內,其中,半數以上與球蛋白結合,與白蛋白的結合量佔5%~7%。自血液清除后的鋦主要沉積在骨骼和肝臟。
(3)排除。鋦自人體內的主要排除途徑是腸道和腎臟。由胃腸道攝入人體內的鋦,因其吸收率很低,大部分自腸道排除。ICRP第48號出版物認為鈈在人體內的代謝參數既適用於鎇,也適用於鋦,即進入血液的鋦,有10%直接排除出體外,50%沉積在骨骼,30%沉積在肝臟,其餘10%沉積在其他器官組織中。鋦自骨骼和肝臟的生物半排期分別為50a和20a。
動物實驗資料表明,鋦對機體的損傷效應與鎇相同。靜脈注入可溶性鋦后,造血系統遭受嚴重破壞,外周血中的紅細胞數明顯減少,白細胞除數量顯著減少外,併發生質的改變;同時還可見到未成熟的白細胞,嗜多染紅細胞及有核紅細胞等。在肝臟中,肝細胞變性、壞死,毛細血管擴張、充血,以及肝小葉邊緣區膽管增生。腎臟損傷表現為在血循環被破壞的基礎上,發展為進行性腎小管壞死,尤以近曲細管和遠曲細管相連部位更甚;在管腔內可見透明管型及顆粒管型;腎小球血管袢早期擴張充血;進而出現蛋白浸潤,腎小球均質化。長期沉積在體內的鋦,晚期可誘發各種腫瘤,如肺癌、骨肉瘤及乳腺癌等。
加速排除:DTPA是加速排出242Cm的首選藥物,促排效果顯著。但DTPA對難溶性鋦化合物(二氧化鋦)的促排效果是很差的。沉積在體內的鋦幾乎全部在骨骼內,而且它們由骨骼中的排除非常緩慢。
