膠體金
標記技術
膠體金是一種常用的標記技術,是以膠體金作為示蹤標誌物應用於抗原抗體的一種新型的免疫標記技術,有其獨特的優點。近年已在各種生物學研究中廣泛使用。在臨床使用的免疫印跡技術幾乎都使用其標記。同時在流式、電鏡、免疫、分子生物學以至生物晶元中都可能例用到。
膠體金(colloidal gold),又稱金溶膠(gold solution),是指分散相粒子直徑在l—150nm之間的金溶膠,屬於多相不均勻體系,顏色呈桔紅色到紫紅色。

膠體金
膠體金顆粒的基礎金核並非是理想的圓球核,較小的膠體金顆粒基本是圓球形的,較大的膠體金顆粒(一般指大於30nm以上的)多呈橢圓形。在電子顯微鏡下可觀察膠體金的顆粒形態。
膠體金因而具有膠體的多種特性,特別是對電解質的敏感性。電解質能破壞膠體金顆粒的外周永水化層,從而打破膠體的穩定狀態,使分散的單一金顆粒凝聚成大顆粒,而從液體中沉澱下來。某些蛋白質等大分子物質有保護膠膠體金、加強其穩定性的作用。呈色性微小顆粒膠體呈紅色,但不同大小的膠體呈色有一定的差別。最小的膠體金(2~5nm)是橙色的,中等大小的膠體金(10~20nm)是酒紅色的,較大顆粒的膠體金(30~80nm)則是紫紅色的。根據這一特點,用肉眼觀察膠體金的顏色可粗略估計金顆粒的大小。
光吸收性膠體金在可見光範圍內有一單一光吸收峰,這個光吸收峰的波長(λmax)在510~550nm範圍內,隨膠體金顆粒大小而變化,大顆粒膠體金的λmax偏向長波長,反之,小顆粒膠體金的λmax則偏於短波長。
在日光下仔細觀察比較膠體金的顏色,可以粗略估計製得的金顆粒的大小。當然也可用分光光度計掃描λmax來估計金顆粒的粒徑。製備的膠體金最好作電鏡觀察,並選一些代表性的作顯微攝影,可以比較精確地測定膠體金的平均粒徑;良好的膠體金應該是清亮透明的,若製備的膠體金混濁或液體表面有漂浮物,提示此次製備的膠體金有較多的凝集顆粒。
膠體金在潔凈的玻璃器皿中可較長時間保存,加入少許防腐劑(如0.02%NaN3)可有利於保存。保存不當時會有細菌生長或有凝集顆粒形成。少量凝集顆粒並不影響以後膠體金的標記,使用時為提高標記效率可先低速離心去除凝集顆粒。
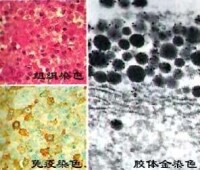
(圖)膠體金標記技術
氯金酸(HauC14)是主要還原材料,通過各種方法進行還原製備金溶膠,常用還原劑有檸檬酸鈉、鞣酸、抗壞血酸、白磷、硼氫化鈉等。根據還原劑類型以及還原作用的強弱,可以製備0.8nm~150nm不等的膠體金。常見的製備方法有一下幾種:
1、紫外光引發還原可製備金溶膠——其還原過程經歷了自由基機理。用紫外可見光譜觀察了不同反應時間溶膠狀態的變化。結果表明,光照反應2h時明顯出現金溶膠粒子,7h后氯金酸基本轉化完畢。同時,研究了穩定劑聚乙烯吡咯烷酮(PVP)的加入對還原過程的影響,結果表明,PVP的加入不僅穩定了溶膠,而且降低了反應速率。用SEM觀察了溶膠粒子聚集體的形貌。最後以1,4-bis(4-vinylpyridyl)phenylene為探針分子研究了這種溶膠的SERS活性。
2、納米金溶膠製備——以水為分散介質,PVP為分散劑,抗壞血酸作還原劑,用較高濃度的氯金酸溶液,在弱酸性條件下,通過化學還原法製得球狀、最大粒徑為20nm的金溶膠結果表明,還原劑用量為抗壞血酸/Au(摩爾比)=3,PVP的用量取PVP/HAuCl4(質量比)=1,還原體系自身pH值3~5,常溫293K為金溶膠製備的最佳條件。在此條件下製得的金粉粒度小,分散性好,且十分穩定,無反溶現象.
3、磷鉬酸作為光催化還原劑製備納米金溶膠——由於DMF與磷鉬雜多陰離子間的電荷轉移作用,導致鉬系雜多酸可成為製備納米金溶膠的光催化還原劑。實驗結果表明,紫外光照作用及光照時間、DMF用量等是影響納米金的形成和形貌的主要因素,選擇適宜的合成條件可以得到粒徑均勻、分散性好的納米金溶膠。
4、超短脈衝激光誘導製備金溶膠的方法——其製法為以氯金酸濃度在0~5mmol/L範圍內的水溶液作為反應溶液,調節可見/近紅外超短脈衝激光光束並聚焦,利用焦點附近的光束輻照氯金酸水溶液來製備金溶膠。本發明的製備方法工藝和裝置簡單,無需還原劑的引入,製備的金溶膠濃度高,穩定性好,雜質含量非常低,可用作高級非線性光學薄膜的前驅體,催化材料,也可用作食品、飲料及化妝品的添加劑。
6、一種採用激光轟擊固液界面連續製備純凈金溶膠——本發明系採用聚焦脈衝激光束在適當氣體保護下轟擊浸於連續流動液相中的,不斷相對移位的金靶表面,在固液界面產生高溫高壓微區而生成純凈的金溶膠流出反應器。本發明方法可連續製備純凈的金溶膠,不含過量還原劑及其反應副產物、保護劑、分散劑等有害雜質,無須提純,作為添加劑可直接應用於微電子器件、超大規模集成晶元、醫學、免疫標記以及食品、飲料、飲用水、酒類、化妝品等行業。

膠體金
膠體金應用電鏡水平的研究最早,發展最快,應用最廣泛。其最大優點是可以通過應用不同大小的顆粒或結合酶標進行雙重或多重標記。直徑為3~15nm 膠體金均可用作電鏡水平的標記物。3~15nm 的膠體金多用於單一抗原顆粒的檢測,而直徑15nm 多用於檢測量較多的感染細胞。
膠體金用於電鏡水平的研究,主要包括:①細胞懸液或單層培養中細胞表面抗原的觀察。②單層培養中細胞內抗原的檢測。③組織抗原的檢測。
金標記在電鏡水平的應用,主要方法包括:包埋前染色、包埋后染色、免疫負染色、雙標記技術和原位雜交技術等。
實驗證明,該法樣本用量少、檢測速度快、對比明顯、操作簡單、敏感性和特異性高,既可用於抗原檢測,也可用於抗體檢測,因此,可同時適用於科研和診斷。
2、膠體金在光鏡水平的應用
膠體金同樣可用做光鏡水平的標記物,取代傳統的熒光素、酶等。各種細胞塗片、切片均可應用。主要用於:①用單克窿抗體或抗血清檢測細胞懸液或培養的單層細胞的膜表面抗原。②檢測培養的單層細胞胞內抗原,③組織中或亞薄切片中抗原的檢測。
膠體金用於光鏡水平的研究,可以彌補其它標記物不可避免的本底過高和內部酶活性干擾等缺點。
3、膠體金在流式細胞儀中的應用:
應用熒光素標記的抗體,通過流式細胞儀計數分析細胞表面抗原,是免疫學研究中的重要技術之一。但由於不同熒光素的光譜相互重疊,區分不同的標記困難,因此必須尋找一種非熒光素標記物,用於流式細胞計數。這樣可以同時進行幾種標記。該標記物必須能夠改變散射角,膠體金可以明顯地改變紅激光散射角,因而可以作為流式細胞儀的標記物之一。
4、凝集試驗:單分散的免疫金溶膠呈清澈透明的溶液,其顏色隨溶膠顆粒大小而變化,當與相應抗原或抗體發生專一性反應后出現凝聚,溶膠顆粒極度增大,光散射隨之發生變化,顆粒也會沉降,溶液的顏色變淡甚至變成無色,這一原理可定性或定量地應用於免疫反應。
5、免疫印跡技術(immunoblotting):免疫印跡是一種較新的免疫化學技術。用聚丙烯醯胺凝膠電泳將蛋白質分離,得到的區帶轉移至硝酸纖維素膜,然後用酶免疫法(或免疫熒光、RIA)進行定量。
免疫膠體金也可用於該法的定量。轉移后的硝酸纖維素膜與某特異性的抗體保溫后,再與經葡萄球菌A蛋白致敏的膠體金溫育,徹底洗去多餘的膠體金,根據膜上膠體金顆粒顏色深淺可測知樣品中的特異性抗原。
利用金顆粒可催化銀離子還原成金屬銀這一原理,採用銀顯影劑增強金顆粒的可見性,更可大大提高測定靈敏度,檢測下限可低至 0.1ng,這種免疫金銀染色法應用已日趨廣泛。
由於膠體金免疫印跡技術簡便、快速,且有相當的高的靈敏度,在臨床免疫診斷上有很大的應用潛力。
6、膠體金在肉眼水平的應用
膠體金取代傳統三大標記物,用於肉眼水平的免疫檢測中。除了膠體金本身具有的特點外,還有以下優點:①試劑和樣本用量極小,樣本量可低至1~2ul;②不需γ-計數器、熒光顯微鏡、酶標檢測儀等貴重儀器,更適於現場應用; ③沒有諸如放射性同位素、鄰苯二胺等有害物質參與;④實驗結果可以長期保存;⑤時間大大縮短,提高了檢測速度。金標過程中,無共價鍵形成,是一定離子濃度下的物理吸附。因此幾乎所有的大分子物質都可被金標記,標記后大分子物質活性不發生改變。實驗結果表明,膠體金的敏感性可達到 ELISA的水平。而結合銀染色時,檢測的敏感性更大大提高。
1、氯金酸易潮解,應乾燥、避光保存。
2、氯金酸對金屬有強烈的腐蝕性,因此在配製氯金酸水溶液時,不應使用金屬葯匙稱量氯金酸。
3、用於製備膠體金的蒸餾水應是雙蒸餾水或三蒸餾水,或者是高質量的去離子水。
4、是以製備膠體金的玻璃容器必須是絕對清潔的,用前應先經酸洗並用蒸餾水沖凈。最好是經硅化處理的,硅化方法可用5%二氯甲硅烷的氯仿溶液浸泡數分鐘,用蒸餾水沖凈后乾燥備用。
5、膠體金的鑒定和保存:膠體金的製備並不難,但要制好高質量的膠體金卻也並非易事。因此對每次制好的膠體金應加以檢定,主要檢查指標有顆粒大小,粒徑的均一程度及有無凝集顆粒等。
影響膠體金溶液穩定性的主要原因是:
1、膠粒間的相互吸引力。當膠粒相距很近時,這種吸引力可能導致膠粒合併變大。
2、水化層的帶電情況。一種溶膠的各個膠粒都帶有相同的電荷。同性電荷相斥,雙電層愈厚,膠粒帶電量愈大,排斥力愈大,愈能阻止膠粒合併聚結,溶膠愈穩定。
3、膠體界面的溶劑膜,當二固體間夾有一厚層液體時,這層液體膜有一個反抗二固體接近的排斥力。兩個膠粒要進一步接近,只有克服它們之間的溶劑化膜的斥力才有可能,因此溶劑膜的斥力是使溶膠穩定的原因之一。
