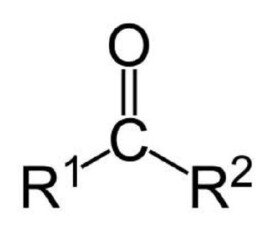
酮
羰基與兩個烴基相連的化合物
酮是羰基與兩個烴基相連的化合物。根據分子中烴基的不同,酮可分為脂肪酮、脂環酮、芳香酮、飽和酮和不飽和酮。芳香酮的羰基直接連在芳香環上;羰基嵌在環內的,稱為環內酮,例如環己酮。按羰基數目又可分為一元酮、二元酮和多元酮。羰基嵌在環內的,稱為環內酮,例如環己酮。一元酮中,羰基連接的兩個烴基相同的稱單酮,例如丙酮(二甲基甲酮)。互不相同的為混酮,例如苯乙酮(苯基甲基甲酮)。酮分子間不能形成氫鍵,其沸點低於相應的醇,但羰基氧能和水分子形成氫鍵,所以低碳數酮(低級酮)溶於水。低級酮是液體,具有令人愉快的氣味,高碳數酮(高級酮)是固體。

酮
酮的結構
上連有兩個烴基,如右圖所示。
酮的結構
a. 選擇含有羰基的最長的碳鏈做主鏈;
b 合併相同取代基名稱,標明位置,寫在酮母體名稱前。
酮的沸點(攝氏度)
酮的沸點
丁酮:79.6

酮的溶解度
苯丙酮:216.5
酮的溶解度(見右圖)
酮
親核加成反應

不飽和酮的反應
和 1,4- 加成。α,β- 不飽和醛(酮)的 1,4- 加成實際相當於 3,4- 加成。
Michael加成
有活潑亞甲基化合物形成的碳負離子,對α,β-不飽和羰基化合物的碳碳雙鍵的親核加成,是活潑亞甲基化物烷基化的一種重要方法,該反應稱為Michael反應。Michael加成最重要的應用是Robinson增環(annelation)反應。若以環酮作為Michael反應的供體,同甲基乙烯基酮(受體)作用,可得產物1,5-二酮,後者經分子內的羥醛縮合併脫水,可在原來環上再增加一個新的六元環,該過程稱為Robinson增環反應。
Robinson成環
從現代有機合成的觀點看,羅賓遜成環反應實際上屬於一種串聯反應。是由一個麥克爾加成與羥醛縮合相串聯而成的反應。在反應開始時,由一個羰基化合物生成的烯醇鹽親核進攻一個α,β-不飽和酮,發生麥克爾加成。產物隨即進行分子內羥醛縮合,得到羅賓遜成環反應產物。
與HCN 的親核加成
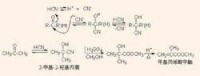
HCN 親核加成
1. 與 HO 反應——生成二醇
2. 與 ROH 反應——生成縮醛(酮)
特點:
a. 縮醛(酮)的結構特點是含有 O-C-O 鍵;
b. 縮醛(酮)反應可用於保護羰基;

酮
此反應;
d. 分子內同時含有羥基和醛(酮)羰基時,可發生分子內縮醛(酮),形成五、六元環;
e. 與 RSH親核加成
f. 與NaHSO親核加成
分子內同時含有強鹼性基團-ONa 和強酸性基團 -SOH,發生分子內酸鹼中和使反應不可逆,生成α-羥基磺酸鈉晶體從有機相中沉澱出來,α-羥基磺酸鈉在酸性條件下可水解為原來的醛(酮)。所以,該反應可以用於醛(酮)的分離。-SOH 是一個很好的離去基團,可以通

酮
該製備2-羥基丙腈的方法雖然歷經兩步,但避免在酸性條件下直接使用 HCN 所帶來的危險。
含氮親核試劑 (G-NH) 對醛酮的親核加成后再消除 HO,從而生成 C=N-G 的 C=N 鍵:
因 G 的不同生成的亞胺類化合物具有各自的名稱
1. 與 NH 的親核加成
2. 與 RNH 及 ArNH 的親核加成
3. 與肼的衍生物的親核加成
4. 與 HNOH 的親核加成及 Beckmann 重排
5. 與 RNH親核加成生成烯胺
1.催化加氫
2.還原劑法
3. Wolff-Kishner-黃鳴龍還原
4. Carnnizzarro反應
5.安息香縮合
1. Tollens試劑、Fehling試劑和 Benedit試劑的氧化
2. Baeyer-Villiger 氧化——RCOOOH 氧化
Perkin反應
Wittig反應
Mannich反應