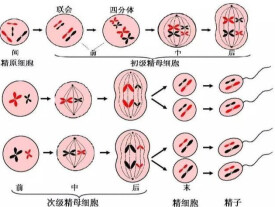
精子發生
精子發生
精子在睾丸的曲細精管( seminiferous tubules )中產生。睾丸的各個組成部分以及整體的功能都受到下丘腦 - 腦垂體內分泌腺體的影響。另外,睾丸局部的自分泌、旁分泌調節機制在睾丸的生精功能調控中也起到重要的作用。
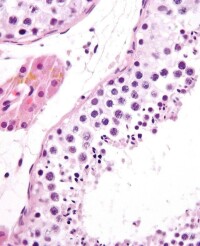
生精小管與成熟精子(蘇木精-伊紅染色)
精睾丸曲細精管。曲細精管共約佔睾丸積 % ~ % ,含生精細胞及管周細胞和支持細胞( Sertoli 細胞)。
曲細精管殊固層( )包繞,包括膠層( )構基底膜管周細胞( )(稱肌纖維細胞)。支持細胞精皮壁細胞。該細胞管壁基底膜延伸曲細精管管腔。廣義言,精皮支持構。支持細胞延伸精皮層,沿支持細胞胞,精原細胞發育至成熟精子的所有形態、生理變化過程都在此發生。支持細胞影響精子發生的過程。另一方面,生精細胞可以調控支持細胞的功能。支持細胞可決定睾丸的最終體積和成人的精子生成數量。
在靠近基底膜一側,支持細胞形成了特殊的膜性結構使細胞彼此之間相互連接,消除細胞間隙(閉塞性緊密連接),構成了血睾屏障的存在。功能完備的血睾屏障依賴於支持細胞的發育成熟,並且在精子生成障礙時血睾屏障功能發生紊亂。血睾屏障可能具有兩個重要的功能:隔離精子使其避免免疫系統的識別;提供減數分裂和精子發生的特殊環境。
精子發生過程起始於生精幹細胞的分化,終止於成熟的精子形成。不同的生精細胞在曲細精管中按照特殊的細胞聯繫排列,形成所謂的精子發生過程。
全部精子發生過程可以被分為 3 個過程
精原細胞位於生精上皮的基底部,分為 A 、 B 兩種類型。 A 型精原細胞進一步分為 Ad 型和 Ap 型精原細胞。在正常情況下, Ad 型精原細胞不發生任何有絲分裂,應該被視為精子發生的精原幹細胞; Ap 型精原細胞則通常分化增殖為兩個 B 型精原細胞。 B 型精原細胞分裂增殖為初級精母細胞,隨後,初級精母細胞開始 DNA 合成過程。
精母細胞經歷了減數分裂的不同階段。粗線期時 RNA 的合成十分活躍。減數分裂的結果產生單倍體生精細胞,又稱精子細胞。在精子生髮過程中,減數分裂是一個非常關鍵的過程,在這個階段,遺傳物質相互重組、遺傳物質只複製一次,細胞連續分裂兩次,最終形成染色體數目減少一半的精子細胞。次級精母細胞產生於第一次分裂后,含有雙份單倍體染色體。在第二次分裂精母細胞演變為單倍體的精子細胞。第一次分裂前期大概持續 1 ~ 3 周,而除此之外的第一次分裂的其他階段和第二次分裂在 1 ~ 2 天之內完成。
第二次分裂后形成精子細胞,是沒有分裂活性的圓形細胞。圓形的精子細胞經過複雜的顯著變化轉變為不同長度的精子細胞和精子。在第二次分裂中,細胞核發生的聚縮和塑性,同時鞭毛形成和胞漿明顯擴張。全部精子細胞變形的過程稱為精子形成。
精子生成過程在時間和空間上有嚴格的順序性。曲細精管中不同成熟階段的生精細胞在管腔中連續、依次排列,提示精子生成過程按照順序依次從第一階段到第二階段,再到第三、第四階段。這個順序稱為生精波( spermatogenic wave )。在人類以及某些猴的部分睾丸組織中,曲細精管的同一轉化部位也可以同時存在多個精子成熟階段。曲細精管同一局部的精子生成過程呈螺旋樣相互聯繫。
除了精子發生的時間和各個階段的空間分佈特徵之外,人類的精子發生還表現出另外一個特徵:人類的生精細胞數目相對較少,同樣,每個支持細胞相對應的生精細胞數目也較低。上述因素以及精子與支持細胞較低的比率( 1 : 5 )導致人類的精子生成數目相對較少。人類每克睾丸組織在 24 小時內生成的精子數目 300 ~ 700 萬。
生精細胞的增殖和分化過程都遵循一個嚴格的模式,所有生精細胞的發育和分化都經過幾個獨立而又緊密聯繫的過程。生精上皮按照程序成功完成每一個發育階段稱為生精上皮周期,每個周期需要 16 天,人類的精子發育到成熟必須經過四個周期,可以推測起碼需要 64 天。
精子發育成熟釋放到曲細精管管腔的過程稱為精子釋放,而這些過程受到多種因素的影響,包括血纖維蛋白溶酶原、激素、溫度、毒性物質。未釋放的精子將被支持細胞吞噬。
睾酮可以抑制LH、FSH的分泌。對於 FSH ,抑制素 B 是更為重要的調節物質。 LH 促進睾丸間質細胞合成睾酮, FSH 則控制支持細胞的調節精子生成作用。睾酮在睾丸間質中的作用對於精子發生過程也十分重要。
精子發生的初次生精過程一般在 FSH 和 LH 的影響下完成。但是高濃度的睾酮單一作用也可以誘導精子發生。在睾酮分泌型睾丸間質細胞瘤的腫瘤附近和 LH 受體激活性突變的患者體內,都可以見到完整的精子發生過程。非常關鍵的治療目的就是試圖在睾丸間質中聚集高濃度的睾酮。臨床常用的辦法是使用hCG,它具有較高的 LH 和 FSH 活性。激素在生精維持、生精再激活中同樣有重要作用。大劑量睾酮通過負反饋機制抑制促性腺激素的分泌,並導致射精中的精子數量大量減少;即使使用 FSH 后精子生成數量也只能達到正常數量的 30%。與之相似,使用 hCG 后也可以造成生精數量減少,其機制是由於 hCG 刺激產生的睾酮發揮了負反饋抑制,但是其抑制生精的作用不如單獨使用睾酮的效果明顯。而且, hCG 的生精抑制作用可以在使用 FSH 后完全恢復。 hCG 和睾酮抑制生精的效果差異是由於在睾丸間質中睾酮的濃度更高。
使用抗體免疫中和 FSH 可以明顯減少靈長類動物以及男子人類的精子發生。在抑制內生性促性腺激素分泌后, FSH 可以持續地維持生精過程。最近的證據發現在腦垂體切除的患者中,在缺少 LH 、 FSH 受體激活性突變的情況下,生精功能可以正常存在。儘管還不知道睾丸間質的睾酮濃度,但是這例患者提示 FSH 受體結構激活對於正常生精是十分必要的。推測睾酮的作用可能是激活 FSH 受體,使 FSH 與其結合后發揮作用。
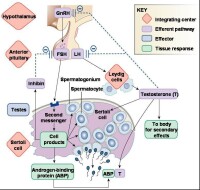
精子發生分泌調控流程圖
睾丸的精子生成受到睾丸局部調節機制的影響。睾丸局部調控可分為旁分泌、自分泌和 胞內分泌( intracrine )。旁分泌作用通常是指距離較遠的細胞局部之間的相互作用和信號傳遞。但是相互作用還包括睾丸不同部分之間的相互作用。
睾丸產生的局部因子對於激素活性調節可能非常重要;局部因子可以被視為調節激素活性和細胞間信號傳導的物質。具有生理功能的局部調節物質首先要具備以下條件:在睾丸內合成、在活體睾丸內發揮作用。具有睾丸局部調控作用的物質因子包括:生長因子、免疫因子、鴉片樣物質、催產素和抗利尿激素,曲細精管管周細胞調節物、腎素、血管緊張素、GHRH、CRH、GnRH、鈣調蛋白、血漿銅藍蛋白、轉運蛋白、糖蛋白、血漿酶原激活物、強啡肽和PACAP等。研究發現這些睾丸功能調節物質處於一種過量儲備狀態,可以在這些物質缺乏時起到補償作用。
睾酮在睾丸內既作為內分泌激素,又作為局部調節物質(通過旁分泌和自分泌)而存在,具有重要的作用。生長因子與細胞表面受體結合后通過特殊的信號傳導通道而誘導細胞特異的分化過程。參與生精調節的主要生長因子包括:轉移生長因子( TGF- α和 TGF- β)、抑制因子、活性因子、神經生長因子( NGF )、胰島素樣生長因子Ⅰ( IGF- Ⅰ)、表皮生長因子( EGF )。與細胞表面受體結合併刺激細胞分化和增殖的細胞因子包括干擾素、腫瘤壞死因子( TNF )、白介素、白血病抑制因子( LIF )、幹細胞因子( SCF )、巨噬細胞移動抑制因子( MIF )等。
精子發生的激素調控 精子發生受垂體分泌的促黃體生成素(LH)、促濾泡生成素(FSH)以及睾丸間質細胞分泌的睾酮調控。間質細胞又稱Leydig細胞,位於各曲細精管之間的間質組織中,它們合成和分泌睾酮進入曲細精管,促進精子發生。睾酮的產生受垂體釋放的LH的控制。垂體分泌的 FSH則刺激支持細胞合成和分泌雄激素結合蛋白,它與睾酮有強的親和能力,以保持睾酮在曲細精管中的濃度,維持它對精子發生的作用。此外FSH還能直接啟動精原細胞分裂和激發早期生殖細胞的發育。
精子發生期間染色質濃縮,使 DNA不能夠轉錄,這種情況在精子完全形成之前完成。各種動物在精子形成中轉錄停止的時刻不完全相同。例如在果蠅,RNA合成在初級精母細胞期間停止,而在小鼠,在成熟分裂后不久的精子細胞中還在進行,要在細胞核開始伸長時才完全停止。