新活素
白色粉末或塊狀物
新活素(凍乾重組人腦利鈉肽),本品適用於患有休息或輕微活動時呼吸困難的急性失代償心力衰竭患者的靜脈治療。按NYHA分級大於Ⅱ級。
新活素
非活性成分:8mg甘露醇、1.73mg磷酸氫二鈉、0.93mg磷酸二氫鈉、9mg氯化鈉。
白色粉末或塊狀物。
0.5mg/支。
使用方法
採用按負荷劑量靜脈推注本品,隨後按維持劑量進行靜脈滴注。
推薦的常用劑量
本品首先以1.5μg /kg靜脈衝擊后,以0.0075μg /kg/min的速度連續靜脈滴注。
劑量範圍
負荷劑量:1.5-2ug/kg,維持劑量速率:0.0075-0.01ug/kg/min(建議開始靜脈滴注的維持劑量速率為:0.0075ug/kg/min)。調整增加滴注給葯速率需謹慎。
用藥方式
本品國內臨床試驗採用連續靜脈滴注24小時的給藥方式。
劑量調整的最佳方法
在給葯期間應密切監視血壓變化。如果在給葯期間發生低血壓,則應降低給藥劑量或停止給葯並開始其它恢復血壓的措施(如輸液、改變體位等)。由於重組人腦利鈉肽引起的低血壓作用的持續時間可能較長(平均2.2小時),所以在重新給葯開始前,必須設置一個觀察期。
靜脈用藥液的製備
不得與其他廠家同類產品混用。盡量使用同批號產品。
從裝有250ml稀釋液的輸液袋中分3次抽取稀釋液(推薦稀釋液:5%葡萄糖注射液、0.9%生理鹽水、含5%葡萄糖和0.45%NaCl注射液、含5%葡萄糖和0.2%NaCl注射液),每次抽出1.5ml,分別加入到3個重組人腦利鈉肽的製劑瓶中(若患者的體重比較輕,沒有必要同時稀釋三支藥物時,可以採用:從裝有100 ml稀釋液的輸液袋中抽取稀釋液16.7ml棄用,並在從該輸液袋中抽出1.5ml,加入到其中的一支重組人腦利鈉肽的製劑瓶中,若需要第二支藥品時,再按照上述方法進行稀釋)。
勿震搖藥瓶,輕輕地搖動藥瓶,使瓶中包括瓶塞在內的所有部分都能與稀釋液接觸,保證藥物充分溶解,只可使用清澈無色的溶液。
從3個藥瓶中分別抽出溶解后的重組人腦利鈉肽藥液,全部注入到容量為250ml的靜脈輸液袋中,此時在輸液袋中本品的藥物濃度大約為6μg/mL。反覆翻轉輸液袋,使藥物充分混勻(對採用100ml輸液袋的體重較輕患者,從已經初步稀釋的一個藥瓶中抽出溶解后的重組人腦利鈉肽藥液,全部注入到上述已經棄用16.7ml稀釋液、規格為100ml的靜脈輸液袋中,此時在輸液袋中本品的藥物濃度大約為6μg/mL。反覆翻轉輸液袋,使藥物充分混勻)。
在患者建立靜脈通路進行靜脈推注和滴注之前,準備一個25mL的輸液針筒。
按照上述方法準備好輸液袋后,抽取給予靜脈衝擊量的重組人腦利鈉肽藥液(見下表),以大約60秒的時間將輸液針筒中的藥液通過靜脈推注入血管,然後以0.0075mL/kg/hr的速率靜脈滴注本品,即滴注的劑量為0.0075μg /kg/min。
換算準確地給予靜脈衝擊的藥液體積及0.0075μg /kg/min的靜脈滴注的速率,可參考以下的公式(或參照以下的給藥劑量表格):
靜脈衝擊劑量(mL)=受試者體重(kg)÷4
靜脈滴注速率(mL/hr)=0.075×受試者體重(kg)
按體重調節rhBNP的靜脈衝擊劑量和靜脈滴注速率
(負荷劑量為1.5μg/kg,靜滴劑量為0.0075μg/kg/min)
患者體重(kg)衝擊劑量體積(ml)靜滴速率(ml/hr)
50 12.5 3.75
60 15.0 4.5
70 17.5 5.25
80 20.0 6.0
90 22.5 6.75
100 25 7.5
110 27.5 8.25
藥物配製后的穩定性
由於藥物中不含防腐劑,必須在24小時內使用溶解后的藥液。無論任何情況下,在使用非胃腸道途徑的藥品之前,應該肉眼觀察藥液中是否存在微粒、變色等情況。溶解后的本品,無論在室溫(20-25°C)或在冷藏(2-8°C)條件下的最長放置時間均不得超過24小時。
配伍禁忌
重組人腦利鈉肽在物理和化學性質上與肝素、胰島素、布美他尼、依那普利拉、依他尼酸(ethacrynate sodium)、肼苯噠嗪和速尿這類注射劑相排斥,不能允許採用重組人腦利鈉肽與這些藥物在同一條靜脈導管中同時輸注。防腐劑偏亞硫酸氫鈉與重組人腦利鈉肽相排斥。因此,含有偏亞硫酸氫鈉的注射藥物不能與重組人腦利鈉肽在相同的輸液管中同時使用。在重組人腦利鈉肽與這些與之相排斥的藥物使用的間期,必須對導管進行沖洗。重組人腦利鈉肽能與肝素結合,能夠與被肝素包被過的導管的內層結合,從而有時就可能降低重組人腦利鈉肽進入患者體內的量。因此,禁止採用肝素包被過的導管輸注重組人腦利鈉肽。但分別採用單獨的導管同時輸注肝素是允許的。
新活素
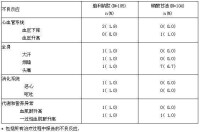
表1.研究過程中發生被認為與用藥相關的不良反應
禁用於對重組人腦利鈉肽中的任何一種成分過敏的患者和有心源性休克或收縮壓<90mmHg的患者。應避免在被懷疑有或已知有低心臟充盈壓的患者中使用重組人腦利鈉肽。
一般注意事項:
應該適當預防本品在採用注射方式給葯時可能有過敏等反應的發生。目前還沒有在採用重組人腦利鈉肽治療時出現嚴重的過敏反應發生的報道。不建議那些不適合使用擴血管藥物的患者如:那些有嚴重瓣膜狹窄、限制性或阻塞性心肌病、限制性心包炎、心包填塞或其它心輸出依賴靜脈迴流或被懷疑存在心臟低充盈壓的患者(見禁忌症)。
腎功能:
在一些敏感人群中,重組人腦利鈉肽可能對腎臟功能有影響。在那些腎臟功能可能依賴於腎素-血管緊張素-醛固酮系統的嚴重心衰患者,採用重組人腦利鈉肽的治療可能引起高氮血症。急性腎衰和需要進行腎透析時,請監測血液生化指標,特別是血清肌酐升高情況。
心血管:
在國外進行的VMAC試驗和在國內進行的臨床試驗,採用重組人腦利鈉肽治療均有低血壓的發生。當出現低血壓時,重組人腦利鈉肽治療組癥狀性低血壓的持續時間(平均2.2小時)比硝酸甘油治療組更長(平均0.7小時)。因此,在採用重組人腦利鈉肽治療時,應該密切監視血壓。當低血壓發生時,應該降低給藥劑量或停止給葯。基線期血壓<100mmHg的患者出現低血壓的發生率更高,因此,在這類患者中採用重組人腦利鈉肽治療應更加謹慎。當重組人腦利鈉肽與其它可能造成低血壓的藥物合用時,低血壓的發生率可能增加。
過敏試驗:
目前在國內外的臨床試驗中均未發生過有關本品的過敏反應報道,並在上市后的實際應用中也沒有對患者進行過敏試驗。
實驗室檢查:
在臨床試驗中,僅發現過1例患者有一過性血肌酐升高的現象。
對死亡率的影響:
與最重要的對照葯硝酸甘油比較,本品也表現出與國外產品大致相同的趨勢。對於死亡率的影響尚待臨床進一步研究。
藥物濫用和依賴:
目前國內外均未專門進行過這方面的研究。
目前國內外均未進行過重組人腦利鈉肽在動物發育和生殖毒性方面的研究,也並不知道採用重組人腦利鈉肽對懷孕婦女進行治療時是否產生胎兒毒性或影響生殖功能。因此,只有當醫生判斷採用重組人腦利鈉肽的治療所產生的益處大於對胎兒的風險時,才能使用。目前也未知這種藥物是否從人類乳汁中分泌。因此,在採用重組人腦利鈉肽對哺乳期婦女治療時,應慎重使用。
目前國內外均未確定重組人腦利鈉肽在兒童患者中使用時的安全性和有效性。
未發現老年患者和年輕患者在使用重組人腦利鈉肽時存在差異。
儘管在國內外的臨床試驗中,存在許多藥物與重組人腦利鈉肽合用的情況,但目前還沒有進行過專門的試驗來證實注射用人腦利鈉肽與其它藥物的相互作用。除了觀察到同時採用口服血管緊張素轉換酶抑製劑與重組人腦利鈉肽合用時癥狀性低血壓的發生率升高外(見注意事項:心血管),還沒有觀察到其它的藥物相互作用現象。本品未排斥利尿劑使用。重組人腦利鈉肽曾經和其它藥物包括:利尿葯、地高辛、口服血管緊張素轉換酶抑製劑、抗凝葯、口服的硝酸鹽類藥物、他汀類藥物、第三類抗心律失常藥物、β-受體拮抗劑、多巴酚酊胺,鈣通道拮抗劑、血管緊張素II受體拮抗劑以及多巴胺合用,儘管沒有進行過專門的對血流動力學參數影響的評價,但沒有證據提示存在任何有臨床意義的血流動力學參數的相互影響。目前還沒有評價過與靜脈注射用擴血管藥物如:硝酸甘油、硝普鈉、米力農或靜脈注射的血管緊張素轉換酶抑製劑合用的情況。
藥物過量的可預期的反應為過度的血壓降低,發生這種情況時,可採取停止給葯、降低劑量和適當的監測手段。嚴重時,可採取擴容治療。
藥物類別
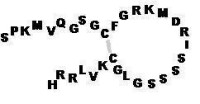
人腦利鈉肽是B型利鈉肽,為人體分泌的一種內源性多肽,在病因誘導下發生心力衰竭後人體應激大量產生的一種補充代償的機制。本品為一種通過重組DNA技術用大腸桿菌生產的無菌凍干製劑,與心室肌產生的內源性腦利鈉肽有相同的氨基酸序列。
作用機制
人腦利鈉肽與特異性的利鈉肽受體(該受體與鳥苷酸環化酶相偶聯)相結合,引起了細胞內環單磷酸鳥苷(cGMP)的濃度升高和平滑肌細胞的舒張。作為第二信使,cGMP能擴張動脈和靜脈,迅速降低全身動脈壓、右房壓和肺毛細管楔壓,從而降低心臟的前後負荷,並迅速減輕心衰患者的呼吸困難程度和全身癥狀。
腦利鈉肽是腎素-血管緊張素-醛固酮系統(RAAS)的天然拮抗劑,它可以拮抗心肌細胞、心纖維原細胞和血管平滑肌細胞內的內皮素、去甲腎上腺素和醛固酮。它可以提高腎小球濾過率,增強鈉的排泄,減少腎素和醛固酮的分泌,以抵制後葉加壓素及交感神經的保鈉保水、升高血壓作用。腦利鈉肽參與了血壓、血容量以及水鹽平衡的調節,增加血管通透性,降低體循環血管阻力及血漿容量,從而降低了心臟前、后負荷,並增加心輸出量。本品沒有正性肌力作用,不增加心肌的耗氧。
臨床藥理
整個試驗共在全國12家心血管臨床研究基地進行,共計209例受試者隨機入組並接受藥物治療(本品組105例,對照組104例),其中導管組103例(本品組51例,對照組52例),非導管組106 例(本品組54例,對照組52例)。
療效分析方面,血流動力學指標評估,用藥前後肺毛細血管楔壓(PCWP)比較, (ITT)人群分析,本品組和對照組在用藥后均呈現下降趨勢。本品組在用藥24小時結束時肺毛細血管楔壓(PCWP)平均下降9.13mmHg,對照組在用藥24小時結束時肺毛細血管楔壓(PCWP)平均下降4.56mmHg,兩組間變化值比較,具有顯著差異(P=0.0368)。符合方案人群(PP人群)分析,兩組間變化值比較,具有顯著差異(P=0.0368)。
本品組肺動脈壓(PAP)檢測值的調整平均值在用藥30分鐘,1小時,2小時及24小時,與對照組相比均有顯著差異(P<0.05),在用藥24小時,試驗組和對照組的PAP檢測均值分別下降10.82mmHg及4.09mmHg。兩組間其它時間點的PAP檢測值無統計學差異(P>0.05)。
CI檢測值的均值變化,重組人腦利鈉肽組在用藥1小時及用藥24小時各上升0.05L/min/m2,對照組分別上升0.11L/min/m2與0.10 L/min/m2,但試驗組和對照組在用藥1小時及用藥24小時的CI檢測均值變化值的統計學比較,均無顯著差異。
RAP檢測值的均值變化,本品組在用藥1小時和用藥24小時,分別下降2.55mmHg與4.83mmHg,對照組在用藥1小時上升2.57mmHg,在用藥24小時下降1.19mmHg。但本品組和對照組在用藥1小時及用藥24小時的RAP調整平均值的統計學比較,均無顯著差異。
血流動力學結果顯示,在24小時用藥期間,對血流動力學功能的改善明顯優於硝酸甘油的作用。
兩組間用藥24小時結束時呼吸困難及全身臨床狀況好轉率的比較,ITT人群和PP人群分析,本品組的呼吸困難及全身臨床狀況好轉率明顯高於對照組(P<0.05)。在用藥30分鐘,1小時,2小時,4小時,8小時,12小時時間點的兩組間呼吸困難好轉率比較,重組人腦利鈉肽組亦明顯高於對照組(P<0.05)
非臨床毒理研究
猴急性毒性試驗:
該試驗觀察本品靜脈滴注給葯對猴的急性毒性,劑量為 0.720 mg/kg-3.645 mg/kg,觀察14天,未觀察到其它急性毒性反應。
猴長期毒性試驗:
觀察連續靜滴本品30天對恆河猴的長期毒性。方法:24隻健康恆河猴雌雄分別按體重隨機分為4組:空白對照組、低劑量組、中劑量組、高劑量組,每組6隻,雌雄各半。低、中、高三劑量組給藥量分別為0.03、0.09和0.3 mg/kg。每天上午餵食前將藥物注入50 ml研製單位提供的溶媒中靜滴,連續30天,空白對照組靜滴等量研製單位提供的溶媒。末次給葯后1天處死一半動物做病理解剖,另一半停葯後繼續觀察15天。觀察癥狀和各項檢測指標。
試驗結果表明:
本品對猴心血管、泌尿系統的影響主要表現為降血壓、利尿。本品對猴藥理毒性作用的靶器官為:肝臟及腎臟,其作用均是可逆的。臨床使用時應密切注意本品對血壓、肝、腎功能的影響。
致癌性和遺傳毒性試驗:
目前國內外均未對重組人腦利鈉肽的致癌性和遺傳毒性進行過專門的研究。
本品人體葯代動力學尚無系統的國內研究資料。
清除:
人體內的人腦利鈉肽以下三種獨立的機制從循環系統中清除(按重要性大小進行排序):1)通過與細胞表面的清除性受體結合隨後進入細胞內並被溶酶體中的蛋白酶水解;2)多肽被內肽酶如在血管內皮上的中性內肽酶所水解切割;3)通過腎臟過濾清除(<2%)。
特殊人群:
儘管重組人腦利鈉肽部分通過腎臟清除,但臨床試驗的數據表明伴有腎功能不全的患者並不需要進行劑量調整。在伴有慢性腎功能不全的患者(血清肌酐範圍:2 mg/dL 至4.3 mg/dL)和有正常腎功能的患者之間,重組人腦利鈉肽對肺毛細管楔壓(PCWP)、心指數(CI)和血管收縮壓(SBP)的影響並不存在顯著的差異。該藥物的清除並不明顯受年齡、性別、內源性腦利鈉肽的基礎濃度、充血性心力衰竭的嚴重程度(以PCWP的基礎值、CI的基礎值以及NYHA的分級標準分級)等因素的影響。
室溫下(不超過30℃)避光貯藏,2-8℃條件下保存最佳。
玻璃管制注射劑瓶。
18個月.
國家食品藥品監督管理局標準YBS00502005
國葯准字S20050033
成都諾迪康生物製藥有限公司
2009年11月10日
2009年6月26日