抗逆轉錄病毒藥物
藥品
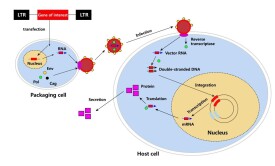
獲得性免疫缺陷綜合征(艾滋病,AIDS)是由人免疫缺陷病毒(HIV)引起的嚴重傳染性疾病。HIV是一種逆轉錄病毒,其逆轉錄過程就是在病毒逆轉錄酶的作用下,以病毒RNA為模板合成前病毒DNA的過程。抗逆轉錄病毒藥是一類於治療逆轉錄病毒(主要HIV)感染的藥物。
美國國立健康研究院(NIH)和一些其他組織推薦有AIDS相關癥狀的患者,使用抗逆轉錄病毒藥物治療。然而,由於藥物複雜的搭配和服用方法,以及可能產生的嚴重副作用,更重要的還有病毒對藥物產生的耐藥性,這些組織也強調需要分析這種治療對沒有癥狀的患者帶來的風險和益處來選擇治療方法。不同種類的抗逆轉錄病毒藥物作用在HIV生命周期的不同階段。
目前國際上共有6大類30多種藥物(包括複合製劑),分為核苷類逆轉錄酶抑製劑(NRTIs)、非核苷類逆轉錄酶抑製劑(NNRTIs)、蛋白酶抑製劑(PIs)、整合酶抑製劑(raltegravir)、融合酶抑製劑(FIs)和CCR5抑製劑。
核苷類逆轉錄酶抑製劑(NRTIs)
NRTIs化學結構與天然核苷相似,在細胞內磷酸化後生成活性代謝產物,通過競爭性抑制天然核苷與HIV1反轉錄酶結合,阻礙HIVcDNA生成,從而抑制HIV複製。國內現有的NRTIs有齊多夫定、拉米夫定、去羥肌苷、司他夫定、阿巴卡韋、替諾福韋、恩曲他濱。
(1)阿巴卡韋
自1989年,阿巴卡韋就和其他抗逆轉錄藥物一起用於艾滋病防治,大約5%的初用患者在使用2周後會產生超敏反應,引起發熱、全身乏力、胃腸道不適,然後出現皮疹,部分患者若再次給予阿巴卡韋將很容易產生致命性不良反應。
(2)司他夫定
司他夫定(d4T)在體內被代謝成三磷酸司他夫定(d4T-TP)產生抗病毒活性,細胞內的d4T-TP水平的改變可能導致司他夫定療效和毒性的改變。研究表明,胸苷酸合酶(TS)基因多態性可影響d4T-TP細胞內濃度,TS低表達患者服用司他夫定后,外周血單核細胞內d4T-TP明顯升高,同時,脂質異常危險性增加。
非核苷類逆轉錄酶抑製劑(NNRTIs)
NNRTIs類藥物通過非競爭性與HIV1反轉錄酶結合,阻礙病毒複製,從而產生抗病毒作用。這類藥物主要由肝臟和腸壁的細胞色素酶P450酶系生物轉化,因此,NNRTIs與其他藥物合用時易產生藥物相互作用。國內現有NNRTIs有奈韋拉平、依法韋倫、依曲韋林。
(1)依法韋倫。依法韋倫是世界範圍內應用最廣泛的NNRTIs之一,常與另兩種NRTIs合用來治療艾滋病。CYP2B6是依法韋倫羥基化的主要代謝酶,參與77%~92%的依法韋倫代謝。有研究表明,CYP3A4、CYP3A5、CYP2A6和UGT2B7也參與部分依法韋倫的代謝。其他一些細胞色素酶也可能參與依法韋倫的代謝,包括CYP2D6、CYP2C9、CYP2C19和CYP2C8,但這些酶的作用還沒完全明確。代謝酶的基因多態性可能導致依法韋倫葯代動力學參數在個體間的較大差異。目前,對CYP2B6基因多態性引起的依法韋倫血葯濃度改變的研究最為深入,現已發現30多個CYP2B6的等位基因,一些等位基因可引起CYP2B6功能的減弱或喪失。被廣泛研究的單核苷酸多態性位點(SNP)為CYP2B6516G>T,該突變可引起依法韋倫和奈韋拉平慢代謝,增加其血葯濃度水平,加強抗病毒能力,同時,也可能導致不良反應發生。另外,CYP2B6983C>T、785A>G、136A>6、1172T>A、499C>G、593T>C、1132C>T也可能引起依法韋倫的慢代謝,而CYP2B618492T>C與依法韋倫的快代謝有關。
(2)奈韋拉平
奈韋拉平主要由CYP2B6和CYP3A4代謝,大量研究表明,CYP2B6516G>T突變與奈韋拉平血葯濃度升高相關,但是這種影響存在一定種族差異。5%的患者服用奈韋拉平后的前幾周可引起超敏反應,表現為皮疹、肝損傷、過敏等,特別是首次使用奈韋拉平且CD4+T細胞>250/mm3的女性患者。研究發現,免疫系統參與超敏反應的發生,人類白細胞抗原(HLA)基因多態性可作為奈韋拉平不良反應預測因子。最新研究發現,在南非人群中HLA-DRB1*0102和HLA-B*5801可能是奈韋拉平肝損傷的危險因素。儘管存在種族差異,但在易感人群中鑒別HLA表型將為最佳治療方法的制定奠定基礎。
蛋白酶抑製劑(PIs)
PIs競爭性阻斷HIV蛋白酶與其天然底物的結合,抑制HIV1後期複製。國內現有PIs有茚地那韋、利托那韋、洛匹那韋、替拉那韋、地瑞拉韋。
(1)洛匹那韋/利托那韋(LPV/r)
LPV/r是常用的PIs類抗逆轉錄病毒藥物,常作為一線抗艾滋病藥物應用於臨床。受細胞色素P450和藥物轉運體P-糖蛋白首過效應的影響,洛匹那韋口服生物利用度低,臨床上常與加強劑利托那韋合用。CYP3A4是蛋白酶抑製劑(PIs)主要代謝酶,同時,PIs又是CYP3A4的競爭性抑製劑。低劑量利托那韋競爭性與小腸和肝臟部位CYP450、P-糖蛋白結合,可以降低洛匹那韋的首過效應,增加其血葯濃度。有機陰離子轉運多肽(OATP/SLCO)是特異性分佈於肝細胞基底膜上的一種轉運蛋白,與體內諸多內源性或外源性物質的肝臟攝取作用關係密切。
整合酶抑製劑
國內現有整合酶抑製劑僅有拉替拉韋。
(1)拉替拉韋
拉替拉韋是第一個被FDA批准可應用於臨床的整合酶抑製劑,通過抑制病毒DNA共價結合到宿主基因組而發揮抗病毒作用。拉替拉韋的主要代謝酶為UDP葡萄糖醛酸轉移酶1A1(UGT1A1),因此人們推測UGT1A1基因多態性可能會影響拉替拉韋葯代動力學參數。已經證實UGT1A1*28等位基因可以降低UGT1A1活性,但兩個以健康人群為研究對象探索UGT1A1基因多態性與拉替拉韋血葯濃度關係的研究並沒有發現其對拉替拉韋血葯濃度的影響。研究發現在患者和健康受試者中的研究發現,UGT1A9*3也許可以解釋部分拉替拉韋個體間血葯濃度差異。
抗逆轉錄病毒藥物治療的指導方案變更過很多次。早期推薦使用“hit hard,hit early”方式,即早服用並大劑量服用。更保守的方法接踵而來,起點定在每毫升350至500 CD4+ T細胞。最近的指導方案用新的標準來考慮使用(雞尾酒療法)HAART治療。
當前,世界衛生組織給出的抗逆轉錄病毒藥物治療(ART)指導方案推薦在發展中國家使用,HIV感染的成年和青少年應該在HIV感染被確認后,並且符合下面任意條件時使用:
晚期HIV病症 WHO規定的HIV IV期,不考慮CD4細胞計數; WHO規定的HIV III期,輔助考慮CD4細胞計數少於350/µl來做出決策; WHO規定的HIV I期和II期,CD4細胞計數少於200/µl。美國的治療指導由美國衛生部(DHHS)制定。適合青少年和成年人的最新指導方案在2005年10月6日出台。
不考慮CD4陽性T細胞計數,所有有艾滋病病史,或和有HIV感染嚴重癥狀的病人可以使用抗逆轉錄病毒藥物治療。。沒有癥狀的病人但CD4陽性T細胞數在200/µl以下的,依舊建議使用抗逆轉錄病毒藥物治療。 CD4陽性T細胞數在201-350/µl的無癥狀病人應該接受該治療。 CD4陽性T細胞數大於350/µl,並且血漿中HIV RNA大於100000/ml的病人,許多有經驗的醫師會推遲治療,但一些醫師會考慮開始治療。該病人的CD4陽性T細胞數大於350/µl,並且血漿中HIV RNA小於100000/ml時,可以考慮延緩治療。以下是首選的任一種服用方法:
efavirenz + lamivudine或者emtricitabine + zidovudine或者tenofovir;或者 lopinavir輔助ritonavir + zidovudine + lamivudine或者emtricitabine 因為HIV在兒童中的病程進展比成年人的快,實驗室參數不能預見病程的危險,尤其對於嬰兒,美國衛生部推薦對於兒童使用更積極的治療方法。適於兒童的新治療方案在2005年11月3日出台。
2005年,美國傳染病預防部(Centers for Disease Control and Prevention in the United States)推薦接觸HIV病毒的人群用28日抗HIV藥物來預防。服用藥物對與在開始的24小時暴露於病毒的人預防有效率達到100%,72小時之內服用的有效率降到52%。
2012年9月,美國研究員黛博拉·佩爾紹德(Deborah Persaud)發現,一名嬰兒使用了高劑量的抗逆轉錄病毒藥物,經過五個月未接受藥物治療,隨後她對嬰兒進行了全面檢查,並發現嬰兒體內已經沒有HIV病毒了,隨後於2013年3月將這一研究結果發表,引起了媒體的關注。
HIV病毒在短短的1.5天里,完成了進入細胞,複製遺傳物質,組裝新病毒,釋放感染其他細胞的過程。HIV病毒在從RNA到DNA逆轉錄的過程中缺乏糾正錯誤的酶。在這種短周期中的高錯誤率使病毒的突變十分迅速,帶來了HIV病毒高的遺傳突變率。多數的變異與親代病毒相比沒有優勢,但有些突變繼承了親代的優勢,讓病毒更容易抵抗人體的免疫系統和抗逆轉錄病毒藥物的防禦。病毒的活性越高,對抗逆轉錄病毒藥物的耐藥性越強,因此抗逆轉錄病毒藥物聯合用藥對於壓制HIV病毒繁殖,對抗病毒的抗藥性是十分重要的。
若抗逆轉錄病毒藥物使用不當,這些抗藥性的菌株會快速成為主要的基因型。不正確的使用逆轉錄抑製劑,例如:zidoyudine,didanosine,zalcitabine,stayudine,和lamivudine,會導致產生多重抗藥性突變。這些突變包括V75I,F77L,K103N,F116Y,Q151M,及M184V突變。這些突變在proteaseinhibitor被廣泛使用前就被發現了,而這些突變對於早期的蛋白酶抑製劑-saquinavir保有敏感性,並且也對現在很少用到的逆轉錄抑製劑-foscarnet具有敏感性。
抗逆轉錄病毒聯合治療法是為了儘可能地抑制HIV病毒的複製。
抗逆轉錄病毒藥物的聯用為HIV的複製製造的多重的障礙,可以使子代數量保持在較低的水平,並能降低產生優勢突變的可能性。如果一個突變對一種藥物產生了耐藥性,另一些葯還能繼續壓制病毒的複製和變異。單獨的抗逆轉錄病毒藥物(很少有例外)不能長時間的對抗HIV病毒感染;所以必須多種藥物聯用來達到持續的效果。因此,目前的標準治療是利用抗逆轉錄病毒聯合治療藥物。藥物的聯合通常是使用兩種RTIs加上一種NRIs或是proteaseinhibitor。這三種藥物的聯合稱做triplecocktail。
抗逆轉錄病毒藥物聯用有協同的正效應和負效應,這點限制了組合方式的數量。例如,ddl和AZT相互抑制,所以同時服用二者的效果比單獨服用一種要差。其他問題也限制了抗逆轉錄病毒藥物的聯用,包括複雜的劑量表和嚴重的不良反應。
近年來,製藥公司共同努力將這些複雜的配方轉換成更簡單的形式,稱為固定劑量組合fixed-dosecombinations。例如把多種抗逆轉錄病毒藥物組合形成藥片(丸),採取每天服用的方式,大大增加了便利性及長遠的效力。
如果一個HIV感染者對於標準的HAART產生耐藥性,選擇就會受到限制。一種選擇是大量聯用抗逆轉錄病毒藥物,被稱為mega-HAART或者補救性治療。但補救性治療通常會加大藥物的不良反應和提高治療花費。另一個選擇是只用一種或兩種抗逆轉錄病毒藥物,這些藥物可以引導病毒像毒力減小的方向突變。最普遍的對於lamivudine(3TC)的耐藥性突變表現為這樣。因此在病毒耐葯時3TC單獨使用還會有些作用。
如果一個HIV感染者對於抗逆轉錄病毒藥物十分耐受,那麼他的治療會變得十分複雜,病情將惡化。治療方法還在繼續改進藥物進入臨床試驗,然而這類葯推廣的局限性使許多發展中國家的病人無法受益。
用藥假期或者被稱為計劃性間斷治療是有意間斷抗逆轉錄病毒藥物治療。這種間斷治療目的是增強HIV病毒對抗逆轉錄病毒藥物的敏感性。間斷治療試圖改變耐藥性的選擇壓力,從而繁殖出對藥物更為敏感的病毒。不幸的事,HIV的生命周期中有一個階段,DNA是完全整合近人類的DNA。在這個階段耐葯的毒株在一定條件下處於休眠狀態,這期間CD4T細胞在機體沒有被入侵的時候也是處於休眠。當抗逆轉錄病毒藥物再次介入時,那些耐葯的毒株會再度出現。
間斷的治療法
是用來減少抗逆轉錄病毒藥物的使用,從而減少不良反應。間斷治療與治療終端不同,間斷治療是在一個短的周期裡面使用或停用抗病毒藥物。治療方案包括“用一周,停一周”(week-on,week-off,"wowo")和跳過周末的“用五天停兩天”(five-days-on,two-days-off,"foto")。研究者在尋找對不同病人最適合的方案。然而原始數據表明,間斷治療法沒有效果,並導致了藥物的耐受。
HIV病毒能損害胸腺產生正常不同種T細胞的能力,因此長期抑制或甚至消除HIV是否能恢復正常的免疫功能目前還不清楚。而且,快速抑制HIV和免疫系統的部分恢復有些時候會產生危險的超敏反應,免疫重建炎性綜合征。這些領域的研究正在進行中。
服用抗逆轉錄病毒藥物可能產生幾種不良反應。這些藥物能產生嚴重的副作用。服用這些藥物要求在不同的時間服用不同藥物,劑量也不相同,這些年,隨著新葯的出現,服用方法稍微簡化。如果病人忘記服藥,會使病毒的抗藥性得到發展。抗逆轉錄病毒藥物價格也很貴,因此世界上多數的HIV感染者得不到有效的藥物治療。
1.常見不良反應
全身不良反應如不適、乏力;神經系統如頭痛、眩暈、注意力不集中、周圍神經炎;消化系統如噁心、嘔吐、腹痛、腹脹、腹瀉、肝損害;血液系統如血細胞減少、貧血,還有口炎、皮疹、葯疹和變態反應等,此外尚有肌痛、炎性水腫、腎結石、高膽紅素血症等。其中有些癥狀與HIV感染和AIDS本身的癥狀相似,應根據癥狀出現時間與服藥時間先後,給予鑒別和一般處理,嚴重者暫停抗逆轉錄病毒藥。
2.特殊不良反應
包括脂肪消耗、脂肪聚集(如肥軀瘦肢)、混合性脂肪分佈、脂肪萎縮症。
(2)高脂血症
表現有高三醯甘油血症、高膽固醇血症,其不良後果為可能增加冠心病的風險,蛋白酶抑製藥中IDV易於引起,其他5種蛋白酶抑製藥以及一些核苷類逆轉錄酶抑製藥都可引起脂代謝障礙。
(3)糖代謝障礙
表現為有胰島素抵抗、高胰島素血症,可能還有胰腺炎。有增加引發糖尿病的風險。
(4)高乳酸血症
大多數患者用雞尾酒療法后都有輕度高乳酸血症。
(5)骨代謝異常
表現有骨質減少、骨質疏鬆和缺血性骨壞死,只在很少數患者中發生,出現時間是在病毒開始受抑制和CD4細胞有改善之際,有人推測與HAART后的免疫重建有關。
(6)肝損害