分子馬達
納米系統
分子馬達(molecular motor)即分子機械或納米馬達(nano-mot-motor,NMM),是由生物大分子構成,利用化學能進行機械做功的納米系統。
分子馬達,又名分子發動機,是分佈於細胞內部或細胞表面的一類蛋白質,它們的構象會隨著與ATP和ADP的交替結合而改變,ATP水解的能量轉化為機械能,引起馬達形變,或者是它和與其結合的分子產生移動。就是說,分子馬達本質上是一類ATP酶。例如肌肉中的肌球蛋白會拉動粗肌絲向中板移動,引起肌肉收縮。而另外兩種分子馬達:驅動蛋白和動力蛋白,它們能夠承載著分子“貨物”,如質膜微粒,甚至是線粒體和溶酶體,在由微管構成的軌道上滑行,起到運輸的作用。
研究人員把金屬鎳製成的螺旋槳嫁接到三磷酸腺苷酶分子中軸上。當它們被浸於ATP溶液后,其中5個分子馬達轉動了起來,轉速達到每秒鐘8轉。這種馬達只有在顯微鏡下才能被觀察到,其鎳螺旋槳長750納米(一納米為十億分之一米)。根據拍攝到的畫面,可以看到一個塵埃粒子先被旋轉的螺旋槳吸入、再被甩出的情景。
分子馬達主要包括驅動蛋白(kinesin)、肌球蛋白(myosin)、動力蛋白(dynein)、DNA解旋酶、RNA聚合酶(RNA polymerase)和旋轉分子馬達(Rotary Molecular Motor)等,這些蛋白在生物體內參與了胞質運輸、DNA和RNA複製、細胞分裂、肌肉收縮和ATP的合成等一系列重要的生命活動。通常,人們按其運動機制將其分為線性分子馬達和旋轉分子馬達,其中線性分子馬達包括驅動蛋白、肌球蛋白和動力蛋白等等,旋轉分子馬達主要包括ATP合酶、細菌鞭毛以及各種門馬達等等。線形分子馬達的結構都可分為頭部、頸部和尾部。實驗表明,線性分子馬達以hand-over-hand(雙手交替,或者叫做鉸進)的形式運動。這種模式中,蛋白的2個臂交替引導運動,就像人走路一樣兩腳交替前進。
1、驅動蛋白
驅動蛋白(kinesin)是1985年從魷魚的軸質(axonplasm)中分離的一種蛋白,主要存在於真核細胞內,以微管蛋白(microtubule)為軌道。體外實驗證明驅動蛋白的運輸具有方向性,沿微管(microtubule)的負極向正極運動,並由此完成各種細胞內外傳質功能,如運送細胞器和物質小泡,並參與細胞的有絲分裂。驅動蛋白是一個大的複合蛋白,由幾個不同的結構域組成,包括2條重鏈和1條輕鏈,總分子量為380×106。它有1對球形的頭,是產生動 力的“電機”,還有一個扇形的尾,是貨物結合部位。
2、動力蛋白
動力蛋白(Dynein)發現1963年,主要存在於真核細胞內以及鞭毛和纖毛中。它們沿微管負向運動運送物質,並在鞭毛和纖毛的運動中起重要作用。Dynein分子量巨大接近1.5×109,由2條相同的的重鏈和一些種類繁多的輕鏈級結合蛋白構成。它有2個大的球形的頭部,是生成力的部位,它在細胞中至少有2個功能:①是有絲分裂中染色體運動的力的來源;②作為負端微管走向的發動機,擔負小泡和各種膜結合細胞器的運輸任務。研究發現,可能是dynein的頸部在決定運動方向上起著決定性的作用。在細胞分裂中,紡錘體的分離就是在類kinesin馬達和dynein的共同作用下完成的。
3、DNA解旋酶
DNA解旋酶作為線性分子馬達,以DNA分子為軌道,與ATP水解釋放的能量相偶聯,在釋放ADP和Pi的同時將DNA雙鏈分開成2條互補單鏈。解旋酶是一類解開氫鍵的酶,由水解ATP來供給能量。它們常常依賴於單鏈的存在,並能識別複製叉的單鏈結構。在細菌中類似的解旋酶很多,都具有ATP酶的活性,大部分的移動方向是5′→3′,但也有3′→5′移到的情況。
4、肌球蛋白
肌球蛋白是微絲結合蛋白,最早發現於肌肉組織,1970年後逐漸發現許多非肌細胞的肌球蛋白。其家族有13個成員,每個成員在結構上都分為頭,頸和尾部三個部分,形似豆芽,而組成上則有輕重兩種鏈。其中的調節輕鏈是肌球蛋白接受調解的位點,就是說,調節輕鏈的磷酸化/去磷酸化狀態影響著肌球蛋白的活性。其中Ⅰ和Ⅱ型是研究得最徹底的分子馬達。一些細胞具有突變的肌球蛋白,它們能正常伸出偽足,但是卻不能成功移動。Ⅰ型和Ⅴ型則是二聚體。趨向微絲的正極運動。蛋白的頭部能就尾部作屈伸運動,並在“屈”的時候拉動微絲相對向後運動。肌球蛋白除了參與肌肉收縮外,還被認為是細胞遷移所需的重要分子之一。肌球蛋白非常可能參與了“前進的四個步驟”裡面胞體收縮的那一步。另外,在細胞突出一端也可觀察到肌球蛋白,它可能是幫助運輸粘著所需要的蛋白質,提高粘著效率。

分子馬達
分子馬達靠很小的增值來工作,轉入蛋白質構象的改變從而能進行有引導的運動,它需要一條引導馬達裝配的運動軌道進行有規則的運動來通過一段距離。實際上,我們以前已經遇到過一類分子馬達,它利用我們即將涉及的分子機器,即沿著DNA和RNA軌跡運動的解螺旋酶。沿重複同一亞單位組成的蛋白絲(如肌纖蛋白和微管)在高度親緣關係和低親緣關係間的馬達蛋白質的循環,是為使絲狀軌道響應於ATP的結合,水解。ATP的每一次結合、推動、釋放,都是產生運動的機制。
也存在一種完全不同的策略,就像大腸桿菌之類的細菌那樣用來產生運動,一套鞭毛扮演著螺旋槳,在細菌細胞膜中做馬達旋轉,這個旋轉的馬達被一個跨膜的蛋白質濃度梯度所驅動,代替被ATP水解所驅動,一套蛋白質濃度梯度去轉動運動的機理類似於ATP合成酶的F0亞基的作用。但是,儲存生化能量的主要模式都是ATP和離子濃度梯度,被漸進式的利用去驅動有機分子運動。
真核細胞含有三種主要的馬達蛋白家族:肌球蛋白、kinesins蛋白和動力蛋白。在肌肉中的肌球蛋白,開始時被描繪成有它自己的作用基礎,沿著肌纖蛋白的絲運動,肌肉肌球蛋白包括兩個拷貝,它們都有一個87kd分子團的重鏈,一個必需的輕鏈,和一個起調節作用的輕鏈。人類基因似乎能編碼超過40種截然不同的肌球蛋白,在肌肉收縮中有些功能和另一些參與不同種類的其他過程。kinesins蛋白在蛋白質、囊泡和沿微管的細胞器轉運中起作用,包括染色體分離。kinesins蛋白常包括兩個拷貝,一個是重鏈,一個是輕鏈,它的重鏈大約只有肌球蛋白長度的一半。人類基因至少能編碼40種kinesins蛋白。在一些真核細胞中,動力蛋白能驅動纖毛和鞭毛的運動,和其他作用蛋白相比,動力蛋白較大,有個大於500kd的分子團重鏈,人類基因似乎能編碼大約10種動力蛋白。
比較肌球蛋白,kinesins和動力蛋白的氨基酸序列,並沒有出現這些蛋白質家族之間有意義的關係,但是,在確定它們的三維結構之後,肌球蛋白和kinesins家族的成員之間被發現有顯著的相似性,特別是肌球蛋白和kinesins都包含同源的P-環NTP酶核心部位,這些在G蛋白中也存在。動力蛋白重鏈的序列分析揭示出它是P-環NTP酶的AAA子家族的一個成員,我們以前在19S蛋白解體系統中遇到過該子家族,動力蛋白有6個序列編碼一個沿著它的長段排列的P-環NTP酶整環。從而,可以利用有關G蛋白和其他P-環NTP酶的知識來分析這些馬達蛋白的運動機理。

分子馬達
由人類控制的分子馬達可以打造納米機器人(也稱分子機器人)。
目前人類還無法製造納米這麼小的機器人,一部分原因是找不到足夠小的動能裝置。分子馬達既然能把生物能轉化為機械能,一旦被人類完美地控制,就完全可以充當納米機器人的發動機。可以把分子馬達看成一個最簡單的納米機器人,像一種長了兩條“腿”的肌球蛋白分子馬達,可以做線性推進運動,在人體內,它的一大作用是在細胞內搬運小泡等物質,理論上,如果再給它裝個筐,它也能運其他東西。
目前,科學家還在研究怎樣把多個分子馬達組合,或把它們和其他分子聯繫,組成一個稍微“複雜”的機器。在實驗室里,科學家已經做成了由350個原子組成的螺旋槳、2.5納米大小的升降機、3納米的剪刀,這些都可以算是納米機器人的雛形。
納米機器人潛在用途十分廣泛,其中特別重要的就是應用於醫療領域。例如美國佛羅里達大學的科學家最近研製出一種能夠100%地殺滅丙肝病毒的納米機器人。這種納米機器人由兩組物質構成:一組是能夠攻擊並摧毀RNA(參與複製丙肝相關蛋白)的酶,另一部分是一種寡核苷酸,能識別疾病相關蛋白並將酶送過去消除危害。在細胞培養和小鼠實驗中,這個新方法已達到了近乎100%的有效率,且沒有任何副作用,例如免疫系統反應。這項新成果促進了醫療納米機器人的發展,目前也逐步向臨床應用邁進。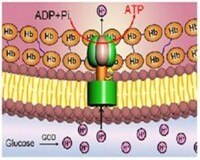

分子馬達
