粘液瘤病毒
粘液瘤病毒
粘液瘤病毒是一種高度接觸性而且高死亡率的疾病,多在兔子身上出現癥狀。多種兔子品種都可感染。
粘液瘤病毒(Myxomavirus)〖BT)〗粘液瘤病毒是高度接觸性並有極高死亡率的疾病。最先發現於南美,隨後發生於墨西哥和美國。50年代后,歐洲各國也有發生。隨著國外種兔的進口,本病傳入我國的危險性甚大,因此必須提高警惕,注意實施檢疫隔離制度。
各種家兔、野家兔(又稱穴兔,Oryctolaguscuniculus)和澳洲野兔(歐洲家兔的後代)對粘液瘤病毒十分敏感。病兔頭部和肛門生殖道部位水腫,發生眼瞼結膜炎,全身具有廣泛分佈的腫瘤樣腫脹。病兔幾乎全部死亡。
本病經常可以摧毀某地區的整個養兔業。烏拉圭和巴西的林兔(Sylvilagusbrasiliensis)是粘液瘤病毒的自然宿主和帶毒者,但其本身只發生少數單在的良性皮膚腫瘤,幾乎沒有死亡病例。但其腫瘤中含有大量病毒,是蚊等昆蟲機械傳播本病的病毒來源。某些野兔,例如北美的加州野兔(Lepuscalifornicus)和某些棉尾兔以及歐洲的褐色野兔(Lepuseuropaeus)和山地野兔(Lepustimidus)等對本病具有完全的抵抗力。
病毒粒子呈磚形。負染時,表面呈串粒狀,由線狀或管狀物質組成。不同株之間病毒基因組的限制性酶切圖譜比較保守。Uriarra(Ur)株、Glenfield(Gv)株和Lansanne(Lu)株粘液瘤病毒基因組全長約為1636kb。除了Lu株病毒基因組388kb位置KpnI位點不同外,這3株病毒EcoRI、KpnI、BamHI、SalI、HindIII、BgII、PstI和PvuII酶的限制性酶切圖譜基本相同。53kbBgII為該病毒基因組的共閉合末端片段。TK基因位於基因組577~593kb之間的16kbSacI-SalI片段上,該片段與相鄰SalI-AA2片段上228bp一起含有4個閱讀框架,其中3個閱讀框架與痘苗病毒L5RJ1R閱讀框架和TK基因相似。第4個閱讀框架MF8a相似於纖維瘤病毒和豬痘病毒的相對於TK基因同一位置的閱讀框架。TK基因、MF8a能被早期轉錄。另一I1L基因位於該病毒基因組保守的中央區域BamHII片段上,編碼雙特異性酪氨酸/絲氨酸磷酸酶,是病毒具有活性的必需因子。
粘液瘤病毒的抵抗力低於大多數其它痘病毒。對熱敏感,不耐pH46以下的酸性環境。50℃30分鐘,55℃10分鐘,60℃以上的溫度於幾分鐘內使其滅活,但病變皮膚中的病毒可在常溫下活存幾個月。如置50%甘油鹽水中,更可長期保持活力。
對乙醚敏感,但能抵抗去氧膽酸鹽。這是粘液瘤病毒獨特的性質。因為其它痘病毒對乙醚和去氧膽酸鹽的敏感性是一致的。
將粘液瘤病毒某些靶基因滅活,構建的重組粘液瘤病毒的致病性減弱。這類基因被稱為病毒毒力因子。目前,粘液瘤病毒已發現了5種這樣的病毒毒力因子。
是由該病毒編碼的一個85個氨基酸殘基組成的多肽。它的羧基區域有40%序列與上皮生長因子(EGF)同源。將滅活MGF的重組粘液瘤病毒接種易感動物,臨床癥狀明顯減弱,伴有輕微呼吸道和結膜上皮細胞增生。用痘苗病毒生長因子、Shope纖維瘤生長因子或鼠α轉化生長因子替代滅活MGF而構建的重組粘液瘤病毒,接種易感動物產生的臨床癥狀和組織病理學變化很難與野毒株粘液瘤病毒區別。從而證明粘液瘤病毒生長因子與其它痘病毒的類似上皮生長因子和細胞生長因子一樣,在粘液瘤病毒致病中具有相似的生物學功能,對靶細胞產生促有絲分裂作用。
SERP1:一種分泌性絲氨酸蛋白酶抑製劑。在感染細胞培養液中分子量為55kDa,具有抑制人纖維蛋白溶解酶、尿激酶和雙鏈組織型纖維蛋白溶解酶原激活因子的生物功能。SERP1基因位於病毒基因組末端,為晚期表達基因。滅活SERP1基因的粘液瘤病毒的致病能力減弱,使50%以上動物恢復健康。病變部位如果沒有SERP1蛋白,就可發生有效的炎症反應,促進感染細胞快速崩解。該毒力因子看來是通過調節炎症反應和與細胞成份反應而呈現致病作用的。
M11L:位於感染粘液瘤病毒細胞表面,類似受體的蛋白質,是早期表達基因,主要生物功能是減少白細胞對粘液瘤病毒產生的腫瘤的浸潤。用滅活M11L重組粘液瘤病毒(vMYXM11L)接種易感動物時,產生非致死性臨床癥狀,形成的腫瘤與野毒株的腫瘤相比,更大更局部化,發生更嚴重的巨噬細胞和異嗜性白細胞浸潤。病毒複製部位的水腫和壞死也很嚴重。表明宿主對vMYXM11L感染產生更有力的炎症反應。
T2:一種腫瘤壞死因子受體類似物。具有與腫瘤壞死因子特異性結合的功能,約52~56kDa大小,為病毒早期表達蛋白。T2基因位於粘液瘤病毒基因組末端區域。將滅活T2基因的重組粘液瘤病毒(vMYXT2)接種易感動物,大部分動物完全康復。T2拮抗腫瘤壞死因子發揮致病作用。有人建議將這類由病毒編碼的細胞淋巴因子受體的類似物,命名為“病毒受體”(viroceptor),其主要功能是阻斷同源淋巴因子。
T7:由粘液瘤病毒MT7閱讀框架編碼,是由感染該病毒的細胞分泌的γ干擾素受體類似物。其主要蛋白質序列相似於人和鼠γ干擾素受體。分子量為37kDa,能特異地結合兔的γ干擾素,具有抑制宿主細胞外γ干擾素的生物學作用。
粘液瘤病毒具有8種以上的抗原成分。將病變組織與陽性血清作瓊脂擴散試驗,出現3~5條沉澱線,且與纖維瘤病毒的可溶性抗原發生交叉反應——既有各該病毒特異的沉澱線,也有幾種病毒共有的沉澱線。患纖維瘤后恢復的家兔,雖對粘液瘤病毒的攻擊仍能感染,但病情較輕,且不死亡。病毒抗原引起補體結合、沉澱以及中和抗體。
粘液瘤病毒可與纖維瘤病毒發生遺傳性復活現象。將粘液瘤病毒置75℃加熱或用乙醚處理,使其完全滅活,隨後加入活的松鼠纖維瘤病毒,混合後接種家兔,可因粘液瘤病毒復活而使家兔發生典型的粘液瘤。
粘液瘤病毒可在雞胚絨毛尿囊膜上生長,並常於接種后3天左右產生痘斑樣病變:或則為直徑05~1mm的散在痘斑,或則融合成較大病變。病毒在雞胚中的傳代並不困難,實驗室內常用雞胚絨毛尿囊膜上的痘斑計數法進行病毒滴定。
粘液瘤病毒可在多種組織培養細胞內增殖併產生細胞病變,包括兔、豚鼠、倉鼠、大鼠、雞和人的組織培養細胞。病毒實驗室內最常應用兔腎、兔心和兔皮膚等細胞培養物,原因是其敏感性和病毒產量均高。而在其它細胞中,僅日齡很小的大鼠細胞能夠支持病毒生長,豚鼠細胞也常需要適應1~2代,才能具有較高的病毒產量和產生比較規律的細胞病變。於兔腎細胞培養物內,感染細胞核發生空泡化,並出現嗜酸性胞漿內包涵體。約在接種后5~6天,細胞單層上出現直徑約3mm的蝕斑。
粘液瘤病毒的致病性主要是因產生細胞免疫功能缺陷以及從多方面阻斷細胞因子網路系統。細胞免疫缺陷與粘液瘤病毒明顯減少細胞表面主要組織相容性複合物(HMC)中I類抗原有關。I類抗原介導的提呈病毒抗原作用的顯著降低,嚴重阻礙細胞介導的對粘液瘤病毒的免疫反應。現已證明,粘液瘤病毒的毒力因子在阻斷細胞因子網路系統中發揮重要作用。
如前述,烏拉圭和巴西的野兔是粘液瘤病毒的儲主,蚊是其傳播媒介,被咬部在一周后出現一個局限性腫瘤樣腫脹。腫脹呈良性經過,不發生全身化,持續存在2~3個月。家兔對粘液瘤病毒具有高度敏感性,在被帶毒昆蟲叮咬后,病毒先在局部增殖,並隨淋巴或血流侵入內臟器官,進一步增殖(可能在其小動脈的內皮細胞內)后,再度引起病毒血症。病毒侵入皮膚,因增殖而引起全身性腫瘤樣腫脹。皮下膠樣腫脹發生於感染后的第3~4天。約於第7~8天,腫脹增大,並散佈於全身。病兔大多於出現癥狀后7~15天死亡。
病兔首先出現眼的炎症,眼瞼腫脹,由結膜流出大量分泌物。最初呈漿液性,但迅速變為膿性。病眼於1~2天即因腫脹而不能睜開。鼻孔也有流出物。臉和耳部出現腫脹,頭部可能變形。生殖孔發炎,併流出膿性分泌物。
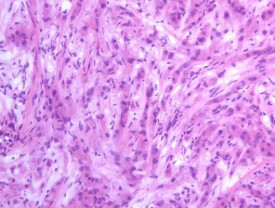
皮膚腫脹物由橡皮樣硬度的膠樣物質組成。淋巴結腫大和出血。將粘液瘤切開檢查,可見到典型的腫瘤組織:同質性的膠樣物內(主要是粘蛋白)含有許多大型的星狀細胞——未分化的間質細胞。腫瘤上皮層變性,上皮細胞腫脹和空泡化,胞漿內含有嗜酸性包涵體。包涵體內有藍染的球菌樣小顆粒——原生小體。粘液瘤病毒對人及其它動物均無致病性。
實驗家兔的死亡率幾乎是100%。在澳大利亞,初次接觸粘液瘤病毒的野兔的死亡率高達90%以上,但在機體和病毒長期多代的相互作用過程中,出現了對粘液瘤病毒具有較大抵抗力的兔以及毒力減弱的毒株,病兔死亡率明顯下降——70%,甚至不到50%。
有些地區隨著兔的抵抗力增加,粘液瘤病毒的毒力也發生變化,英國對1961~1981年之間粘液瘤病毒野毒株的毒力進行調查,發現粘液瘤病毒毒力是逐漸增強的。
中國家兔人工接種粘液瘤病毒,死亡率幾乎達100%。
1971~1978年對英格蘭和威爾士三個地區野兔群感染粘液瘤病毒的調查顯示:每年秋季是發病高峰,隨後在2月~4月病例再次增多。公兔比母兔,成年兔比幼兔更易感染。
40年代前後,澳大利亞兔患嚴重,估計全國約有幾十億隻野兔,大量損壞草原植被,影響畜牧業的發展。1950年,在7個地點同時釋放粘液瘤帶毒兔,希望造成嚴重疫病,達到消滅野兔的目的。但6個地點的試驗都失敗了,只在墨山河谷這一地區引起了野兔的嚴重疫病,於幾十萬畝土地上消滅了野兔。後來發現這主要是因為該地區有大量蚊孳生的緣故。隨後的試驗進一步證明只在潮濕和多蚊地區,粘液瘤病毒才能大量傳播。1952年,一個法國醫生退休到他的農村莊園。為了消滅野兔,他釋放了幾隻粘液瘤病兔。結果不僅消滅了他莊園內的野兔,而且在18個月內傳遍整個法國、比利時、德國和荷蘭,並越過英吉利海峽傳到英國。
粘液瘤病毒-免疫和防制
對於家兔,防蚊和消滅虱、蚤等吸血昆蟲,及時隔離和撲殺病兔,常有防制粘液瘤病發生的明顯效果。
病後耐過兔的血清抗體持續存在達18個月,應用強毒攻擊,或則出現小型的局部病變,或則不發生任何病變。免疫母兔所生的仔兔,也有部分被動免疫力。但是Sobey等(1975)報道,具有母源抗體的仔兔在被帶毒的蚤叮咬或出生後接觸病兔時,仍易發生感染而死亡。其感染率和死亡率與對照兔沒有差別。
應用基因工程手段,滅活或缺失粘液瘤病毒生長因子、SERP1、M11L或T2,構建重組粘液瘤病毒,可明顯降低其致病作用。接種這些重組病毒的易感動物,在恢復后都能抵抗野毒株粘液瘤病毒的攻擊。接種兔纖維瘤病毒,可以導致良性腫瘤,家兔不死,但可耐受粘液瘤病毒的致死性攻擊。
某些國家已將弱毒疫苗進行商品生產,包括應用人胎組織長期培養或在兔腎或皮膚傳代細胞上減毒的疫苗株。
對於典型病例,根據粘液瘤典型的臨床癥狀和病理變化,不難建立診斷。但對毒力較弱的粘液瘤病毒引起的非典型病例,或因兔群具有較高抵抗力,病情或病變不嚴重時,診斷比較困難。可採取病變組織作切片檢查,尋找星狀的“粘液瘤細胞”以及用腫瘤組織接種敏感家兔作感染試驗。必要時可採取病變部組織,作成乳劑後接種雞胚絨毛尿囊膜。隨後再以中和試驗或交叉保護試驗等鑒定之。