心包剝脫術
心包剝脫術
心包剝脫術常用於治療慢性縮窄性心包炎。慢性縮窄性心包炎是累及心包壁層及臟層的慢性炎症過程。引起心包纖維化及增厚,限制心臟的舒張活動,從而降低心臟功能。縮窄性心包炎已有顯著的臨床癥狀者,經過一段時間的治療及休息而無好轉,其自然預后多不良。大部分病人在保守治療條件下很難恢復正常活動能力。Somerville W提出:一旦出現慢性縮窄性心包炎的癥狀及體征。病人在喪失一般活動能力的生存壽命大約為5~15年。當腹水等出現時,病情進展迅速,特別是兒童。有的病人最終以循環衰竭或肝腎功能不全而死亡。因此,一旦確定診斷,外科手術是根本的治療措施,切除縮窄的心包,以使心臟逐步恢復功能。術后心功能的恢復依賴於:①選擇適當時機手術,在纖維鈣化形成之前較易剝離,同時心肌損害也較輕;②心包剝離的範圍,是否能將雙側心室表面的增厚心包完全切除。手術宜在病情相對穩定的條件下實施。所以術前應進行充分、嚴格的內科治療。結核菌引起的縮窄性心包炎,應給予系統的抗結核藥物治療,在體溫、血沉及全身營養狀況接近正常或比較穩定后實施手術。
(1)縮窄性心包炎診斷明確,即應手術治療。
(3)病情嚴重,保守治療無明顯改善者,一些學者主張早行心包開窗術,以改善全身功能狀況,然後進行心包切除術。
(1)老年病人伴嚴重心、肺疾病,不能耐受手術者。
(2)癥狀輕微,病情無進展者。
2.除明確為非結核性縮窄性心包炎之外,應抗結核治療不少於6周,最好為3個月。
3.肝腫大、腹水和周圍水腫明顯者,酌情給予利尿製劑及補鉀,糾正水電解質平衡失調。
4.心率過快者可酌情小劑量應用洋地黃類藥物。
手術前儘可能達到以下要求:
②飲食狀況有所進步;
③心率不超過120次/min,實驗室檢查基本正常,體溫正常及活動能力提高;
④每日尿量比較衡定。
常用的手術徑路有3種:①胸骨正中劈開切口;②雙側胸前橫切口;③左胸前外側切口(圖1)。
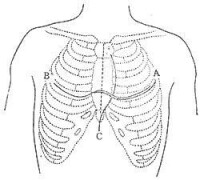
心包剝脫術
A.左側前外切口;B.雙側胸前切口;C.胸骨正中切口
1.胸骨正中劈開切口 此種手術入路能夠充分顯示心臟前面及右側面,易行剝離腔靜脈及右心緣部位的增厚心包,術后對呼吸功能影響小。對合併有肺內病變及呼吸功能較差的病例,多採用此切口。其缺點是,左心室膈神經后的心包部分及心尖部分顯露較差。有學者認為膈神經后的心包不必切除。
3.雙側胸前橫切口 此切口優點是手術野暴露良好,可兼顧心臟左右兩側,能徹底切除心包,術中有意外發生也便於處理。其缺點是切口較長,創傷較大,術后肺功能影響大。
4.經左胸前外側切口心包剝脫術 病人麻醉后取仰卧位,左肩胛下置一枕墊,左手放在壁下(圖2)。沿左側第五肋間隙,左乳腺下方,作一弧形切口。切開肌肉進胸。胸廓內動脈結紮切斷。第五肋軟骨靠近胸骨處斷開。撐開胸廓顯露胸腔。將左膈神經從心包內銳性分離,盡量多帶些脂肪及軟組織,以免傷及膈神經。在左心室部位切開心包,盡量偏後外側,選擇無鈣化區。切口下面有時可見到分層,或有心包積液。但大部分情況下,切開心包即達心肌表面。在心外膜之外找到分層,沿分層進行鈍性或銳性剝離並逐漸擴大範圍。如增厚的壁層與臟層心包間尚有腔隙,可先切除壁層使心臟搏動初步得到改善,再處理纖維增厚的臟層心包。若心包粘連緻密或分層不清,應使用剪刀或刀片進行銳性分離,細緻精確地進行解剖。避免強用純器剝離,以防止心肌創傷及心肌破裂。
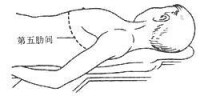
心包剝脫術
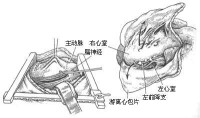
心包剝脫術
圖2 左前外側切口手術操作示意圖
心包剝離的順序應沿縱行切口的兩側,向右前方及左後方分離。應盡量成片切除,如發生心肌破裂,可利用已剝脫的心包修補止血。右側的心包片應分離至左側的房室溝,上界至胸腺的下方。左側的心包片上界應分離至主肺動脈干,並將其縮窄環切斷,以免引起嚴重的術后右心室壓力過高;下界應將膈肌鍵以外的增厚心包完全遊離或切除;后界儘可能將左心室表現的心包完全遊離。在分離室間溝部位時,格外注意勿損傷冠狀動脈分支,此處如有鈣化應給予留置,在其它部位繼續剝離。左心房表面的增厚心包對血流動力學影響不大,剝離時較易撕破,止血困難,不需要強行剝離。儘可能切開松解左心房與下腔靜脈附近的環形縮窄,房室溝處如存在環形縮窄應予切斷。術中應注意先完全剝脫左心室部位的心包,然後剝離右心室流出道,以防發生急性肺水腫。待心包完全剝離之後,再將心包片切除。重症病人心肌萎縮明顯。在剝離心包后,心肌表面顏色較淡,剝離範圍應適可而止,心室表面及主要縮窄環解除即可。剝離完畢即可應用洋地黃製劑。手術結束時要徹底止血,心包切除邊緣用電凝止血。如有必要可在左心耳或肺靜脈置放測壓管,有利於術后病情觀察。安放兩根閉式胸腔引流管。
5.經胸骨正中切口心包剝脫術 採用氣管內插管全身麻醉。患者取仰卧位,背部肩胛骨區墊高使胸部挺出,胸骨正中劈開。如有胸骨后粘連,應邊分離粘連,邊用開胸器撐開兩側胸骨。先自心尖部位開始剝離心包。此外心包粘連輕,心包增厚不明顯,易於剝離。用刀片逐次劃開增厚的心包。增厚的心包與外膜之間常常有一層疏鬆結締組織,為正確剝離心包的分界面。切開增厚心包后,可見跳動的心臟向外突出。分離一部分心包后,助手輕輕用鉗子提起心包片,術者以左手輕壓在心臟表面,可充分顯露增厚心包與心肌粘連的程度。如粘連較疏鬆時,可用手指套紗布或花生米鉗予以鈍性分離,分離時的用力部位應在心包面上。遇到條索或條帶狀粘連時,需用剪刀或手術刀片銳性分離。如粘連愈著十分緊密,應放棄原來的分離部位,而在其它位重新切開、分離心包,即先易后難。根據術中病人心功能狀態及心包粘連程度決定剝離範圍。一般剝離的基本範圍:應是心尖部位需完全剝脫;左側面接近左側膈神經處;房室溝及下腔靜脈入口處的纖維性縮窄環必須松解。剝離的順序應該是左心室→右心室流出道→房室溝縮窄環→下腔靜脈環形束帶。
心包機化良好且非常易於剝離者,心包完全剝離最佳。如術中出現心律失常,循環不穩定或心肌顏色發白,心臟擴大,心肌收縮無力,剝離操作需適可而止,主要部位(左、右心室面及下腔靜脈縮窄環)剝脫即可。同時應用地高辛及利尿製劑,儘早完全手術,以提高手術安全性。術后必要時給多巴胺等正性肌力藥物。
1.低心排:在心包剝離過程中,由於急性心臟擴張,特別是右心室表面心包剝除后,在體靜脈高壓的作用下,心室急劇快速充盈、膨脹,產生急性低心排。因此,術中應限制液體輸入,左心室解除縮窄后,立即應用西地蘭及速尿,在強心的同時,排隊過多液體減輕心臟負擔。術后12~48h之內,應用多巴胺等兒茶酚胺類藥物。如對藥物反應效果較差,低心排不能糾正,可使用主動脈內氣囊反搏。
2.膈神經損傷:左前外側切口在開始心包剝脫之前,應先遊離左側膈神經,儘可能隨同膈神經多保留脂肪及軟組織。如損傷膈神經,可造成膈肌的矛盾呼吸運動,影響氣體交換。不利於呼吸道分泌物的排出。
3.冠狀動脈損傷:在分離前室間溝部位時,要格外注意,勿損傷冠狀動脈。其分支或末端出血,可縫扎止血。遇到該部位有局限的鈣化斑塊時,可以留置不予處理,不可勉強切除。
4.心肌破裂:對於嵌入心肌的鈣化病灶,一般可島形保留,不可勉強剝除。對於剝離界限不清,嚴重粘連時,可將增厚的心包作“井”字切開,部分地解除心肌表面束縛。萬一發生心肌破裂時,術者用左手食指平壓在裂口上,利用遊離的心包片縫蓋在破裂口的周圍,可挽救病人的生命。
3.強心利尿:術後繼續給予利尿藥物,減輕鈉水瀦留,在充分補鉀的條件下,給予洋地黃製劑。嚴格控制液體輸入量。
1.手術死亡率 近年來有所下降,約4%。McCaughan BC報告術前病人的心功能狀態是影響手術死亡率的最重要因素。術前心功能為Ⅰ~Ⅱ級(NYHA)者手術死亡率為0;心功能Ⅲ及Ⅳ級者,手術死亡率分別為10%及46%。術前腹水,周圍水腫,心臟內壓力及低心臟指數的程度對手術死亡率有一定的影響。
2.晚期生存情況 Kirklin JW報告手術后5年及15年生存率分別為84%與59%。McCaughan BC報告5年、15年及30年生存率分別為84%、71%與52%。影響晚期生存的主要因素仍是術前心功能狀態,而與手術入路無明顯關係(圖3)。
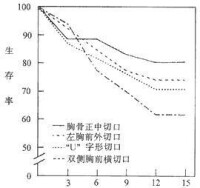
心包剝脫術
圖3 心包剝脫術後晚期生存率
此外,Kirklin報告,採用胸骨正中切口及左側前外側切口,再手術率僅為2%。
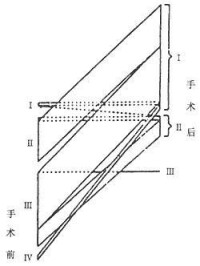
3.術后血流動力學變化 所有病人在安靜狀態下,心功能的各項血流動力學指標均正常。約10%~20%的病人在體力活動時,出現輕微的肺動脈壓力升高,心排量不能代償性增加。如心室表面增厚心包剝脫不全,則血流動力學不能較好地改善。McCaughan BC報告大部分病人遠期效果較好,幾乎全部病人都能達到心功Ⅰ~Ⅱ級(圖4)。
心包剝脫術
