人體胚胎
人體胚胎
人體胚胎學總論或稱人體早期發生,是指從受精 至第八周末的發育時期,即胚前期和胚期。此時期的胚胎髮育變化甚大,並易受內、外環境因素的影響。人體胚胎學總論的內容包括:生殖細胞和受精,卵裂和胚泡形成,植入和胚層形成,胚體形成和胚層分化,胎膜和胎盤。
生殖細胞和受精
(一)生殖細胞
1.精子的獲能 精子中的半數含Y染色體(23,Y),半數含X染色體(23,X)。射出的精子雖有運動能力,卻無穿過卵子周圍放射冠和透明帶的能力。這是由於精子頭的外表有一層能阻止頂體酶釋放的糖蛋白。精子在子宮和輸卵管中運行過程中,該糖蛋白被女性生殖管道分泌物中的酶降解,從而獲得受精能力,此現象稱獲能(capacitation)。精子在女性生殖管道內的受精能力一般可維持1天。
2.卵子的成熟 從卵巢排出的卵子處於第二次成熟分裂的中期,並隨輸卵管傘的液流進入輸卵管,在受精時才完成第二次成熟分裂。若未受精,於排卵后12~24小時退化。
(二)受精
受精(fertilization)是精子穿入卵子形成受精卵的過程,它始於精子細胞膜與卵子細胞膜的接觸,終於兩者細胞核的融合。受精一般發生在輸卵管壺腹部。應用避孕套、輸卵管粘堵或輸精管結紮等措施,可以阻止精子與卵子相遇,從而阻止受精。
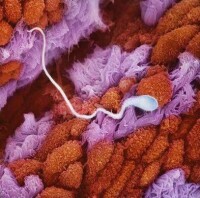
精子識別及與卵細胞表面接觸、融合
受精開始時,精子頭側面的細胞膜與卵細胞膜融合,隨即精子的細胞核和細胞質進入卵內。精子進入卵子后,卵子淺層細胞質內的皮質顆粒立即釋放溶酶體酶樣物質,使透明帶結構發生變化,稱為透明帶反應,從而阻止其它精子穿越透明帶。在極少的情況下,兩個精子同時進入卵子形成三倍體細胞的胚胎,此種胚胎均流產或出生后很快死亡。精子入卵后,卵子迅速完成第二次成熟分裂。此時精子和卵子的細胞核分別稱為雄原核(male pronucleus)和雌原核(female pronucleus)。兩個原核逐漸在細胞中部靠攏,核膜隨即消失,染色體混合,形成二倍體的受精卵(fertilized ovum),又稱合子(zygote)。
受精的意義在於:①受精使卵子的緩慢代射轉入代謝旺盛,從而啟動細胞不斷地分裂;②精子與卵子的結合,恢復了二倍體,維持物種的穩定性;③受精決定性別,帶有Y染色體的精子與卵子結合發育為男性,帶有X染色體的精子與卵子結合則發育為女性;④受精卵的染色體來自父母雙方,加之生殖細胞在成熟分裂時曾發生染色體聯合和片斷交換,使遺傳物質重新組合,使新個體具有與親代不完全相同的性狀。
受精后,母體血漿內很快出現一種免疫抑制物,稱早期妊娠因子(early pregnancy factor),它是目前檢查早期妊娠的一種指征。
卵裂和胚泡形成
受精卵由輸卵管向子宮運行中,不斷進行細胞分裂,此過程稱卵裂(cleavage)。卵裂產生的細胞稱卵裂球(blastomere)。隨著卵裂球數目的增加,細胞逐漸變小,到第3天時形成一個12~16個卵裂球組成的實心胚,稱桑椹胚(morula)。
桑椹胚的細胞繼續分裂,細胞間逐漸出現小的腔隙,它們最後匯合成一個大腔,桑椹胚轉變為中空的胚泡。胚泡(blastocyst,又稱囊胚)於受精的第4天形成並進入子宮腔。胚泡外表為一層扁平細胞。稱滋養層(trophoblast),中心的腔稱胚泡腔(blastocoele),腔內一側的一群細胞,稱內細胞群(inner cell mass)。胚泡逐漸長大,透明帶變薄而消失,胚泡得以與子宮內膜接觸,植入開始。
植入和胚層形成
此階段的主要變化是:胚泡植入子宮內膜,獲得進一步發育的適宜環境和充足的營養供應;內細胞群分化為由內、中、外三個胚層構成的胚盤,它是人體各器官和組織的原基;胎膜與胎盤也漸形成和發育。
(一)植入
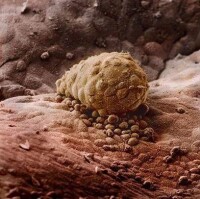
植入8天及12天
植入時的子宮內膜處於分泌期,植入后血液供應更豐富,腺體分泌更旺盛,基質細胞變肥大,富含糖原和脂滴,內膜進一步增厚。子宮內膜的這些變化稱蛻膜反應,此時的子宮內膜稱蛻膜(decidua)。根據蛻膜與胚的位置關係,將其分為三部分:①基蛻膜(decidua basalis),是位居胚深部的蛻膜;②包蛻膜(decidua capsularis),是覆蓋在胚宮腔側的蛻膜;③壁蛻膜(decidua parietalis),是子宮其餘部份的蛻膜。
胚泡的植入部位通常在子宮體和底部,最多見於後壁。若植入位於近子宮頸處,在此形成胎盤,稱前置胎盤(placenta previa),分娩時胎盤可堵塞產道,導致胎兒娩出困難。若植入在子宮以外部位,稱宮外孕(ectopic pregnancy),常發生在輸卵管,偶見於子宮濶韌帶、腸系膜,甚至卵巢表面等處。宮外孕胚胎多早期死亡。
胚泡的植入是以母體性激素的正常分泌使子宮內膜保持在分泌期為基礎的,透明帶消失和胚泡適時進入宮腔是植入的條件。若母體內分泌紊亂或內分泌受藥物干擾,子宮內膜周期性變化則與胚泡的發育不同步,子宮內膜有炎症或有避孕環等導物,均可阻礙胚泡的植入。
人卵體外受精(fertilization in vitro,VIF)技術建立於1969年。用IVF技術獲得的受精卵在體外發育到桑椹胚或早期胚泡,再移植到子宮內的技術稱胚胎移植(embryo transfer,ET)。應用IVF和ET技術於1978年誕生了第一例“試管嬰兒”(test tube baby),我國大陸於1988年春天誕生了首例“試管嬰兒”。IVF和ET技術的開展,可以解決因輸卵管堵塞而不能懷孕婦女的生育問題。目前,體外受精獲得的早期人胚,經冷凍保存后再移植入子宮的胚胎也獲得成活。
(二)胚層形成
在第二周胚泡植入時,內細胞群的細胞也增殖分化,逐漸形成一個圓盤狀的胚盤(embryonic disc),此時的胚盤由內、外兩個胚層。外胚層(ectoderm)為鄰近滋養層的一層柱狀細胞,內胚層(endoderm)是位居胚泡腔側的一層立方細胞,兩層緊貼在一起。繼之,在外胚層的近滋養層側出現一個腔,為羊膜腔,腔壁為羊膜。羊膜與外胚層的周緣續連,故外胚層構成羊膜腔的底。內胚層的周緣向下延伸形成另一個囊,即卵黃囊,故內胚層構成卵黃囊的頂。羊膜腔的底(外胚層)和卵黃囊的頂(內胚層)緊相貼連構成的胚盤是人體的原基。滋養層、羊膜腔和卵黃囊則是提供營養和起保護作用的附屬結構。此時期的胚泡腔內出現鬆散分佈的胚外中胚層細胞。它們先充填於整個胚泡腔。繼而細胞間出現腔隙,腔隙逐漸匯合增大,在胚外中胚層內形成一個大腔,稱胚外體腔。胚外中胚層則分別附著於滋養層內面及卵黃囊和羊膜的外面,羊膜腔頂壁尾側與滋養層之間的胚外中胚層將兩者連接起來。稱體蒂(body stalk)。
至第3周初,胚盤外層細胞增殖,在胚盤外胚層尾側正中線上形 成一條增厚區,稱原條。原條(primitive streak)的頭端略膨大,為原結(primitive node)。原條的出現,胚盤即可區分出頭尾端和左右側。繼而在原條的中線出現淺溝,原結的中心出現淺凹,分別稱原溝和原凹。原條深面的細胞則逐漸遷移到內外胚層之間,形成鬆散的間充質。原條兩側的間充質細胞繼續向側方擴展,形成胚內中胚層(intraembryonic mesoderm),它在胚盤邊緣與胚外中胚層續連。從原結向頭側遷移的間充質細胞,形成一條單獨的細胞索,稱脊索(notochord),它在早期胚胎起一定支架作用。脊索向頭端生長,原條則相對縮短,最終消失。若原條細胞殘留,在人體骶尾部可分化形成由多種組織構成的畸胎瘤。
胚層分化
從第4周初至第8周末的發育過程,胚胎不僅初具人形,而且胚盤的三胚層分化發育,建成各器官系統的雛形;胎膜和胎盤也於此時期發育形成。此時期的胚胎髮育對環境因素的作用十分敏感,某些有害因素(病毒、藥物等)易通過母體影響胚胎髮育,導致發生某些嚴重的先天性畸形。
(一)胚體形
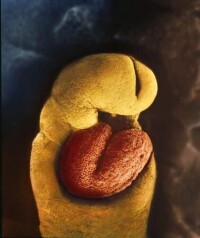
胚胎24天、20周、36周外形
圓柱形胚體形成的結果:胚體凸入羊膜腔的羊水內;體蒂和卵黃囊連於胚體腹側臍處,外包羊膜,形成原始臍帶;口咽膜和泄殖腔膜分別轉到胚體頭和尾的腹側;外胚層包於胚體外表;內胚層卷折到胚體內,形成頭尾方向的原始消化管,管中份的腹側借縮窄的卵黃蒂與卵黃囊通連,管頭端由口咽膜封閉,尾端由泄殖腔膜封閉。至第8周末,胚體外表已可見眼、耳和鼻的原基及發育中的四肢,初具人形。
(二)胚層分化
胚體形成的同時,三個胚層也逐漸分化形成各器官的原基。
1.外胚層的分化 脊索形成后,誘導其背側中線的外胚層增厚呈板狀,稱神經板(neural plate)。神經板隨脊索的生長而增長,且頭側寬於尾側。繼而神經板中央沿長軸下隱形成神經溝(neural groove),溝兩側邊緣隆起稱神經褶(neural fold),兩側神經褶在神經溝中段靠攏並癒合,癒合向兩端延伸,使神經溝封閉為神經管(neural tube)。神經管兩側的表面外胚層在管的背側靠攏並癒合,使神經管位居於表面外胚層的深面。神經管將分化為中樞神經系統以及松果體、神經垂體和視網膜等。在神經褶癒合過程中,它的一些細胞遷移到神經管背側成一條縱行細胞索,繼而分裂為兩條分別位於神經管的背外側,稱神經嵴(neural crest),它將分化為周圍神經系統及腎上腺髓質等結構。位於體表的表面外胚層,將分化為皮膚的表皮及其附屬器,以及牙釉質、角膜上皮、晶狀體、內耳膜迷路、腺垂體、口腔和鼻腔與肛門的上皮等。
2.中胚層的分化 中胚層在脊索兩旁從內側向外側依次分化為軸旁中胚層、間介中胚層和側中胚層。分散存在的中胚層細胞,稱間充質,分化為結締組織以及血管、肌組織等。脊索則大部份退化消失,僅在椎間內殘留為髓核。
(1)軸旁中胚層(paraxial mesoderm):緊鄰脊索兩側的中胚層細胞迅速增殖,形成一對縱行的細胞索,即軸旁中胚層。它隨即裂為塊狀細胞團,稱體節(somite)。體節左右成對,從頸部向尾依次形成,隨胚齡的增長而增多,故可根據體節的數量推算早期胚齡。第5周時,體節全部形成,共約42~44 對。體節將分化為皮膚的真皮、大部份中軸骨骼(如脊柱、肋骨)及骨骼肌。
(2)間介中胚層(intermediate mesoderm):位於軸旁中胚層與側中胚層之間,分化為泌尿生殖系統的主要器官。
(3)側中胚層(lateral mesoderm):是中胚層最外側的部份,兩側的側中胚層在口咽膜的頭側匯合為生心區。隨著胚體的形成,生心區移到胚體原始消化管的腹側,口咽膜的尾側,分化形成心臟。側中胚層迅速裂為兩層。與外胚層鄰近的一層,稱體壁中胚層(parietall mesoderm),將分化為體壁(包括肢體)的骨骼、肌肉、血管和結締組織;與內胚層鄰近的一層,稱臟壁中胚層(visceral mesoderm),覆蓋於原始消化管外面,將分化為消化和呼吸系統的肌組織、血管和結締組織等。兩層之間的腔為原始體腔,最初呈馬躥鐵形,繼而從頭端到尾端分化為心包腔、胸膜腔和腹膜腔。
3.內胚層的分化 在胚體形成的同時,內胚層卷折形成原始消化管。原始消化管將分化為消化管、消化腺、呼吸道和肺的上皮組織,以及中耳、甲狀腺、甲狀旁腺、胸腺、膀胱和陰道等的上皮組織。
胎膜和胎盤是對胚胎起保護、營養、呼吸和排泄等作用的附屬結構,有的還有一定的內分泌功能。胎兒娩出后,胎膜、胎盤與子宮蛻膜一併排出,總稱衣胞。
(一)胎膜
胎膜(fetal membrane)包括絨毛膜、羊膜、卵黃囊、原囊和臍帶。
1.絨毛膜絨毛膜(chorion)由滋養層和襯於其內面的胚外中胚層組成。植入完成後,滋養層已分化為合體滋養層和細胞滋養層兩層,繼之細胞滋養層的細胞局部增殖,形成許多伸入合體滋養層內的隆起,這時,表面有許多突起的滋養層和內面的胚外中胚層合稱為絨毛膜。絨毛膜包在胚胎及其它附屬結構的最外面,直接與子宮培膜接觸,膜的外表有大量絨毛(villi)。絨毛的發育使絨毛膜與子宮蛻膜接觸面增大,利於胚胎與母體間的物質交換。第2周末的絨毛僅由外表的合體滋養層和內部的細胞滋養層構成,稱初級絨毛干。第3周時,胚外中胚層逐漸伸入絨毛干內,改稱次級絨毛干。此後,絨毛干內的間充質分化為結締組織和血管,形成三級絨毛干。絨毛干進而發出分支,形成許多細小的絨毛。同時,絨毛干末端的細胞滋養層細胞增殖,穿出合體滋養層。伸抵蛻膜組織,將絨毛干固著於蛻膜上。這些穿出的細胞滋養層細胞還沿蛻膜擴展,彼此連接,形成一層細胞滋養層殼,使絨毛膜與子宮蛻膜牢固連接。絨毛干之間的間隙,稱絨毛間隙(intervillous space)。絨毛間隙內充以從子宮螺旋動脈來的母體血。胚胎藉絨毛汲取母血中的營養物質並排出代謝產物。
胚胎早期,整個絨毛膜表面的絨毛均勻分佈。之後,由於包蛻膜側的血供匱乏,絨毛逐漸退化、消失,形成表面無絨毛的平滑絨毛膜(smooth chorion)。基蛻膜側血供充足,該處絨毛反覆分支,生長茂密,稱叢密絨毛膜(villous chorion),它與基蛻膜組成胎盤。叢密絨毛膜內的血管通過臍帶與胚體內的血管連通。此後,隨著 胎的發育增長及羊膜腔的不斷擴大,羊膜、平滑絨毛膜和包蛻膜進上步凸向子宮腔,最終與壁蛻膜癒合,子宮腔逐漸消失。
絨毛膜為早期胚胎髮育提供和氧氣,從密絨毛膜參與組成胎盤。在絨毛膜發育過程中,若血管未通連,胚胎可因缺乏營養而發育遲緩或死亡。若絨毛膜發生病變,如滋養層細胞過度增生、絨毛內結締組織變性水腫(水泡狀胎塊)、滋養層細胞癌變(絨毛膜上皮癌)等,不僅嚴重影響胚胎的發育,還危及母體健康。
2.羊膜羊膜(amnion)為半透明薄膜,羊膜腔內充滿羊水(amniotic fluid),胚胎在羊水中生長發育。羊膜最初附著於胚盤的邊緣,隨著胚體形成、羊膜腔擴大和胚體凸入羊膜腔內,羊膜遂在胚胎的腹側包裹在體蒂表面,形成原始臍帶。羊膜腔的擴大逐漸使羊膜與絨毛膜相貼,胚外體腔消失。羊水呈弱鹼性,含有脫落的上皮細胞和一些胎兒的代謝產物。羊水主要由羊膜不斷分泌產生,又不斷地被羊膜吸收和被胎兒吞飲,故羊水是不斷更新的。羊膜和羊水在胚胎髮育中起重要的保護作用,如胚胎在羊水中可較自由的活動,有利於骨骼肌的正常發育,並防止胚胎局部粘連或受外力的壓迫與震蕩。臨產時,羊水還具擴張宮頸沖洗產道的作用。隨著胚胎的長大,羊水也相應增多,分娩時約有1000~15000ml。羊水過少(500ml以下),易發生羊膜與胎兒粘連。影響正常發育,羊水過多(2000ml以上),也可影響胎兒正常發育。羊水含量不正常,還與某些先天性畸形有關,如胎兒無腎或尿道閉鎖可致羊水過少,胎兒消化道閉鎖或神經管封閉不全可致羊水過多,穿刺抽取羊水,進行細胞染色體檢查或測定羊水中某些物質的含量,可以早期診斷某些先天性異常。
3.卵黃囊卵黃囊(yolk sac)位於原始消化管腹側。鳥類胚胎的卵黃很發達,囊內貯有大量卵黃,為胚胎髮育提供營養。人胚胎的卵黃囊內沒有卵黃,卵黃囊不發達,它的出現也是種系發生和進化的反映。人胚胎卵黃囊被包入臍帶后,與原始消化管相連的卵黃蒂於第6周閉鎖,卵黃囊也逐漸退化,但人類的造血幹細胞和原始生殖細胞卻分別來自卵黃囊的胚外中胚層和內胚層。
4.尿囊 尿囊(allantois)是從卵黃囊尾側向體蒂內伸出的一個盲管,隨著胚體的形成而開口於原始消化管尾段的腹側,即與後來的膀胱通連。尿囊閉鎖后形成膀胱至臍的臍正中韌帶。鳥類胚胎的尿囊發達,具氣體交換和儲存代謝廢物的功能。人胚胎的氣體交換和廢物排泄由胎盤完成,尿囊僅為遺跡性器官,但其壁的胚外中胚層形成臍血管。
5.臍帶臍帶(umbilical cord)是連於胚胎臍部與胎盤間的索狀結構。臍帶外被羊膜,內含體蒂分化的粘液性結締組織。結締組織內除有閉鎖的卵黃蒂和尿囊外,還有臍動脈和臍靜脈。臍血管的一端與胚胎血管相連。另一端與胎盤絨毛血管續連。臍動脈有兩條,將胚胎血液運送至胎盤絨毛內,在此,絨毛毛細血管內的胚胎血與絨毛間隙內的母血進行物質交換。臍靜脈僅有一條,將胎盤絨毛彙集的血液送回胚胎。胎兒出生時,臍帶長40~60cm ,粗1.5~2cm,透過臍帶表面的羊膜,可見內部盤曲纏繞的臍血管。臍帶過短,胎兒娩出時易引起胎盤過早剝離,造成出血過多;臍帶過長,易纏繞胎兒肢體或頸部,可致局部發育不良,甚致胎兒窒息死亡。
(二)胎盤
1.胎盤的結構 胎盤(placenta)是由胎兒的叢密絨毛膜與母體的基蛻膜共同組成的圓盤形結構。足月胎兒的胎盤重約500g,直徑15~20cm,中央厚,周邊薄,平均厚約2.5cm。胎盤的胎兒面光滑,表面覆有羊膜,臍帶附於中央或稍偏,透過羊膜可見呈放射狀走行的臍血管分支。胎盤的母體面粗糙,為剝離后的基蛻膜,可見15~30個由淺溝分隔的胎盤小葉(cytoledon)。
在胎盤垂直切面上,可見羊膜下方為絨毛膜的結締組織,臍血管的分支行於其中。絨毛膜發出約40~60根絨毛干。絨毛干又發出許多細小絨毛,乾的末端以細胞滋養層殼固著於基蛻膜上。臍血管的分支沿絨毛干進入絨毛內,形成毛細血管。絨毛干之間為絨毛間隙,由基蛻膜構成的短隔伸入間隙內,稱胎盤隔(placental septum)。胎盤隔將絨毛干分隔到胎盤小葉內,每個小葉含1~4根絨毛干。子宮螺旋動脈與子宮靜脈開口於絨毛間隙,故絨毛間隙內充以母體血液,絨毛浸在母血中。
2、胎盤的血液循環和胎盤膜胎盤內有母體和胎兒兩套血液循環,兩者的血液在各自的封閉管道內循環,互不相混,但可進行物質交換。母體動脈血從子宮螺旋動脈流入絨毛間隙,在此與絨毛內毛細血管的胎兒血進行物質交換后,由子宮靜脈迴流入母體。胎兒的靜脈血經臍動脈及其分支流入絨毛毛細血管,與絨毛間隙內的母體血進行物質交換后,成為動脈血,又經臍靜脈迴流到胎兒。
胎兒血與母體血在胎盤內進行物質交換所通過的結構,稱胎盤膜(placental membrane)或胎盤屏障(placental barrier)。早期胎盤膜由合體滋養層、細胞滋養層和基膜、薄層絨毛結締組織及毛細血管內皮和基膜組成。發育後期,由於細胞滋養層在許多部位消失以及合體滋養層在一些部位僅為一薄層胞質,故胎盤膜變薄,胎血與母血間僅隔以絨毛毛細血管內皮和薄層合體滋養層及兩者的基膜,更有利於胎血與母血間的物質交換。
3.胎盤的功能
(1)物質交換:進行物質交換是胎盤的主要功能,胎兒通過胎盤從母血中獲得營養和O2,排出代謝產物和CO2。因此胎盤具有相當於出生后小腸、肺和腎的功能。由於某些藥物、病毒和激素可以透過胎盤膜影響胎兒,故孕婦用藥需慎重。
(2)內分泌功能:胎盤的合體滋養層能分泌數種激素,對維持妊娠起重要作用。主要為:①絨毛膜促性腺激素(human chorionic gonadotropin,HCG),其作用與黃體生成素類似,能促進母體黃體的生長發育,以維持妊娠,HCG在妊娠第2周開始分泌,第8周達高峰,以後逐漸下降;②絨毛膜促乳腺生長激素(human chorionic somatomammotropin,HCS),能促使母體乳腺生長發育,HCS於妊娠第2月開始分泌,第8月達高峰,直到分娩;③孕激素和雌激素,於妊娠第4月開始分泌,以後逐漸增多。母體的黃體退化后,胎盤的這兩種激素起著繼續維持妊娠的作用。
雙胎(twins)又稱孿生,雙胎的發生率約佔新生兒的1%。雙胎有兩種。
1.雙卵孿生 一次排出兩個卵子分別受精后發育為雙卵孿生(dizygotic twins),占雙胎的大多數。它們有各自的胎膜與胎盤,性別相同或不同,相貌和生理特性的差異如同一般兄弟姐妹,僅是同齡而已。
2.單卵孿生 由一個受精卵發育為兩個胚胎,故此種雙胎兒的遺傳基因完全一樣。它們的性別一致,而且相貌和生理特徵也極相似。單卵孿生(monozygotic twins)可以是:①一個胚泡內出現兩個內細胞群,各發育為一個胚胎,這類孿生兒有各自的羊膜,但共有一個絨毛膜與胎盤;②胚盤上出現兩個原條與脊索;誘導形成兩個神經管,發育為兩個胚胎,這類攣生兒同位於一個羊膜腔內,也共有一個絨毛膜與胎盤;③卵裂球分離為兩團,它們各自發育為一個完整的胚,但人的卵裂球圍以透明帶,卵裂球分離的可能性較小。
(1)一個胚泡內出現兩個內細胞群;(2)一個胚盤形成兩個原條;(3)單卵雙胎聯體畸胎
一次娩出兩個以上新生兒為多胎(multiple birth)。多胎的原因可以是單卵性、多卵性或混合性,常為混合性多胎。多胎髮生率低,三胎約萬分之一,四胎約百萬分之一;四胎以上更為罕見,多不易存活。
在單卵孿生中,當一個胚盤出現兩個原條並分別發育為兩個胚胎時,若兩原條靠得較近,胚體形成時發生局部聯接,稱聯體雙胎(conjoined twins)。聯體雙胎有對稱型和不對稱型兩類。對稱型指兩個胚胎一大一小,小者常發育不全,形成寄生胎或胎中胎。
臨床常以月經齡推算胚胎齡,即從孕婦末次月經的第一天算起,至胎兒娩出共約40周。胚胎學者則常用受精齡,即從受精之日為起點推算胚胎齡,受精一般發生在末次月經第一天之後的2周左右,故從受精到胎兒娩出約經38周。但由於婦女的月經周期常受環境變化的影響,故胚胎齡的推算難免有誤差。
胚胎學研究工作者所獲得的人胚胎標本,大多缺乏產婦月經時間的準確記錄。胚胎學家根據大量胚胎標本的觀察研究,總結歸納出各期胚胎的外形特徵和長度,以作為推算胚胎齡的依據。如第1~3周,主要根據胚的發育狀況和胚盤的結構;第4~5周,常利用體節數及鰓弓與眼耳鼻等始基的出現情況;第6~8周,則依據四肢與顏面的發育特徵。胎齡的推算,主要根據顏面、皮膚、毛髮、四肢、外生殖器等的發育狀況,並參照身長,足長和體重等。
胚胎長度的測量標準有三種:①最長值(greatest length,GL),多用於測量第1~3周的胚;②頂臀長(crown-rump length,CRL),又稱坐高,用於測量第4周及以後的胚胎;③頂跟長(crown-heal length,CHL),又稱立高,常用於測量胎兒。用B超測定孕婦體內胚胎的頂臀長等與直接測量胚胎標本的數據很接近,故應用B超測量是一個值得開展的工作。
從受精卵發育為一個新個體歷經複雜的演變過程,包括細胞增殖、死亡、分化、識別、遷移和功能表達,以及組織和器官的形成等。這些變化具嚴密規律,具有精細的時間順序和空間關係。來自同一受精卵的細胞,它們的基因結構是相同的,胚胎髮育變化中,細胞基因的表達起決定作用,並受內外環境因素的影響。胚胎髮育機理是現代發育生物學中重大的研究課題。
細胞分化
細胞分化(cell differentiation)是指幼稚細胞發育為具有某些特殊結構和功能的過程。如桑椹胚分化為內細胞群和滋養層兩類不同的細胞。內細胞群又分化為三個胚層,三個胚層再分化形成各種組織。又如,造血幹細胞先分化為各種造血相祖細胞,後者再分化為不同的血細胞;骨原細胞分化為成骨細胞或軟骨細胞;精原細胞分化為精子等。這是廣義的分化概念,它包括形態結構和功能的成熟過程。狹義的或更嚴格的分化概念,是指原始的或尚未定向的細胞不可逆地轉變為某種定向細胞的時刻,它稱之為決定(determination)。細胞的決定發生在它的形態結構變化之前,它的主要標誌是能合成某種特殊蛋白質(如酶、受體等),故可以用測定蛋白質、受體或酶等技術研究細胞的分化。
不同種屬動物,其早期胚胎細胞出現決定的時間不同。如無脊椎動物的卵裂球已經決定,故一部分卵裂球不能發育為完整的個體;而哺乳類的卵裂球尚未決定,其一部分卵裂球也可發育為一個完整的胚胎。如人桑椹胚若被分隔成兩團細胞,它們各自可發育為一個胎兒(單卵孿生)。
形態發生
組織和器官的形態發生(morphogenesis)是通過細胞的形態變化和運動、細胞的識別和粘著、細胞增殖和死亡等過程而實現的。
1.細胞形態變化和運動 胚胎的形態發生多與細胞層的鋪展、卷折、陷入、隆起和細胞遷移有關,而這又與細胞內微絲、微管配布引起的細胞形態變化和細胞外基質大分子物質的濃度有關。如外胚層在形成神經板、神經溝和神經管的過程中,細胞內微管先沿其兩極平行縱向排列,細胞則沿縱軸伸長形成神經板,繼而微絲平行排列於細胞頂端,細胞該端變窄,神經板逐漸下陷形成神經溝與神經管。體外培養的細胞向一個方向運動時,細胞則伸長,胞質內的微管也沿伸長和運的方向縱行排列,細胞前緣的細胞膜呈波浪狀前行運動,也是與膜下大量微絲的參與相關的。基質大分子物質如纖維粘連蛋白(fibronectin)、層粘連蛋白(laminin)、膠原、糖胺多糖等也參與細胞的運動,它們可能通過細胞膜的蛋白受體與胞質內微絲連接,從而調節微絲、微管的排列方向而引起運動。細胞通過這種方式識別這些物質的濃度梯度,從而調整運動的方向。
(1)外胚層細胞呈立方形,微絲和微管任意分佈
(2)細胞變長,微管平行於長軸排列,形成神經板
(3)細胞頂部縮窄,微絲與表面平行分佈,形成神經管
2.細胞識別和粘著 胚胎髮育中,同類或相關細胞能彼此識別,經過遷移能按一定的模式類聚和粘著在一起,構成組織。近年認為,這是由於細胞膜上的糖蛋白受體與相關細胞細胞衣內的糖鏈結合的結果。
3.細胞增殖和死亡 胚胎時期的細胞增殖十分旺盛,其調控機制,尚不完全清楚。已知與多種刺激相應細胞增殖的化學因子有關,如生長激素、性激素、神經生長因子、表皮生長因子、血細胞生長因子、成纖維細胞生長因子、血細胞發生的多種集落刺激因子等。許多組織的細胞還產生抑素,可抑制自身的增殖。細胞內cAMP濃度下降時,細胞分裂加快,反之減慢。
胚胎髮生中廣泛存在細胞定時死亡現象,稱程序性細胞死亡(apoptosis)。它是器官正常發生的重要因素,唯其機制不明。如人胚的尾芽和鰓的定期消失;早期手和足都形似槳板,在預定指或趾之間的細胞死亡后,才能形成指或趾。又如循環系統發生過程中的某段動脈或靜脈的定時退化、女性中腎管的定期退化、男性中腎旁管的定期消失等都屬此例。
胚胎組織的相互影響
在胚胎的細胞分化和形態發生中,組織或細胞之間常是互以對方為條件而相互影響的。當相互作用的一方導致另一方的發育發生變化時,稱此現象為誘導(induction)。誘導的實例甚多,如脊索誘導其背側的外胚層發生神經管;眼發生中的視泡誘導表面外胚層發生晶狀體;肢芽中胚層誘導表面外胚層形成頂嵴,後者決定肢體的形態發育。還有多層次誘導現象,如視泡誘導形成晶狀體,後者再誘導表面外胚層和鄰近的間充質形成角膜。相互誘導作用的事例如在是腎的發生中,輸尿管芽誘導生后腎組織形成腎小管,生后腎組織又誘導輸尿管芽分支形成集合小管。誘導作用具有嚴格的組織特異性和發育時期的限制,若過程受到干擾,改變原有的時空關係,就可能發生先天性畸形。關於誘導作用的機理,雖有不少實驗研究,但迄今仍無明確結論。
2015年4月,中國科學家團隊首次成功修改人類胚胎的DNA,這在國內獲得不少科學家的支持,但卻在西方引起爭議。位於廣州的中山大學生物學副教授黃軍就和他的同事,利用最新科技“切開”一個基因,該基因主要與地中海貧血症有關。在中國南方,地中海貧血症是兒童中最常見、但有時可能致命的血液異常。
但這一研究在科學界引發了一些批評。有關首次修改人類胚胎基因的研究的論文最初是投給《自然》與《科學》期刊的,但由於道德問題,論文被期刊拒絕。論文的作者們在另一本期刊《蛋白質與細胞》中發文表示,他們明白圍繞有關研究的道德爭議。
他們表示,研究使用的是醫院丟棄的有問題的胚胎,也就是接受了數個精子的卵子,而這些胚胎在世界各地的實驗室都已經被廣泛使用了數十年,因為它們不會成功孕育出嬰兒。
英國生物學家Edward Lanphier向《自然》雜誌表達了他的批評。他說,我們要暫停這一研究,並確保我們就前進的方向進行廣泛的討論。目前黃軍就未能被聯繫上就事件置評,但他的研究在國內贏得了不少生物學家的支持。清華大學生物學教授陳國強表示,有關批評所提出的要求過於武斷。
黃軍就的團隊用了86個廢棄胚胎做實驗,並發現,DNA編輯只在其中28個胚胎中成功,也就是成功率大約30%。除此以外還有其他值得警惕的問題。新的基因編輯技術,名為CRISPR,經常找錯目標基因,在之後的處理環節中,就會發現胚胎中有一些變異。黃軍就和他的團隊在他們的論文中指出,要小心使用這種技術。