甲酸
無色而有刺激性氣味的液體
甲酸是一種有機物,化學式為HCOOH,分子量46.03,俗名蟻酸,是最簡單的羧酸。無色而有刺激性氣味的液體。弱電解質,酸性很強,有腐蝕性,能刺激皮膚起泡。存在於蜂類、某些蟻類和毛蟲的分泌物中。是有機化工原料,也用作消毒劑和防腐劑。
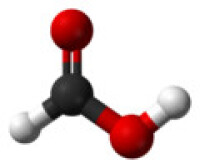
分子結構模型
甲酸具有與大多數其他羧酸相同的性質,儘管在通常情況下甲酸不會生成醯氯或者酸酐。甲酸脫水分解為一氧化碳和水。甲酸具有和醛類似的還原性。它能起銀鏡反應,把銀氨絡離子中的銀離子還原成金屬銀,而自己被氧化成二氧化碳和水:
HCOOH+2AgOH→2Ag+2H2O+CO2
甲酸是唯一能和烯烴進行加成反應的羧酸。甲酸在酸的作用下(如硫酸,氫氟酸),和烯烴迅速反應生成甲酸酯。
儲運條件:本品應密封於陰涼乾燥處避光保存。

甲酸
是先將一氧化碳與甲醇於80℃和4MPa條件下,以甲醇鈉為催化劑進行反應,生成甲酸甲酯,然後在酸性催化劑存在下,使甲酸甲酯於90~140℃和0.5~1.8MPa條件下水解得甲醇和甲酸,經分離精製可獲得85%以上的濃甲酸。甲醇則返回羰基化反應器。反應式如下:
CO+CH3OH─→HCOOCH3
HCOOCH3+H2O─→HCOOH+CH3OH
由於酯的水解是可逆反應,故又可以先使甲酸酯與氨在80~100℃和0.4~0.6MPa下反應製得甲醯胺,再在85℃用70%的硫酸連續水解製得甲酸。
工業上甲酸生產主要有甲酸鈉法、甲醯胺法、丁烷(或輕油)液相氧化法和甲酸甲酯水解法四種工藝路線。
甲酸鈉法是甲酸的傳統生產方法,但勞動條件差,污染嚴重。不少工業化國家已淘汰該法,但中國絕大多數甲酸生產企業仍採用此法。德國BASF公司開發的甲醯胺法工藝因生產成本太高,隨後也遭淘汰。丁烷(或輕油)液相氧化工藝是一種生產醋酸同時聯產甲酸的生產方法,每生產1t乙酸,副產0.05~0.25t甲酸,上世紀70年代曾是國外生產甲酸的主要方法,後來隨著甲醇低壓羰基合成醋酸技術的工業化,使該法已無發展前途,現在大部分丁烷(或輕油)液相氧化裝置已相繼停產。國外甲酸生產主要採用甲酸甲酯水解工藝,約佔甲酸總產能的80%以上。
甲酸甲酯水解法工藝過程為:(1)甲醇與CO羰基化合成甲酸甲酯;(2)甲酸甲酯水解生成甲酸和甲醇,甲醇循環使用。依工藝的不同特點,該法又可分為Kemira-Leonard工藝、Bethlechem Stell工藝、BASF工藝和USSR工藝。這四種水解工藝各有所長,以Kemira-Leonard工藝投資最省,工藝過程最為經濟合理。
在新技術路線開發方面,其主要研發路線有:
(1)甲酸前體-甲酸甲酯製備技術,此領域有甲醇催化脫氫法、甲醇氧化脫氫法、CO2與甲醇加氫縮合法、合成氣直接合成法等,其中,甲醇羰基化制甲酸甲酯工藝和甲醇催化脫氫制甲酸甲酯工藝近年來國內外研究較多,有一定工業化應用前景。
(2)甲醛一步法直接氧化催化生成甲酸。BIC開發的這項技術採用V-Ti-O催化劑,溫度範圍約為100~140℃,甲酸初始選擇性可達到約96%~98%,催化劑產出率達到70g甲酸/L·h,該法已進行了實驗室實驗和中試。
(3)CO2直接加氫製取甲酸。這項技術從90年代中期開始,採用釕系催化劑,在20.5MPa、50℃和三乙胺存在下合成甲酸。從環保角度來看,這一路線具有一定開發意義,但離工業化還有較長的距離,仍然處於基礎探索階段。
(4)甲酸鈉法:一氧化碳和氫氧化鈉溶液在160-200℃和2MPa壓力下反應生成甲酸鈉,然後經硫酸酸解、蒸餾即得成品。
(5)甲醇羰基合成法(又稱甲酸甲酯法):甲醇和一氧化碳在催化劑甲醇鈉存在下反應,生成甲酸甲酯,然後再經水解生成甲酸和甲醇。甲醇可循環送入甲酸甲酯反應器,甲酸再經精餾即可得到不同規格的產品。
(6)甲醯胺法:一氧化碳和氨在甲醇溶液中反應生成甲醯胺,再在硫酸存在下水解得甲酸,同時副產硫酸銨。原料消耗定額:甲醇31 kg/t、一氧化碳702 kg/t、氨314 kg/t、硫酸1010 kg/t。另外,丁烷枵輕油氧化法主要用來生產乙酸,甲酸作為副產品回收,處於研究階段的方法有一氧化碳和水直接合成法。
精製方法:無水甲酸可在減壓下直接分餾製得,分餾時用冰水冷卻凝結。對含水甲酸,可用硼酐或無水硫酸銅做乾燥劑。五氧化二磷和氯化鈣能與甲酸作用,不宜用作乾燥劑。對試劑級88%的甲酸,可用鄰苯二甲酸酐迴流6小時后蒸餾的方法除去其中的水分。進一步純化可利用分步結晶法。甲酸與乙酸混在一起時,可加入脂肪烴進行共沸蒸餾分離。
(7)將適量的一氧化碳和氫氧化鈉水溶液在160~200 ℃下反應生成甲酸鈉,經中和、蒸餾、冷凝而得。或者在三乙胺水溶液中,以鈀絡合物為催化劑,二氧化碳與氫氣於140~160℃反應製得。
(8)以甲酸鈉與濃硫酸作用製得工業級甲酸,然後可用活性炭吸附后減壓蒸餾以製得純品,也可加入B2O3CuSO4進行減壓蒸餾精製。
(9)二氧化碳法:在鈀絡合物催化下,在三乙胺水溶液中,二氧化碳與氫氣於140~160 ℃反應而得。
(10)主要採用合成酸化法和高壓催化法。合成酸化法:用焦炭燃燒產生的一氧化碳與氫氧化鈉合成甲酸鈉,再用硫酸酸化,經蒸餾而得。高壓催化法:將一氧化碳和水蒸氣在催化劑存在下,於高溫高壓下反應而得。
(11)將甲酸與五氧化二磷混合,進行減壓蒸餾,反覆5-10次,方可得到無水甲酸,但得量低,費時長,會造成一些分解。將甲酸與硼酸醉進行蒸餾,操作簡便,效果更好。將硼酸置甩壺中高溫脫水至不再產生氣泡,所得熔融物倒在鐵片上,置乾燥器中冷卻,然後研磨成粉。將硼酸酚細粉加到甲酸中,放置幾日,形成硬塊,分出清徹液體進行減壓蒸餾,收集22-25 ℃/12-18 mm餾份為產品。蒸餾器應是全磨口接頭並有乾燥管保護。
在無水丙三醇中加熱草酸,后蒸汽蒸餾得到。或在鹽酸作用下水解異乙腈得到:,異乙腈的製備由乙胺和氯仿反應獲得。(因異乙腈具有令人不愉快的氣味,此反應必須在通風櫥中進行。)
GB/T 2093-2011 工業用甲酸
甲酸含量:以酚酞作指示劑,用氫氧化鈉溶液滴定。
鐵(Fe):按GB/T 3049-2006規定進行。
蒸發殘渣:按GB/T 6026-1998規定進行。

甲酸
(3)化學工業:甲酸鈣、甲酸鈉、甲酸銨、甲酸鉀、甲酸乙酯、甲酸鋇、二甲基甲醯胺、甲醯胺、橡膠防老劑、季戊四醇、新戊二醇、環氧大豆油、環氧大豆油酸辛酯、特戊醯氯、脫漆劑、酚醛樹脂、酸洗鋼板等。
(4)皮革工業:皮革的鞣製劑、脫灰劑和中和劑。
(5)橡膠工業:天然橡膠凝聚劑。
(6)其它:還可以製造印染煤染劑,纖維和紙張的染色劑、處理劑、增塑劑、食品保鮮和動物飼料添加劑等。
(7)製取CO 。化學式: HCOOH(濃H2SO4催化)加熱=CO+H2O。
(9)甲酸及其水溶液能溶解許多金屬、金屬氧化物、氫氧化物及鹽,所生成的甲酸鹽都能溶解於水,因而可作為化學清洗劑。甲酸不含氯離子,可用於含不鏽鋼材料的設備的清洗。
1、疏水參數計算參考值(XlogP):-0.2
2、氫鍵供體數量:1
3、氫鍵受體數量:2
4、可旋轉化學鍵數量:0
5、互變異構體數量:無
6、拓撲分子極性表面積(TPSA):37.3
7、重原子數量:3
8、表面電荷:0
9、複雜度:10.3
10、同位素原子數量:0
11、確定原子立構中心數量:0
12、不確定原子立構中心數量:0
13、確定化學鍵立構中心數量:0
14、不確定化學鍵立構中心數量:0
15、共價鍵單元數量。
急性毒性:LD50:1100 mg/kg(大鼠經口)。LC50:15000 mg/m3,15 min(大鼠吸入)。人吸入750 mg/m3(15 s),劇烈刺激黏膜引起咽痛,咳嗽,胸痛;人經口約30 g,腎功能衰竭或呼吸功能衰竭而死亡。
亞急性和慢性毒性:小鼠飲水中含0.01%~0.25%遊離甲酸,2~4個月內無任何影響;含0.5%則影響食慾並使其生長緩慢。小鼠吸入10 g/m3以上時,1~4 d后死亡。
代謝:甲酸可通過消化道、呼吸道和皮膚吸收。在體內部分被氧化,部分以原形由尿排出,以原形排出的量受給毒劑量、途徑、濃度等因素的影響,一般佔總攝入量的18%~25%。
中毒機理:甲酸能以羧基(-COOH)或以醛基(H-C=O)的形式起作用,故與其他同族酸相比毒性較大。發病機理主要是對機體的刺激、腐蝕作用而引起各種損傷。
刺激性:家兔經眼:122 mg,重度刺激。家兔經皮開放性刺激試驗:610 mg,輕度刺激。
致突變性:微生物致突變:大腸桿菌71 ppm(3 h)。姊妹染色單體交換:人淋巴細胞10 mmol/L。
生態學資料:其它有害作用:該物質對環境有危害,應特別注意對水體的污染。
健康危害:主要引起皮膚、粘膜的刺激癥狀。接觸后可引起結膜炎、眼瞼水腫、鼻炎、支氣管炎,重者可引起急性化學性肺炎。濃甲酸口服后可腐蝕口腔及消化道粘膜,引起嘔吐、腹瀉及胃腸出血,甚至因急性腎功能衰竭或呼吸功能衰竭而致死。皮膚接觸可引起炎症和潰瘍。偶有過敏反應。
環境危害:對環境有危害,對水體可造成污染。
燃爆危險:本品可燃,具強腐蝕性、刺激性,可致人體灼傷。
危險特性:可燃。其蒸氣與空氣可形成爆炸性混合物,遇明火、高熱能引起燃燒爆炸。與強氧化劑接觸可發生化學反應。具有較強的腐蝕性。
有害燃燒產物:一氧化碳。
滅火方法:消防人員須穿全身防護服、佩戴氧氣呼吸器滅火。用水保持火場容器冷卻,並用水噴淋保護去堵漏的人員。
滅火劑:抗溶性泡沫、乾粉、二氧化碳。
眼睛防護:呼吸系統防護中已作防護。
身體防護:穿橡膠耐酸鹼服。
手防護:戴橡膠耐酸鹼手套。
其他防護:工作現場禁止吸煙、進食和飲水。工作完畢,淋浴更衣。注意個人清潔衛生。
迅速撤離泄漏污染區人員至安全區,並進行隔離,嚴格限制出入。切斷火源。建議應急處理人員戴自給正壓式呼吸器,穿防酸鹼工作服。不要直接接觸泄漏物。儘可能切斷泄漏源。防止流入下水道、排洪溝等限制性空間。小量泄漏:用砂土或其它不燃材料吸附或吸收。也可以將地面灑上蘇打灰,然後用大量水沖洗,洗水稀釋後放入廢水系統。大量泄漏:構築圍堤或挖坑收容。用泡沫覆蓋,降低蒸氣災害。噴霧狀水冷卻和稀釋蒸汽。用泵轉移至槽車或專用收集器內,回收或運至廢物處理場所處置。
診斷要點:
(1)吸入低濃度蒸氣,可致眼結膜及呼吸道刺激癥狀,如鼻咽部不適、咽痛、咳嗽、胸痛、呼吸困難等;吸入高濃度后可有流淚、流涕、噴嚏、咳嗽、咽痛及聲音嘶啞等,重者可發生結膜炎、眼瞼水腫、鼻炎、支氣管炎,甚至可引起急性化學性肺炎。
(2)皮膚接觸主要引起刺激癥狀,表現為皮膚髮紅、結膜充血。7%甲酸溶液亦可引起皮膚灼傷,有水皰,灼傷處無痛,癒合后不留瘢痕。
(3)吞飲后出現流涎、口腔和咽喉有灼熱感,並伴有嘔吐、腹瀉及劇烈的腹痛。濃甲酸可腐蝕口腔及消化道黏膜,引起嘔吐、腹瀉及胃腸出血,並可引起腎損害,重者可死亡。
處理原則:
(1)吸入中毒,予以吸氧。可給予2%~4%的碳酸氫鈉溶液霧化吸入,防治化學性肺炎。
(2)眼部損害可用生理鹽水或2%碳酸氫鈉溶液沖洗。如現場無上述溶液則應立即用大量清水沖洗。重者可用腎上腺糖皮質激素及抗生素眼藥水交替點眼,必要時請眼科處理。
(3)皮膚接觸后,用清水、生理鹽水或4%碳酸氫鈉溶液清洗。
(5)對症治療。
預防措施:生產中有甲酸蒸氣發生時,應有合理通風,工人宜戴防毒面具。接觸者宜戴橡皮手套、圍裙等。甲酸灼傷部位可先用清水沖洗,再用弱鹼溶液中和,蓋以消毒敷料。
健康危害:主要引起皮膚、粘膜的刺激癥狀。接觸后可引起結膜炎、眼瞼水腫、鼻炎、支氣管炎,重者可引起急性化學性肺炎。濃甲酸口服后可腐蝕口腔及消化道粘膜,引起嘔吐、腹瀉及胃腸出血,甚至因急性腎功能衰竭或呼吸功能衰竭而致死。皮膚接觸可引起炎症和潰瘍。偶有過敏反應。
急性毒性:LD501100mg/kg(大鼠經口),LC5015000mg/m3(大鼠吸入,15min)。
刺激性:家兔經皮:610mg,輕度刺激(開放性刺激試驗);家兔經眼:122mg,重度刺激。
亞急性與慢性毒性:小鼠飲水中含0.01%~0.25%遊離甲酸,2~4個月內無任何影響;0.5%則影響食慾並使其生長緩慢。小鼠吸入10g/m3以上時,1~4d后死亡。
致突變性:微生物致突變,大腸桿菌70ppm(3h)。姐妹染色單體互換,人淋巴細胞10mmol/L。細胞遺傳學分析,倉鼠卵巢10mmol/L。
生態毒性:LC50:175mg/L(24h)(藍鰓太陽魚);46mg/L(96h)(金魚);122mg/L(48h)(金色圓腹雅羅魚,靜態);34mg/L(48h)(水蚤)。
生物降解性:MITI-I測試,初始濃度100ppm,污泥濃度30ppm,2周后降解100%。
非生物降解性:空氣中,當羥基自由基濃度為5.00×105個/cm3時,降解半衰期為36d(理論)。
吸入:迅速脫離現場至空氣新鮮處。保持呼吸道通暢。如呼吸困難,給輸氧。如呼吸停止,立即進行人工呼吸。就醫。
誤食:用水漱口,給飲牛奶或蛋清。就醫。
皮膚接觸:立即脫去被污染衣著,用大量流動清水沖洗,至少15分鐘。就醫。
眼睛接觸:立即提起眼瞼,用大量流動清水或生理鹽水徹底沖洗至少15分鐘。就醫。
迅速撤離泄漏污染區人員至安全區,並進行隔離,嚴格限制出入。切斷火源。建議應急處理人員戴自給正壓式呼吸器,穿防酸鹼工作服。不要直接接觸泄漏物。儘可能切斷泄漏源。防止流入下水道、排洪溝等限制性空間。
小量泄漏:用砂土或其它不燃材料吸附或吸收。也可以將地面灑上蘇打灰,然後用大量水沖洗,洗水稀釋後放入廢水系統。
大量泄漏:構築圍堤或挖坑收容。用泡沫覆蓋,降低蒸氣災害。噴霧狀水冷卻和稀釋蒸汽。用泵轉移至槽車或專用收集器內,回收或運至廢物處理場所處置。
工程式控制制:生產過程密閉,加強通風。提供安全淋浴和洗眼設備。
呼吸系統防護:可能接觸其蒸氣時,必須佩戴自吸過濾式防毒面具(全面罩)或自吸式長管面具。緊急事態搶救或撤離時,建議佩戴空氣呼吸器。
眼睛防護:呼吸系統防護中已作防護。
身體眼睛防護:穿橡膠耐酸鹼服。
手防護:戴橡膠耐酸鹼手套。
其他防護:工作現場禁止吸煙、進食和飲水。工作完畢,淋浴更衣。注意個人清潔衛生。
危險特性:可燃;其蒸氣與空氣可形成爆炸性混合物,遇明火、高熱能引起燃燒爆炸。與強氧化劑接觸可發生化學反應。具有較強的腐蝕性。
有害燃燒產物:一氧化碳
滅火劑:抗溶性泡沫、乾粉、二氧化碳。
滅火注意事項:消防人員須穿全身防護服、佩戴氧氣呼吸器滅火。用水保持火場容器冷卻,並用水噴淋保護去堵漏的人員。
用焚燒法或甲醇羰基化法處置。
職業接觸限值:
中國MAC(mg/m3):未制定標準。
前蘇聯MAC(mg/m3):1。
TLVTN:OSHA 5ppm,9.4mg/m3; ACGIH 5ppm,9.4mg/m3。
TLVWN:ACGIH 10ppm,19mg/m3。
密閉操作,加強通風。操作人員必須經過專門培訓,嚴格遵守操作規程。建議操作人員佩戴自吸過濾式防毒面具(全面罩),穿橡膠耐酸鹼服,戴橡膠耐酸鹼手套。遠離火種、熱源,工作場所嚴禁吸煙。使用防爆型的通風系統和設備。防止蒸氣泄漏到工作場所空氣中。避免與氧化劑、鹼類、活性金屬粉末接觸。搬運時要輕裝輕卸,防止包裝及容器損壞。配備相應品種和數量的消防器材及泄漏應急處理設備。倒空的容器可能殘留有害物。
儲存於陰涼、通風的庫房。遠離火種、熱源。庫溫不超過30℃,相對濕度不超過85%。保持容器密封。應與氧化劑、鹼類、活性金屬粉末分開存放,切忌混儲。配備相應品種和數量的消防器材。儲區應備有泄漏應急處理設備和合適的收容材料。
鐵路運輸時應嚴格按照鐵道部《危險貨物運輸規則》中的危險貨物配裝表進行配裝。起運時包裝要完整,裝載應穩妥。運輸過程中要確保容器不泄漏、不倒塌、不墜落、不損壞。嚴禁與氧化劑、鹼類、活性金屬粉末、食用化學品等混裝、混運。運輸時運輸車輛應配備相應品種和數量的消防器材及泄漏應急處理設備。運輸途中應防曝晒、雨淋,防高溫。公路運輸時要按規定路線行駛,勿在居民區和人口稠密區停留。
危險品運輸編號
UN1779
安全說明
S23:不要吸入蒸汽。
S26:萬一接觸眼睛,立即使用大量清水沖洗並送醫診治。
S45:出現意外或者感到不適,立刻到醫生那裡尋求幫助(最好帶去產品容器標籤)。
危險類別碼
R35:引起嚴重灼傷。
易燃。能與水、乙醇、乙醚和甘油任意混溶,和大多數的極性有機溶劑混溶,在烴中也有一定的溶解性。
相對密度(d204)1.220。折光率1.3714。燃燒熱254.4 kJ/mol,臨界溫度306.8 ℃,臨界壓力8.63 MPa。閃點68.9 ℃(開杯)。密度1.22g/cm,飽和蒸氣壓(24℃)5.33 kPa。
濃度高的甲酸在冬天易結冰。
禁配物:強氧化劑、強鹼、活性金屬粉末。
危險特性:其蒸氣與空氣形成爆炸性混合物,遇明火、高熱能引起燃燒爆炸。與強氧化劑可發生反應。
溶解性:與水混溶,不溶於烴類,可混溶於乙醇、乙醚,溶於苯。
甲酸在濃硫酸的催化作用下分解為CO和H2O,由於甲酸的結構特殊,它的一個氫原子和羧基直接相連。也可看做是一個羥基甲醛。因此甲酸同時具有酸和醛的性質。
甲酸具有與大多數其他羧酸相同的性質,儘管在通常情況下甲酸不會生成醯氯或者酸酐。甲酸脫水分解為一氧化碳和水。甲酸具有和醛類似的還原性。它能起銀鏡反應,把銀氨絡離子中的銀離子還原成金屬銀,而自己被氧化成二氧化碳和水。
甲酸是唯一能和烯烴進行加成反應的羧酸。甲酸在酸的作用下(如硫酸,氫氟酸),和烯烴迅速反應生成甲酸酯。但是類似於Koch反應的副反應也會發生,產物是更高級的羧酸。
辛醇/水分配係數的對數值:-0.54,爆炸上限%(V/V):57.0,爆炸下限%(V/V):18.0。
甲酸為強的還原劑,能發生銀鏡反應。在飽和脂肪酸中酸性最強,離解常數為2.1×10。在室溫慢慢分解成一氧化碳和水。與濃硫酸一起加熱至60~80℃,分解放出一氧化碳。甲酸加熱到160℃以上即分解放出二氧化碳和氫。甲酸的鹼金屬鹽加熱至400℃生成草酸鹽。
1、摩爾折射率:8.40
2、摩爾體積(cm/mol):39.8
3、等張比容(90.2K):97.5
4、表面張力(dyne/cm):35.8
5、極化率(10cm):3.33
用於調配蘋果、番木瓜、菠蘿蜜、麵包、乾酪、乳酪、奶油等食用香精及威士忌酒、朗姆酒用香精。在最終加香食品中濃度約為l~18mg/kg。
